Abordagem
Uma história e exame clínico completos são os primeiros passos para o diagnóstico. Os relatos dos cuidadores sobre mudanças nos sintomas comportamentais e psicológicos são a principal fonte de informação para os médicos, e devem ser avaliados por meio de entrevistas com os cuidadores.[72] Quando um clínico geral suspeitar de demência frontotemporal (DFT) em um adulto de <70 anos de idade, ou quando houver história familiar de demência, ele deve encaminhar o paciente a um especialista em, ou serviço de, avaliação de memória para uma avaliação abrangente.[73]
Diagnosticar a DFT continua sendo um desafio, e essa doença é subdiagnosticada. Isso ocorre em parte devido à sobreposição de sintomas entre a variante comportamental da DFT (vcDFT) e diversos transtornos psiquiátricos primários.[28][74] Apesar das características sobrepostas, há elementos clínicos que podem diferenciar a vcDFT dos transtornos psiquiátricos primários.[75]
Usar uma abordagem algorítmica pode auxiliar no processo de descartar ou confirmar as condições psiquiátricas primárias de maneira sistemática.[76]
O Neuropsychiatric International Consortium for Frontotemporal Dementia propôs uma lista de recomendações para a avaliação da vcDFT para melhorar sua diferenciação dos transtornos psiquiátricos primários.[28][77]
[Figure caption and citation for the preceding image starts]: Características clínicas que auxiliam no diagnóstico diferencial entre a variante comportamental da DFT (vcDFT) e a doença psiquiátrica primáriaAntonioni A et al. Ex Rev of Neuro 2025; 25(3): 323-57; usado com permissão da Informa UK Limited, comercializada como Taylor & Francis Group, www.tandfonline.com [Citation ends].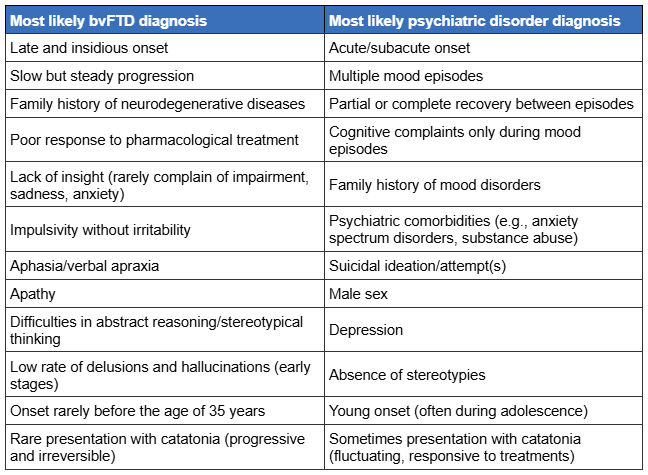
História
Uma história completa deve ser obtida de uma pessoa que tenha estado familiarizada com o paciente antes do início da doença de maneira independente. É necessário um relato completo de todas as mudanças na conduta social interpessoal do paciente, na regulação da conduta pessoal (por exemplo, desinibição), nas emoções (por exemplo, apatia, empatia), comportamentos estereotipados, hábitos alimentares, habilidades cognitivas e consciência sobre sua doença, bem como aspectos duradouros do temperamento, caráter, atitudes e hábitos.[72]
As características comuns no início são:
Início insidioso de embrutecimento na personalidade e alterações no comportamento e nos hábitos sociais
Perda gradualmente progressiva da fluência ou compreensão da linguagem
Falta de cuidados pessoais progressiva e abandono de trabalho, atividades e contatos sociais.
É essencial determinar uma cronologia dos sintomas. Na DFT, as alterações de personalidade, linguagem, hábitos e atividades geralmente precedem o desenvolvimento de comprometimento da memória, desorientação ou apraxias. A maioria dos pacientes com DFT apresentará um ou mais sintomas comportamentais e psicológicos de demência, como apatia, desinibição, alterações no apetite e na alimentação, irritabilidade, agitação e agressividade, comportamento motor aberrante, problemas de sono, e deambulação, durante a evolução da doença.[78][79] A desinibição pode se apresentar como impulsividade, perda de etiqueta, ações excessivas ou perseverativas, inadequação sexual e hipersexualidade, e outros comportamentos transgressivos, como furtos em lojas.[80][81] Psicose e/ou depressão podem estar presentes, mas com menos frequência do que em outros tipos de demência, e os sintomas de depressão podem preceder o início da DFT.[78][79][82]
A DFT pode estar associada a quedas e a sintomas de parkinsonismo. Tais características são sugestivas de DFT com parkinsonismo, síndrome corticobasal e paralisia supranuclear progressiva. A DFT também pode estar associada a perda e fraqueza musculares, sugerindo esclerose lateral amiotrófica (ELA). Além disso, perguntar sobre sintomas motores como fraqueza, falta de coordenação, dificuldades de mobilidade, tremores, espasmos, dificuldades no equilíbrio, dificuldade para subir escadas, predisposição a quedas e problemas de deglutição pode sugerir parkinsonismo (relacionado à síndrome corticobasal [SCB] ou paralisia supranuclear progressiva [PSP]) ou ELA.
Como a afasia progressiva primária (APP) constitui o outro grupo principal no espectro da DFT, a anamnese deve incluir quaisquer alterações subjetivas ou observadas na proficiência da linguagem ou na comunicação.
Uma história familiar completa é necessária se houver suspeita de DFT. O escore de Goldman é uma medida de força da história familiar que leva em consideração o grau de relatividade dentro das famílias.[83] Uma história familiar positiva deve se estender para além da DFT e da demência de início na juventude para incluir doença de Parkinson e distúrbios relacionados, ELA e transtornos psiquiátricos de início tardio inexplicáveis.[28]
O médico deve perguntar sobre episódios prévios com sintomas de transtorno mental (tratados ou não), como mania ou depressão recorrentes, que podem apontar para um transtorno psiquiátrico primário em vez da DFT. Também é improvável que compulsões angustiantes sejam causadas por uma DFT.
Deve ser explorada a possibilidade de haver condições como hipertireoidismo (perguntando-se, por exemplo, sobre intolerância ao calor, perda de peso, apesar da ingestão excessiva de alimentos, tremores e palpitações), pois as características do hipertireoidismo, como irritabilidade, inquietação, aumento da ingestão de alimentos (com diminuição da saciedade) e distraibilidade podem mimetizar as apresentações da DFT.
A documentação cuidadosa das formas de incapacidade compõe a base do planejamento do tratamento. As incapacidades incluem desorientação, comprometimento da comunicação, falhas no autocuidado e na socialização, perda de controle vesical e intestinal e incapacidade de se vestir.
Exame
Os pacientes com DFT podem não apresentar anormalidade neurológica ou comprometimento cognitivo no início da doença. Alguns pacientes apresentam sinais motores sutis e/ou deficits cognitivos executivos no início da doença. Sinais sutis sugestivos de disfunção do lobo frontal surgem à medida que a doença evolui, incluindo comportamento de utilização e um ou mais reflexos como o glabelar, orbicular da boca (snout), de sucção, de procura (rooting) ou de preensão. Muitos pacientes manifestam parkinsonismo, apresentando também alguma combinação de tremor em repouso, hipofonia, lentidão de movimentos, menor variação nas expressões faciais, postura inclinada e instabilidade da marcha. A presença de outros sinais motores, como distonia, clônus e membro estranho, deve ser verificada. Da mesma forma, sinais oculomotores como sacadas verticais lentas e nistagmo vertical devem ser avaliados. Quando presente, a ELA é caracterizada por fraqueza progressiva assimétrica dos músculos espinhais ou bulbares, a qual pode estar acompanhada por fraqueza faríngea. Vários comprometimentos na linguagem, como aqueles relacionados à articulação, fluência, gramática, compreensão, nomeação, repetição, semântica, leitura, escrita, recuperação de palavras e circunlocuções, devem ser observados. Embora não seja comumente uma característica proeminente dos estágios iniciais da DFT, os deficits de memória e outros deficits cognitivos, como agnosia e apraxia, também devem ser observados.
Testes cognitivos
O desempenho nos testes cognitivos deve ser registrado à avaliação inicial e, em seguida, a cada 6 meses. Não é incomum que os escores nos testes cognitivos estejam na faixa normal por até 1 ano após a apresentação, diminuindo de modo constante por cerca de 3-4 anos antes de o paciente não poder ser mais testado. Eles são realizados por especialistas e neuropsicólogos e ajudam no diagnóstico, pois documentam uma predominância de deficits nos domínios executivo e/ou de linguagem da cognição, com relativa preservação da memória, da orientação e da praxia.
O Miniexame do Estado Mental (MEEM) continua sendo o teste cognitivo simples mais amplamente utilizado (e mais bem compreendido). No entanto, os pacientes com DFT podem pontuar acima da pontuação de corte de 24/30, mesmo se tiverem comprometimento cognitivo significativo, portanto ele é de utilidade limitada para a detectar a DFT. Portanto, na prática, outros testes cognitivos geralmente são preferenciais para a DFT:
A Avaliação Cognitiva de Montreal (MoCA) pode ser usada para avaliar o declínio cognitivo ao longo do tempo; alguns subconjuntos podem fornecer informações sobre mau funcionamento do lobo frontal e acompanhar a progressão.[84][85]
O Addenbrooke’s Cognitive Examination III (ACE III) é um teste de múltiplos domínios da atenção, memória, linguagem, fluência e funções visoespaciais. O escore total máximo é 100, com subescores para vários domínios também sendo calculados. Ele foi validado como uma ferramenta de rastreamento para deficits cognitivos na DFT e na doença de Alzheimer.[86]
A Bateria de Avaliação Frontal (FAB) é um exame realizado à beira do leito que pode ser administrado em 10 minutos e é útil para rastrear e identificar disfunções do lobo frontal.[87]
A Entrevista Executiva (EXIT) é uma ferramenta útil de rastreamento à beira do leito para detectar possíveis disfunções do lobo frontal. Ela é composta por um perfil curto de 25 itens e leva aproximadamente 15 minutos.[88] A Quick EXIT é uma versão abreviada de 14 itens da EXIT original que foi desenvolvida omitindo 11 itens que foram avaliados como se encaixando menos bem na escala.[89]
O Inventário Comportamental Frontal (Frontal Behavioural Inventory; FBI) é um questionário quantificável de 24 itens, respondido por meio de entrevista com um informante.[90] O objetivo é identificar alterações precoces do comportamento e da personalidade na vcDFT.[91]
O Cambridge Behavioural Inventory Revised (CBI-R) é um questionário baseado em informantes usado para avaliar sintomas comportamentais em doenças neurodegenerativas, incluindo a DFT.[92]
A Sydney Language Battery (SYDBAT) é um teste para caracterizar deficits de linguagem em variantes da afasia progressiva primária (APP).[93][94] Quatro subtestes de linguagem (nomeação, compreensão de palavras, repetição e associação semântica) são avaliados. Um fonoaudiólogo pode ser envolvido em uma avaliação abrangente da linguagem e na elaboração de intervenções e estratégias compensatórias nos pacientes com APP.[95]
As escalas neurocomportamentais também podem ser úteis na diferenciação de outras formas de demência.[96]
A evolução da DFT difere bastante da maioria das outras formas de demência porque os problemas de memória não são graves nos estágios iniciais. A maioria das escalas de classificação de demência é enviesada em relação à detecção de agravamento da doença de Alzheimer. A escala de classificação frontotemporal (FRS) foi desenvolvida especificamente para a DFT, e pode detectar a deterioração funcional ao longo de 12 meses.[97] O nível da gravidade da demência é mais precisamente estimado pela FRS que pelas escalas convencionais de classificação de demências.
O teste de 60 faces de Ekman é um teste usado para verificar o reconhecimento de emoções faciais.[98] Um processamento emocional deficiente é detectável nos pacientes com DFT e é uma característica clínica importante na vcDFT e na demência semântica.[99] O reconhecimento de emoções pode estar significativamente prejudicado na vcDFT em comparação à doença de Alzheimer em todas as emoções, exceto a felicidade.[100] Além disso, o reconhecimento da raiva é mais comprometido na DFT do que na doença de Alzheimer, enquanto o deficit no reconhecimento do medo é mais característico da doença de Alzheimer.[101]
Testes neuropsicológicos mais abrangentes de múltiplos domínios são úteis, além dos testes cognitivos iniciais descritos anteriormente nesta seção, particularmente nos estágios iniciais, quando as manifestações da DFT são sutis. Os exemplos de baterias de testes formais que são apropriadas nesse cenário incluem o Sistema de Função Executiva Delis-Kaplan (D-KEFS), a Bateria de Cognição Executiva e Social (ESCB) e itens selecionados da Escala de Inteligência Wechsler para Adultos (WAIS).[102]
Avaliação laboratorial
Testes de rastreamento de rotina que devem ser realizados na apresentação para descartar outras doenças incluem:
Hemograma completo
proteína C-reativa
Hormônio estimulante da tireoide
T4 livre
Perfil metabólico
Testes de função renal
Testes da função hepática
Níveis séricos de vitamina B12
Níveis de folato sérico
Teste sorológico para sífilis
Teste sorológico para doença de Lyme
Teste sorológico para HIV.
Os resultados dos testes hematológicos, sorológicos e bioquímicos são geralmente normais.
Exame imagiológico do cérebro
Os objetivos do exame de imagem nas pessoas com suspeita de DFT são:[103][104]
Avaliar anormalidades cerebrais estruturais potencialmente tratáveis (elas podem mimetizar um quadro clínico de DFT)
Identificar características que corroborem um diagnóstico de DFT
Fornecer informações prognósticas e ajudar a iniciar o tratamento mais precocemente.
A ressonância nuclear magnética (RNM) é a principal modalidade de imagem para o diagnóstico de DFT; a tomografia computadorizada (TC) deve ser solicitada se houver suspeita de diagnóstico de DFT, mas a RNM não estiver disponível ou for contraindicada.
A RNM demonstra os padrões clássicos de atrofia associados à DFT, a qual afeta predominantemente os lobos frontal e temporal.[104]
A TC pode ser usada para descartar anormalidades estruturais, como massas ou hematomas subdurais, as quais podem se apresentar como disfunção do lobo frontal, mas também pode mostrar uma atrofia indicativa de DFT.[104]
A tomografia por emissão de pósitrons (PET) com fluordesoxiglucose (FDG)/CT pode ajudar a diferenciar a DFT da doença de Alzheimer e da demência com corpos de Lewy, mostrando hipometabolismo principalmente nos lobos frontal e temporal, frequentemente com assimetria esquerda-direita.[103][104][105] Ela é mais útil quando combinada com a RNM.[104]
Uma PET-CT para amiloide negativa pode ajudar a descartar a doença de Alzheimer, mas pode ser positiva em uma pequena proporção de pacientes com DFT, possivelmente indicando uma patologia mista.[104] A tomografia computadorizada por emissão de fóton único (SPECT) de perfusão cerebral pode detectar hipoperfusão, mas geralmente é considerada menos útil que a FDG-PET-CT na imaginologia inicial da suspeita de DFT.[104]
Os subtipos de DFT podem ser determinados pela observação de padrões específicos de atrofia e hipometabolismo:[104][106][107][108][109][110][111][112]
A vcDFT está tipicamente associada à atrofia na RNM estrutural e hipometabolismo na FDG-PET no córtex pré-frontal e nos lobos temporais anteriores, com preservação relativa das regiões mais posteriores do cérebro, como o lobo occipital. A interrupção na conectividade estrutural do cérebro, medida com o uso de imagem por tensor de difusão (DTI), também é uma característica.
A demência semântica está associada a padrões característicos de atrofia na RNM estrutural, e o hipometabolismo nos lobos temporais anteriores é evidente na FDG-PET.
A afasia progressiva primária (APP) está associada a padrões relativamente focais de atrofia na RNM e hipometabolismo na FDG-PET no lobo frontal posterior esquerdo.
A variante logopênica da APP mostra atrofia na RNM e hipometabolismo na FDG-PET nos lobos temporoparietal lateral e parietal medial (esquerdo maior que direito), e no lobo frontal esquerdo.
A paralisia supranuclear progressiva está associada a atrofia do mesencéfalo na RNM (que pode se manifestar como sinais do "beija-flor", de "Mickey Mouse" ou de "glória-da-manhã") e ao hipometabolismo do mesencéfalo e do lobo frontal na FDG-PET.
Na degeneração corticobasal, a RNM mostra atrofia cortical assimétrica envolvendo as regiões frontal posterior e parietal, juntamente com dilatação dos ventrículos laterais. A FDG-PET demonstra hipometabolismo nas regiões parietal superior e frontal superior e, menos frequentemente, nos gânglios da base e no tálamo.
Nos pacientes com vcDFT e esclerose lateral amiotrófica, a RNM pode mostrar atrofia nas regiões pré-motoras e giros pré-centrais.
Métodos avançados de RNM (por exemplo, morfometria baseada em vóxeis, RNM funcional em estado de repouso, DTI, arterial spin labelling e índice anteroposterior) podem diferenciar a DFT da doença de Alzheimer, com uma sensibilidade de 60 a 83% e uma especificidade de 63 a 93% relatadas.[103][113]
Estudos da estrutura fina das redes neuronais adultas e "centros" de rede sub-regionais específicos provavelmente oferecem referências normativas no diagnóstico diferencial de demências comuns incluindo demência frontotemporal (DFT).[114] De forma geral, na DFT, ruptura da substância branca é mais grave que dano da substância cinzenta.[115]
[Figure caption and citation for the preceding image starts]: Padrões de neuroimagem associados à variante comportamental da DFT (vcDFT) e à variante não fluente da afasia progressiva primária (vnfAPP). RNM estrutural e FDG-PET demonstrando a variabilidade nos padrões de atrofia e hipometabolismo na DFT. No caso da vcDFT, observa-se atrofia bilateral significativa e hipometabolismo no lobo frontal. No caso da vnfAPP, a atrofia e o hipometabolismo são lateralizados e afetam muito mais o lobo frontal esquerdo do que o direito.Peet BT et al. Neurotherapeutics 2021 Abr; 18 (2): 728-52; usado com permissão [Citation ends].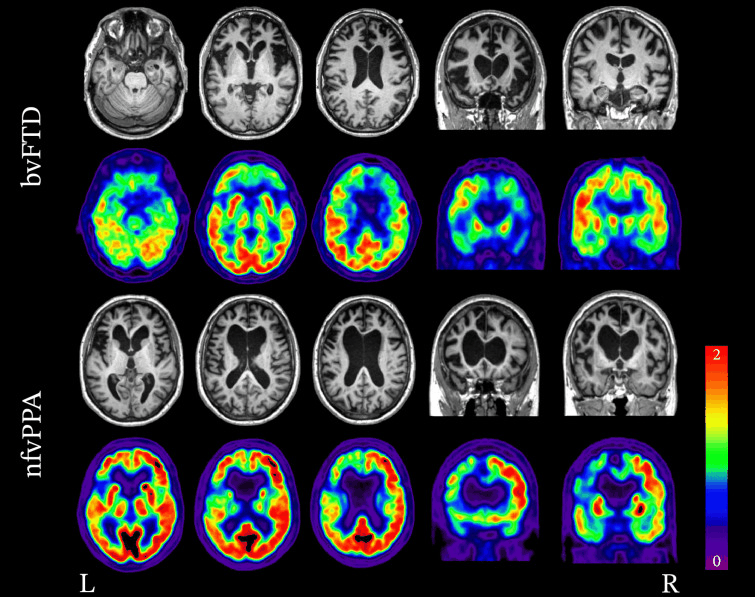
[Figure caption and citation for the preceding image starts]: RNM ponderada em T1 coronal (a, b) e RNM com FDG-PET fundida (c) em um paciente com demência semânticaBhogal P et al. Eur Radiol 23, 3405-17 (2013); usado com permissão [Citation ends].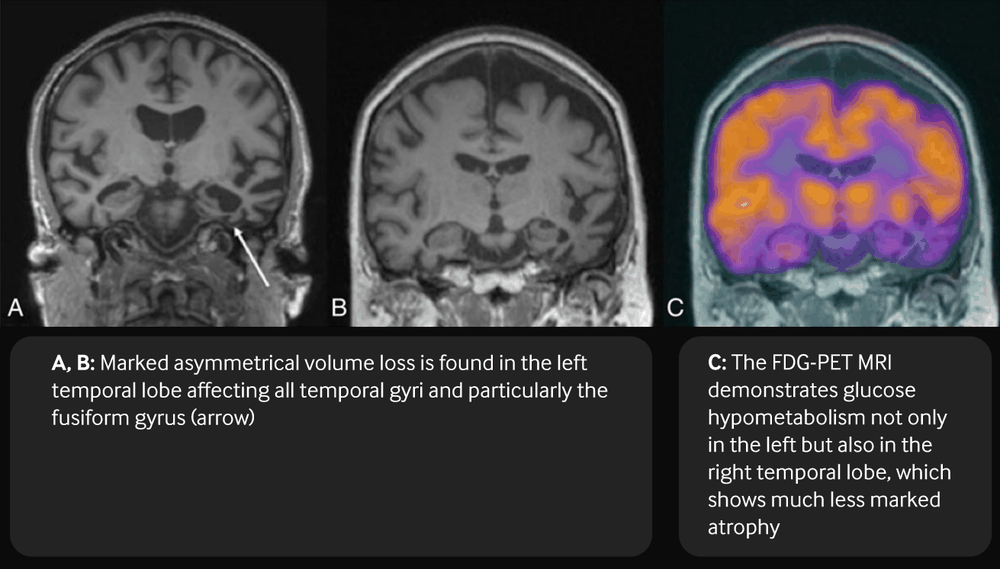
Teste genético
Os testes genéticos para identificar uma mutação relevante conhecida geralmente não estão disponíveis em serviços de genética clínica de rotina. O contexto clínico é raramente esclarecedor; um diagnóstico clínico do subtipo de demência é frequentemente temporário, e não há neuropatologia dos familiares afetados. Se a testagem genética for realizada, a equipe de genética clínica necessita de recursos laboratoriais suficientes para fazer a distinção entre os subtipos de demência.[116]
A história familiar de DFT é um bom indicador da adequação da testagem genética. Mutações nos genes GRN e MAPT estão presentes quase exclusivamente nos pacientes com uma forte história familiar, enquanto a expansão do C9orf72 pode ocorrer na doença aparentemente esporádica.[117] Com base na experiência clínica e nas evidências disponíveis, o teste genético é desejável para todos os pacientes com vcDFT provável ou possível, e nos pacientes com suspeita de vcDFT com características psiquiátricas fortes e pelo menos um membro da família afetado. O rastreamento para mutações em C9orf72 deve ocorrer para todos os pacientes com suspeita de DFT com sintomas psiquiátricos proeminentes ou história familiar de transtorno psiquiátrico primário de início tardio (mesmo se não forem atendidos todos os critérios diagnósticos completos).[28] A testagem genética (para MAPT, GRN e C9orf72) deve ser realizada caso os resultados possam contribuir para decisões relacionadas a gestação.
O teste genético deve ser considerado dentro do contexto de um serviço de genética clínica com a capacidade de oferecer suporte educacional e psicológico para as famílias afetadas. Recomenda-se aconselhamento pré e pós-teste. O aconselhamento genético avalia a história familiar e aconselha sobre os testes genéticos e seu impacto. Ajuda os indivíduos e suas famílias a entender os riscos e implicações potenciais da DFT, especialmente os tipos familiares, e facilita decisões sobre testes genéticos e o manejo da condição. Após os testes, o aconselhamento ajuda na interpretação dos resultados e fornece suporte e informações sobre padrões de herança e riscos potenciais para outros membros da família.[118][119]
Outros testes
Um eletroencefalograma (EEG) ou uma eletromiografia (EMG) podem ser indicados em circunstâncias específicas para se descartarem outros diagnósticos.
eletroencefalograma (EEG)
O uso do EEG na demência é recomendado quando houver uma história de convulsões ou de alteração no nível de consciência, aumentando a possibilidade de epilepsia, encefalopatia ou evolução subaguda atípica.[106][120] Padrões de anormalidades epileptiformes lateralizadas ou bilaterais, ou ondas lentas (às vezes trifásicas e periódicas) apoiam um diagnóstico de epilepsia de início tardio, doença por príon, ou encefalopatias tóxicas, metabólicas, sépticas, autoimunes e anóxicas.[106][121][122][123]
Embora existam poucos dados, as pesquisas até o momento dão suporte a um potencial uso da eletroencefalografia e da magnetoencefalografia na identificação da DFT.[124] Os resultados de um estudo pequeno mostram que a eletroencefalografia integrada ao aprendizado de máquina detecta a DFT com alta acurácia; análises adicionais desse método nesse cenário são necessárias para confirmar a validade.[125]
eletromiografia (EMG)
Uma EMG pode ser indicada se forem observados sintomas e sinais sugestivos de esclerose lateral amiotrófica. Na disfunção do neurônio motor inferior, uma EMG pode mostrar evidências de alteração neurogênica crônica (potenciais das unidades motoras grandes de duração e/ou amplitude aumentadas) e evidências de denervação contínua (potenciais de fibrilação ou ondas agudas positivas, ou potenciais de fasciculação).[126]
Exame do tecido cerebral
O exame neuropatológico é o padrão para o diagnóstico definitivo. Os espécimes podem ser obtidos por biópsia cerebral, mas isso geralmente não é recomendado. Portanto, a confirmação patológica é normalmente obtida no final da vida e é especialmente importante na caracterização da demência familiar.
O diagnóstico neuropatológico baseia-se em critérios formais.[127][128] Ao exame macroscópico, é encontrada atrofia regional afetando predominantemente os lobos frontais e/ou temporais. A neuropatologia molecular permite que a maioria dos casos de DFT seja colocada em um de três subgrupos moleculares: degeneração lobar frontotemporal com tau (30% a 50% dos casos), proteína de ligação ao DNA TAR (TDP-43) ou acúmulo de proteína FET.[53]
Biomarcadores em fluidos
Há um interesse crescente em explorar potenciais biomarcadores em fluidos corporais no líquido cefalorraquidiano (LCR), soro e plasma para fins diagnósticos, prognósticos e de estadiamento.
Não há um único biomarcador em fluido específico que identifique exclusivamente patologias de DFT associadas a casos esporádicos. Vários marcadores foram e continuam sendo estudados. O uso de uma combinação de marcadores potencialmente pode aumentar a acurácia diagnóstica.[129]
Em comparação com a doença de Alzheimer, a DFT é caracterizada por níveis mais elevados de Aß42 no LCR e valores mais baixos de t-tau/Aß42 e p-tau/Aß42. A proporção de p-tau/Aß42 parece ser o biomarcador mais sensível e específico para discriminar a DFT com distúrbio de linguagem primário da doença de Alzheimer.[130] Também se demonstrou que os níveis plasmáticos de p-tau-181 e p-tau-217 estão elevados na doença de Alzheimer, mas não na DFT, exceto para certas mutações em MAPT.[131][132] Nos pacientes com proteinopatia da proteína de ligação ao DNA TAR 43 (TDP-43), há uma redução na proporção de p-tau181 em relação à tau total.[133]
O uso deste conteúdo está sujeito ao nosso aviso legal