El diagnóstico se basa en los síntomas y signos clínicos. No existen pruebas diagnósticas de laboratorio específicas para la enfermedad. En 1974, se reconocieron y se reportaron los principales signos. Posteriormente, la American Heart Association (AHA) actualizó estos criterios, que fueron respaldados por la American Academy of Pediatrics.[1]McCrindle BW, Rowley AH, Newburger JW, et al; American Heart Association. Diagnosis, treatment, and long-term management of Kawasaki disease: a scientific statement for health professionals from the American Heart Association. Circulation. 2017 Apr 25;135(17):e927-99.
https://www.ahajournals.org/doi/full/10.1161/cir.0000000000000484
http://www.ncbi.nlm.nih.gov/pubmed/28356445?tool=bestpractice.com
[28]Jone PN, Tremoulet A, Choueiter N, et al. Update on diagnosis and management of Kawasaki disease: a scientific statement from the American Heart Association. Circulation. 2024 Dec 3;150(23):e481-500.
https://www.ahajournals.org/doi/10.1161/CIR.0000000000001295
http://www.ncbi.nlm.nih.gov/pubmed/39534969?tool=bestpractice.com
[30]Kawasaki T, Kosaki T, Okawa S, et al. A new infantile acute febrile mucocutaneous lymph node syndrome (MLNS) prevailing in Japan. Pediatrics. 1974 Sep;54(3):271-6.
http://www.ncbi.nlm.nih.gov/pubmed/4153258?tool=bestpractice.com
Las guías de práctica clínica del Centro único y punto de acceso para la reumatología pediátrica en Europa (SHARE) recomiendan considerar el diagnóstico de la enfermedad de Kawasaki (EK) en cualquier niño con una enfermedad febril, exantemática, con inflamación sistémica, especialmente si la fiebre persiste durante más de 4 días.[31]Kuemmerle-Deschner JB, Hansmann S, Wulffraat NM, et al. Recommendations for collaborative paediatric research including biobanking in Europe: a Single Hub and Access point for paediatric Rheumatology in Europe (SHARE) initiative. Ann Rheum Dis. 2018 Mar;77(3):319-327.
http://www.ncbi.nlm.nih.gov/pubmed/29021237?tool=bestpractice.com
El diagnóstico rápido es clave, ya que el tratamiento en los 10 días posteriores al inicio de la fiebre reduce significativamente el riesgo de desarrollar dilatación de la arteria coronaria o aneurisma.[28]Jone PN, Tremoulet A, Choueiter N, et al. Update on diagnosis and management of Kawasaki disease: a scientific statement from the American Heart Association. Circulation. 2024 Dec 3;150(23):e481-500.
https://www.ahajournals.org/doi/10.1161/CIR.0000000000001295
http://www.ncbi.nlm.nih.gov/pubmed/39534969?tool=bestpractice.com
[32]Gorelik M, Chung SA, Ardalan K, et al. 2021 American College of Rheumatology/Vasculitis Foundation guideline for the management of Kawasaki disease. Arthritis Care Res (Hoboken). 2022 Apr;74(4):538-48.
http://www.ncbi.nlm.nih.gov/pubmed/35257507?tool=bestpractice.com
La AHA establece que la EK idealmente debe diagnosticarse en los 4-5 días posteriores a la enfermedad para los pacientes con EK completa, y lo antes posible en los 10 días posteriores al inicio de la fiebre para los pacientes con sospecha de EK incompleta.[28]Jone PN, Tremoulet A, Choueiter N, et al. Update on diagnosis and management of Kawasaki disease: a scientific statement from the American Heart Association. Circulation. 2024 Dec 3;150(23):e481-500.
https://www.ahajournals.org/doi/10.1161/CIR.0000000000001295
http://www.ncbi.nlm.nih.gov/pubmed/39534969?tool=bestpractice.com
Fase aguda
La fase aguda se prolonga, normalmente, durante 7 a 11 días.
Además de fiebre, los pacientes deben presentar al menos cuatro más de los cinco signos y síntomas siguientes:
Erupción eritematosa polimorfa.
Inyección conjuntival no purulenta bilateral (tiene lugar en el 90% de los casos).
Cambios orofaríngeos, incluidos hiperemia difusa, lengua de fresa y cambios en los labios (p. ej., hinchazón, agrietamiento, eritema y sangrado).
Cambios en las extremidades periféricas, incluidos eritema, edema, induración y descamación, que pueden causar problemas para caminar.
Linfadenopatía cervical no purulenta. Esto ocurre en el 40% de los casos (aunque otros informes indican que la cifra es de 50% a 75%) y suele ser un solo nodo cervical no supurativo agrandado que mide aproximadamente 1.5 cm o más.
Estos criterios son solo directrices para prevenir diagnósticos equivocados o sobrediagnósticos. Según estas guías de práctica clínica, se puede realizar un diagnóstico en el día 4 de la fiebre si se cumplen los cuatro criterios principales, especialmente cuando hay enrojecimiento e hinchazón de las manos y los pies. Los médicos con experiencia que han tratado a muchos pacientes con EK, pueden establecer el diagnóstico en el día 3 de la fiebre si hay una presentación clínica clásica.[1]McCrindle BW, Rowley AH, Newburger JW, et al; American Heart Association. Diagnosis, treatment, and long-term management of Kawasaki disease: a scientific statement for health professionals from the American Heart Association. Circulation. 2017 Apr 25;135(17):e927-99.
https://www.ahajournals.org/doi/full/10.1161/cir.0000000000000484
http://www.ncbi.nlm.nih.gov/pubmed/28356445?tool=bestpractice.com
[28]Jone PN, Tremoulet A, Choueiter N, et al. Update on diagnosis and management of Kawasaki disease: a scientific statement from the American Heart Association. Circulation. 2024 Dec 3;150(23):e481-500.
https://www.ahajournals.org/doi/10.1161/CIR.0000000000001295
http://www.ncbi.nlm.nih.gov/pubmed/39534969?tool=bestpractice.com
La fiebre debe ser alta, generalmente superior a 39 °C (102 °F), pero a menudo supera los 39.9 °C (104 °F). Los pacientes suelen estar irritables más allá de lo esperado para el grado de fiebre.
El SHARE europeo recomienda que se pueda llegar a un diagnóstico antes de los 5 días de fiebre si se cumplen cuatro criterios principales o si hay evidencias de dilatación de las arterias coronarias (puntuación Z >2 pero <2.5) o aneurisma (puntuación Z ≥2,5) o si existen evidencias de inflamación persistente, sin diagnóstico alternativo, y una sospecha clínica de EK.[13]de Graeff N, Groot N, Ozen S, et al. European consensus-based recommendations for the diagnosis and treatment of Kawasaki disease - the SHARE initiative. Rheumatology (Oxford). 2019 Apr 1;58(4):672-82.
https://academic.oup.com/rheumatology/article/58/4/672/5233868?login=false
http://www.ncbi.nlm.nih.gov/pubmed/30535127?tool=bestpractice.com
El diagnóstico de EK incompleta se puede realizar según las guías de práctica clínica de la AHA en un niño con fiebre prolongada inexplicable y dos o tres criterios clínicos, o en bebés con ≥7 días de fiebre sin diagnóstico alternativo, junto con hallazgos de laboratorio o ecocardiográficos compatibles.[28]Jone PN, Tremoulet A, Choueiter N, et al. Update on diagnosis and management of Kawasaki disease: a scientific statement from the American Heart Association. Circulation. 2024 Dec 3;150(23):e481-500.
https://www.ahajournals.org/doi/10.1161/CIR.0000000000001295
http://www.ncbi.nlm.nih.gov/pubmed/39534969?tool=bestpractice.com
Las guías de práctica clínica SHARE destacan que se trata de un enfoque pragmático de esta situación, pero carece de una base empírica y los estudios que validan los criterios de la enfermedad de Kawasaki incompleta son una importante prioridad de investigación.[13]de Graeff N, Groot N, Ozen S, et al. European consensus-based recommendations for the diagnosis and treatment of Kawasaki disease - the SHARE initiative. Rheumatology (Oxford). 2019 Apr 1;58(4):672-82.
https://academic.oup.com/rheumatology/article/58/4/672/5233868?login=false
http://www.ncbi.nlm.nih.gov/pubmed/30535127?tool=bestpractice.com
La ecocardiografía en este escenario que muestra vasculitis coronaria confirmaría el diagnóstico, pero un ecocardiograma normal no excluye el diagnóstico. Además, la enfermedad de Kawasaki incompleta se presenta con mayor frecuencia en bebés con riesgo de desarrollar anomalías en las arterias coronarias y que pueden presentar fiebre prolongada como único hallazgo clínico. En pacientes con sospecha de EK, la presencia de irritabilidad o eritema y/o induración en el lugar de la vacunación previa con Bacilo Calmette-Guerin (BCG) son signos que aumentan la probabilidad de diagnóstico.[13]de Graeff N, Groot N, Ozen S, et al. European consensus-based recommendations for the diagnosis and treatment of Kawasaki disease - the SHARE initiative. Rheumatology (Oxford). 2019 Apr 1;58(4):672-82.
https://academic.oup.com/rheumatology/article/58/4/672/5233868?login=false
http://www.ncbi.nlm.nih.gov/pubmed/30535127?tool=bestpractice.com
[Figure caption and citation for the preceding image starts]: Recomendaciones de SHARE para el tratamiento de la sospecha de enfermedad de Kawasaki incompletade Graeff N, Groot N, Ozen S, et al. Recomendaciones europeas basadas en el consenso para el diagnóstico y el tratamiento de la enfermedad de Kawasaki: la iniciativa SHARE. Rheumatology (Oxford). 2019;58(4):672-682. [Citation ends].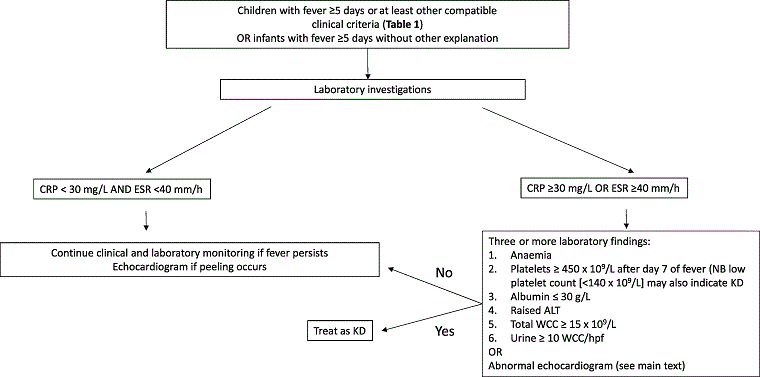
La ecocardiografía se considera positiva para alteraciones coronarias si se cumple cualquiera de las siguientes condiciones:[1]McCrindle BW, Rowley AH, Newburger JW, et al; American Heart Association. Diagnosis, treatment, and long-term management of Kawasaki disease: a scientific statement for health professionals from the American Heart Association. Circulation. 2017 Apr 25;135(17):e927-99.
https://www.ahajournals.org/doi/full/10.1161/cir.0000000000000484
http://www.ncbi.nlm.nih.gov/pubmed/28356445?tool=bestpractice.com
[28]Jone PN, Tremoulet A, Choueiter N, et al. Update on diagnosis and management of Kawasaki disease: a scientific statement from the American Heart Association. Circulation. 2024 Dec 3;150(23):e481-500.
https://www.ahajournals.org/doi/10.1161/CIR.0000000000001295
http://www.ncbi.nlm.nih.gov/pubmed/39534969?tool=bestpractice.com
Arteria coronaria descendente anterior izquierda o arteria coronaria derecha puntuación Z ≥2.5
Se observa aneurisma en la arteria coronaria
Tres o más otras características sugestivas, incluyendo la disminución de la función ventricular izquierda, insuficiencia mitral, derrame pericárdico o puntajes Z en la arteria coronaria descendente anterior izquierda o en la arteria coronaria derecha de 2.0 a 2.5.
Además, la presencia de proteína C reactiva (PCR) ≥3 mg/dL y/o la velocidad de sedimentación globular (VSG) ≥40 mm/hora, más 3 o más de las siguientes características de laboratorio, puede aumentar el índice de sospecha de EK:[28]Jone PN, Tremoulet A, Choueiter N, et al. Update on diagnosis and management of Kawasaki disease: a scientific statement from the American Heart Association. Circulation. 2024 Dec 3;150(23):e481-500.
https://www.ahajournals.org/doi/10.1161/CIR.0000000000001295
http://www.ncbi.nlm.nih.gov/pubmed/39534969?tool=bestpractice.com
anemia
recuento de plaquetas ≥450.000/mm³
albúmina ≤3.0 g/dl
alanina aminotransferasa (ALT) elevada
recuento de leucocitos ≥15.000/mm³
orina con ≥10 leucocitos/campo de gran aumento.
En ausencia de una prueba diagnóstica patognomónica, estos criterios son fundamentales para diagnosticar a un paciente con EK.[28]Jone PN, Tremoulet A, Choueiter N, et al. Update on diagnosis and management of Kawasaki disease: a scientific statement from the American Heart Association. Circulation. 2024 Dec 3;150(23):e481-500.
https://www.ahajournals.org/doi/10.1161/CIR.0000000000001295
http://www.ncbi.nlm.nih.gov/pubmed/39534969?tool=bestpractice.com
Hallazgos infrecuentes en la exploración física en la fase aguda
Los hallazgos menos frecuentes pueden incluir: rigidez en el cuello causada por meningitis aséptica, parálisis facial, uveítis anterior (70%), derrame pleural, infiltrado pulmonar, derrame pericárdico con o sin miocarditis e insuficiencia cardíaca congestiva (ICC).
Otros hallazgos infrecuentes incluyen dolor abdominal, vómitos, pseudoobstrucción, diarrea, hepatitis, ictericia obstructiva, distensión de la vesícula biliar o hidropesía biliar, pancreatitis, afectación de las articulaciones (artralgias o artritis), meatitis, vulvitis, uretritis con piuria estéril, proteinuria, nefritis e insuficiencia renal aguda. Además, se puede encontrar gangrena en las extremidades periféricas, pústulas, lesiones similares a eritemas multiformes, eritema perianal (de 50% a 70%), máculas, pápulas, erupciones similares a las del sarampión y eritema similar al de la escarlatina.
Se puede observar ronquera relacionada con edema y eritema de la laringe. Los datos prospectivos han documentado ronquera en el 11 al 30% de los pacientes con EK; en estos estudios, la ronquera fue más común en niños de <18 meses.[33]Gámez-González LB, Ulloa-Gutierrez R, Murata C, et al. Kawasaki disease presenting with hoarseness: a multinational study of the REKAMLATINA network. Pediatr Int. 2021 Jun;63(6):643-8.
http://www.ncbi.nlm.nih.gov/pubmed/33099854?tool=bestpractice.com
[34]Leuin SC, Shanbhag S, Lago D, et al. Hoarseness as a presenting sign in children with Kawasaki disease. Pediatr Infect Dis J. 2013 Dec;32(12):1392-4.
https://pmc.ncbi.nlm.nih.gov/articles/PMC3887132
http://www.ncbi.nlm.nih.gov/pubmed/23811742?tool=bestpractice.com
En raras ocasiones, los pacientes pueden presentar el síndrome de shock de Kawasaki, una forma grave de EK caracterizada por shock vasodilatador, hipotensión y mala perfusión, con o sin disfunción miocárdica.[28]Jone PN, Tremoulet A, Choueiter N, et al. Update on diagnosis and management of Kawasaki disease: a scientific statement from the American Heart Association. Circulation. 2024 Dec 3;150(23):e481-500.
https://www.ahajournals.org/doi/10.1161/CIR.0000000000001295
http://www.ncbi.nlm.nih.gov/pubmed/39534969?tool=bestpractice.com
[35]Kanegaye JT, Wilder MS, Molkara D, et al. Recognition of a Kawasaki disease shock syndrome. Pediatrics. 2009 May;123(5):e783-9.
https://pmc.ncbi.nlm.nih.gov/articles/PMC2848476
http://www.ncbi.nlm.nih.gov/pubmed/19403470?tool=bestpractice.com
Las ulceraciones orales, la faringitis exudativa, la conjuntivitis exudativa o unilateral y la erupción vesicular no son características de la EK y pueden sugerir un diagnóstico alternativo.[28]Jone PN, Tremoulet A, Choueiter N, et al. Update on diagnosis and management of Kawasaki disease: a scientific statement from the American Heart Association. Circulation. 2024 Dec 3;150(23):e481-500.
https://www.ahajournals.org/doi/10.1161/CIR.0000000000001295
http://www.ncbi.nlm.nih.gov/pubmed/39534969?tool=bestpractice.com
Fase subaguda
Esta etapa dura entre 2 y 3 semanas, durante las cuales los signos y síntomas de presentación están en proceso de resolución, incluyendo entre otros, la irritabilidad persistente y la disminución del apetito. La inyección conjuntival y el agrietamiento de los labios pueden persistir en esta fase.
Las características típicas durante esta fase de la enfermedad incluyen descamación periungueal, mejora de los biomarcadores de fase aguda, desarrollo de trombocitosis, desarrollo de aneurisma en la arteria coronaria y reducción de la temperatura.
Etapa convaleciente/crónica
Esta fase dura entre 4 y 6 semanas; los principales signos y síntomas se han resuelto y los marcadores de inflamación se han normalizado. Sin embargo, en los pacientes que han desarrollado secuelas cardíacas, los aneurismas en las arterias coronarias pueden persistir y empeorar, y pueden desarrollarse complicaciones potencialmente mortales como la trombosis o el infarto de miocardio. El 60% de los aneurismas pequeños se resolverán.
Análisis clínicos iniciales
Las guías de práctica clínica europeas SHARE recomiendan las siguientes pruebas de laboratorio que deben monitorizarse en todos los pacientes: VSG, proteína C-reactiva, hemograma completo, función hepática, albúmina sérica, sodio sérico (para hiponatremia asociada a enfermedad grave), función renal y análisis de orina.[13]de Graeff N, Groot N, Ozen S, et al. European consensus-based recommendations for the diagnosis and treatment of Kawasaki disease - the SHARE initiative. Rheumatology (Oxford). 2019 Apr 1;58(4):672-82.
https://academic.oup.com/rheumatology/article/58/4/672/5233868?login=false
http://www.ncbi.nlm.nih.gov/pubmed/30535127?tool=bestpractice.com
También deben monitorizarse la ferritina y el fibrinógeno si se sospecha un síndrome de activación macrofágica. En particular, la VSG no es una prueba especialmente útil tras el tratamiento con inmunoglobulina intravenosa (IGIV), ya que puede elevarse debido a la unión de la inmunoglobina a los eritrocitos.[1]McCrindle BW, Rowley AH, Newburger JW, et al; American Heart Association. Diagnosis, treatment, and long-term management of Kawasaki disease: a scientific statement for health professionals from the American Heart Association. Circulation. 2017 Apr 25;135(17):e927-99.
https://www.ahajournals.org/doi/full/10.1161/cir.0000000000000484
http://www.ncbi.nlm.nih.gov/pubmed/28356445?tool=bestpractice.com
[13]de Graeff N, Groot N, Ozen S, et al. European consensus-based recommendations for the diagnosis and treatment of Kawasaki disease - the SHARE initiative. Rheumatology (Oxford). 2019 Apr 1;58(4):672-82.
https://academic.oup.com/rheumatology/article/58/4/672/5233868?login=false
http://www.ncbi.nlm.nih.gov/pubmed/30535127?tool=bestpractice.com
[28]Jone PN, Tremoulet A, Choueiter N, et al. Update on diagnosis and management of Kawasaki disease: a scientific statement from the American Heart Association. Circulation. 2024 Dec 3;150(23):e481-500.
https://www.ahajournals.org/doi/10.1161/CIR.0000000000001295
http://www.ncbi.nlm.nih.gov/pubmed/39534969?tool=bestpractice.com
Durante la fase aguda, muchos marcadores de reactantes de fase aguda como la VSG, la PCR y la ferritina se elevan significativamente. Estas pruebas tienden a volver a niveles normales entre el final de la fase subaguda y la etapa convaleciente y la PCR vuelve a los valores normales más rápidamente que la VSG. Si la VSG y la PCR fueran normales o estuvieran muy levemente elevadas (VSG <40 mm/hora y/o PCR <190 nm/L [<20 mg/L o<2 mg/dL]) al inicio de la fase aguda, esto sería atípico de la EK y deberían considerarse diagnósticos alternativos incluyendo infecciones estreptocócicas (especialmente escarlatina), y enfermedades víricas, con consulta de enfermedades infecciosas si fuera necesario. En la fase aguda se observa una anemia normocrómica de leve a moderada, junto con un recuento elevado de leucocitos. Durante la fase subaguda, se produce trombocitosis de forma típica con un recuento de plaquetas que aumenta durante la segunda semana y continúa durante la tercera, normalmente con recuentos de plaquetas de hasta 1000 x 10⁹/L (1 millón/microlitro), pero ocasionalmente se observan recuentos de hasta 2000 x 10⁹/L (2 millones/microlitro).
ECG y ecocardiograma
Las guías de práctica clínica europeas SHARE y la AHA recomiendan que se realice un ECG y un ecocardiograma en el momento del diagnóstico, pero su obtención no debe retrasar el inicio del tratamiento.[1]McCrindle BW, Rowley AH, Newburger JW, et al; American Heart Association. Diagnosis, treatment, and long-term management of Kawasaki disease: a scientific statement for health professionals from the American Heart Association. Circulation. 2017 Apr 25;135(17):e927-99.
https://www.ahajournals.org/doi/full/10.1161/cir.0000000000000484
http://www.ncbi.nlm.nih.gov/pubmed/28356445?tool=bestpractice.com
[13]de Graeff N, Groot N, Ozen S, et al. European consensus-based recommendations for the diagnosis and treatment of Kawasaki disease - the SHARE initiative. Rheumatology (Oxford). 2019 Apr 1;58(4):672-82.
https://academic.oup.com/rheumatology/article/58/4/672/5233868?login=false
http://www.ncbi.nlm.nih.gov/pubmed/30535127?tool=bestpractice.com
[28]Jone PN, Tremoulet A, Choueiter N, et al. Update on diagnosis and management of Kawasaki disease: a scientific statement from the American Heart Association. Circulation. 2024 Dec 3;150(23):e481-500.
https://www.ahajournals.org/doi/10.1161/CIR.0000000000001295
http://www.ncbi.nlm.nih.gov/pubmed/39534969?tool=bestpractice.com
El American College of Rheumatology también recomienda encarecidamente obtener un ecocardiograma con mediciones de la arteria coronaria sin demora para los niños con sospecha de EK incompleta y fiebre.[32]Gorelik M, Chung SA, Ardalan K, et al. 2021 American College of Rheumatology/Vasculitis Foundation guideline for the management of Kawasaki disease. Arthritis Care Res (Hoboken). 2022 Apr;74(4):538-48.
http://www.ncbi.nlm.nih.gov/pubmed/35257507?tool=bestpractice.com
La ecocardiografía es crucial en el tratamiento de la enfermedad de Kawasaki para identificar anomalías de la arteria coronaria. Durante la fase aguda, es importante realizar un ecocardiograma inicial para descartarlos y buscar evidencia de miocarditis, valvulitis o derrame pericárdico. El ECG está indicado para descartar alteraciones en la conducción. Taquicardia, un intervalo PR prolongado, cambios en la onda T y el segmento ST y un voltaje de ondas R disminuido pueden indicar miocarditis. Cambios en la onda T y el segmento ST o en la onda Q pueden indicar un infarto de miocardio. El ECG también puede mostrar ondas T bífidas.[36]Oyamada J, Shimizu C, Kim J, et al. Bifid T waves on the ECG and genetic variation in calcium channel voltage-dependent beta 2 subunit gene (CACNB2) in acute Kawasaki disease. Congenit Heart Dis. 2019 Mar;14(2):213-20.
https://www.techscience.com/chd/v14n2/38763
http://www.ncbi.nlm.nih.gov/pubmed/30395415?tool=bestpractice.com
Tenga en cuenta que en la primera semana de la enfermedad, el ecocardiograma suele ser normal y no descarta el diagnóstico.[1]McCrindle BW, Rowley AH, Newburger JW, et al; American Heart Association. Diagnosis, treatment, and long-term management of Kawasaki disease: a scientific statement for health professionals from the American Heart Association. Circulation. 2017 Apr 25;135(17):e927-99.
https://www.ahajournals.org/doi/full/10.1161/cir.0000000000000484
http://www.ncbi.nlm.nih.gov/pubmed/28356445?tool=bestpractice.com
[28]Jone PN, Tremoulet A, Choueiter N, et al. Update on diagnosis and management of Kawasaki disease: a scientific statement from the American Heart Association. Circulation. 2024 Dec 3;150(23):e481-500.
https://www.ahajournals.org/doi/10.1161/CIR.0000000000001295
http://www.ncbi.nlm.nih.gov/pubmed/39534969?tool=bestpractice.com
Si los hallazgos del ecocardiograma son anormales en alguna de las etapas durante la evolución de la enfermedad, el médico debe derivar el paciente a un cardiólogo pediátrico para que se le realice un análisis diagnóstico cardíaco completo y le sean administrados cuidados de seguimiento.
Las guías de práctica clínica de SHARE y la AHA recomiendan repetir rutinariamente el ECG y el ecocardiograma 1-2 semanas después del tratamiento, o antes para pacientes de alto riesgo.[1]McCrindle BW, Rowley AH, Newburger JW, et al; American Heart Association. Diagnosis, treatment, and long-term management of Kawasaki disease: a scientific statement for health professionals from the American Heart Association. Circulation. 2017 Apr 25;135(17):e927-99.
https://www.ahajournals.org/doi/full/10.1161/cir.0000000000000484
http://www.ncbi.nlm.nih.gov/pubmed/28356445?tool=bestpractice.com
[13]de Graeff N, Groot N, Ozen S, et al. European consensus-based recommendations for the diagnosis and treatment of Kawasaki disease - the SHARE initiative. Rheumatology (Oxford). 2019 Apr 1;58(4):672-82.
https://academic.oup.com/rheumatology/article/58/4/672/5233868?login=false
http://www.ncbi.nlm.nih.gov/pubmed/30535127?tool=bestpractice.com
[28]Jone PN, Tremoulet A, Choueiter N, et al. Update on diagnosis and management of Kawasaki disease: a scientific statement from the American Heart Association. Circulation. 2024 Dec 3;150(23):e481-500.
https://www.ahajournals.org/doi/10.1161/CIR.0000000000001295
http://www.ncbi.nlm.nih.gov/pubmed/39534969?tool=bestpractice.com
Para los pacientes con características de alto riesgo (edad <6 meses, puntuación Z ≥2.5 en el ecocardiograma en el momento del diagnóstico), la AHA recomienda realizar una ecocardiografía al menos cada 2-3 días (o con la frecuencia recomendada por un cardiólogo) para evaluar el empeoramiento de la dilatación, lo que puede provocar una mayor intensificación del tratamiento. Mantener al paciente hospitalizado y continuar repitiendo el ecocardiograma (y valorando el tratamiento) hasta que las dimensiones luminales hayan dejado de avanzar.[28]Jone PN, Tremoulet A, Choueiter N, et al. Update on diagnosis and management of Kawasaki disease: a scientific statement from the American Heart Association. Circulation. 2024 Dec 3;150(23):e481-500.
https://www.ahajournals.org/doi/10.1161/CIR.0000000000001295
http://www.ncbi.nlm.nih.gov/pubmed/39534969?tool=bestpractice.com
Para pacientes con aneurismas grandes o gigantes en expansión, realice una ecocardiografía al menos cada 2-3 días mientras las dimensiones se expanden rápidamente, al menos una vez por semana en los primeros 45 días de la enfermedad (a menos que el tamaño del aneurisma se haya remodelado a un rango moderado o pequeño), y luego mensualmente hasta el tercer mes después del inicio de la enfermedad.[1]McCrindle BW, Rowley AH, Newburger JW, et al; American Heart Association. Diagnosis, treatment, and long-term management of Kawasaki disease: a scientific statement for health professionals from the American Heart Association. Circulation. 2017 Apr 25;135(17):e927-99.
https://www.ahajournals.org/doi/full/10.1161/cir.0000000000000484
http://www.ncbi.nlm.nih.gov/pubmed/28356445?tool=bestpractice.com
[28]Jone PN, Tremoulet A, Choueiter N, et al. Update on diagnosis and management of Kawasaki disease: a scientific statement from the American Heart Association. Circulation. 2024 Dec 3;150(23):e481-500.
https://www.ahajournals.org/doi/10.1161/CIR.0000000000001295
http://www.ncbi.nlm.nih.gov/pubmed/39534969?tool=bestpractice.com
Para los pacientes con un ecocardiograma normal en el momento del diagnóstico, la evidencia sugiere que el riesgo de desarrollar cambios en la arteria coronaria es extremadamente bajo si se trata de pacientes que responden al tratamiento y tienen un ecocardiograma normal 1-2 semanas después del alta.[28]Jone PN, Tremoulet A, Choueiter N, et al. Update on diagnosis and management of Kawasaki disease: a scientific statement from the American Heart Association. Circulation. 2024 Dec 3;150(23):e481-500.
https://www.ahajournals.org/doi/10.1161/CIR.0000000000001295
http://www.ncbi.nlm.nih.gov/pubmed/39534969?tool=bestpractice.com
Sin embargo, si las imágenes de la arteria coronaria no son óptimas o los marcadores de laboratorio de inflamación son anormales en la semana 1-2 de seguimiento, la guía de práctica clínica de la AHA de 2024 recomienda considerar repetir el seguimiento a las 4-6 semanas.[28]Jone PN, Tremoulet A, Choueiter N, et al. Update on diagnosis and management of Kawasaki disease: a scientific statement from the American Heart Association. Circulation. 2024 Dec 3;150(23):e481-500.
https://www.ahajournals.org/doi/10.1161/CIR.0000000000001295
http://www.ncbi.nlm.nih.gov/pubmed/39534969?tool=bestpractice.com
Las guías de práctica clínica europeas SHARE recomiendan un ecocardiograma a las 6-8 semanas después del inicio de la enfermedad para todos los pacientes, y un ECG y un ecocardiograma al menos semanalmente en pacientes con inflamación continua para controlar las secuelas cardíacas.[13]de Graeff N, Groot N, Ozen S, et al. European consensus-based recommendations for the diagnosis and treatment of Kawasaki disease - the SHARE initiative. Rheumatology (Oxford). 2019 Apr 1;58(4):672-82.
https://academic.oup.com/rheumatology/article/58/4/672/5233868?login=false
http://www.ncbi.nlm.nih.gov/pubmed/30535127?tool=bestpractice.com
En aquellos con alteraciones coronarias en el ecocardiograma inicial, SHARE recomienda repetir el ecocardiograma al menos una vez a la semana para garantizar la estabilización.[13]de Graeff N, Groot N, Ozen S, et al. European consensus-based recommendations for the diagnosis and treatment of Kawasaki disease - the SHARE initiative. Rheumatology (Oxford). 2019 Apr 1;58(4):672-82.
https://academic.oup.com/rheumatology/article/58/4/672/5233868?login=false
http://www.ncbi.nlm.nih.gov/pubmed/30535127?tool=bestpractice.com
A más largo plazo, SHARE recomienda repetir el ECG y la ecocardiografía cada 3-6 meses en niños con aneurismas en la arteria coronaria, dependiendo de su gravedad.[13]de Graeff N, Groot N, Ozen S, et al. European consensus-based recommendations for the diagnosis and treatment of Kawasaki disease - the SHARE initiative. Rheumatology (Oxford). 2019 Apr 1;58(4):672-82.
https://academic.oup.com/rheumatology/article/58/4/672/5233868?login=false
http://www.ncbi.nlm.nih.gov/pubmed/30535127?tool=bestpractice.com
Las guías de práctica clínica de la AHA incluyen un sistema de estratificación para el seguimiento y el tratamiento a largo plazo basado principalmente en las dimensiones luminales máximas de las arterias coronarias, normalizadas como puntuaciones Z; tiene en cuenta la afectación coronaria pasada y actual para categorizar a los pacientes según su nivel de riesgo de desarrollar isquemia miocárdica.[1]McCrindle BW, Rowley AH, Newburger JW, et al; American Heart Association. Diagnosis, treatment, and long-term management of Kawasaki disease: a scientific statement for health professionals from the American Heart Association. Circulation. 2017 Apr 25;135(17):e927-99.
https://www.ahajournals.org/doi/full/10.1161/cir.0000000000000484
http://www.ncbi.nlm.nih.gov/pubmed/28356445?tool=bestpractice.com
[28]Jone PN, Tremoulet A, Choueiter N, et al. Update on diagnosis and management of Kawasaki disease: a scientific statement from the American Heart Association. Circulation. 2024 Dec 3;150(23):e481-500.
https://www.ahajournals.org/doi/10.1161/CIR.0000000000001295
http://www.ncbi.nlm.nih.gov/pubmed/39534969?tool=bestpractice.com
Sin afectación: siempre <2
Solo dilatación: 2.0 a <2.5
Aneurisma de pequeño tamaño: ≥2.5 a <5.0
Aneurisma de tamaño medio: ≥5 a <10, y dimensión absoluta <8 mm
Aneurisma grande o gigante: ≥10, o dimensión absoluta ≥8 mm
Las características clínicas adicionales que indican el riesgo de isquemia miocárdica incluyen un mayor número total, longitud, número de ramas y ubicación distal de los aneurismas; anomalías estructurales y funcionales de la pared del vaso; vasos colaterales deficientes; revascularización previa, trombosis de la arteria coronaria o infarto de miocardio; y disfunción ventricular.[1]McCrindle BW, Rowley AH, Newburger JW, et al; American Heart Association. Diagnosis, treatment, and long-term management of Kawasaki disease: a scientific statement for health professionals from the American Heart Association. Circulation. 2017 Apr 25;135(17):e927-99.
https://www.ahajournals.org/doi/full/10.1161/cir.0000000000000484
http://www.ncbi.nlm.nih.gov/pubmed/28356445?tool=bestpractice.com
Otras pruebas diagnósticas
Se realizan pruebas adicionales para excluir o identificar otra afectación del sistema de órganos:
Pruebas de función hepática: se deben realizar con frecuencia en todos los pacientes con sospecha de EK para evaluar la presencia de hepatitis. La transaminitis es un hallazgo común en la EK. El paciente puede presentar dolor abdominal, ictericia y náuseas o vómitos, además de fiebre alta.
Análisis de orina: se debe realizar con frecuencia en todos los pacientes con sospecha de EK; en el 50% de los pacientes, mostrará piuria estéril moderada a leve de origen uretral. Si el análisis de orina es anormal, se debe realizar un cultivo para descartar una infección urinaria.
Radiografía de tórax: se realiza si se sospecha de la presencia de pericarditis o neumonitis.
Ultrasonografía de la vesícula biliar: para excluir hidropesía de la vesícula biliar (si se sospecha).
Ultrasonografía de testicular: para excluir epididimitis (si se sospecha).
Punción lumbar: se realiza si el paciente presenta rigidez de nuca y fiebre alta. Esta prueba es necesaria para excluir la presencia de meningitis.
Estudios por imágenes cardíacas avanzadas
La angiografía por tomografía computarizada (ATC), la angiografía por resonancia magnética (ARM) y el cateterismo cardíaco con angiografía pueden ser recomendadas por cardiología para evaluar más a fondo los aneurismas coronarios, especialmente en el contexto de hallazgos poco claros en la ecocardiografía o en presencia de aneurismas gigantes.[28]Jone PN, Tremoulet A, Choueiter N, et al. Update on diagnosis and management of Kawasaki disease: a scientific statement from the American Heart Association. Circulation. 2024 Dec 3;150(23):e481-500.
https://www.ahajournals.org/doi/10.1161/CIR.0000000000001295
http://www.ncbi.nlm.nih.gov/pubmed/39534969?tool=bestpractice.com
Estas pruebas son responsabilidad del cardiólogo y se solicitarían cuando los hallazgos del ecocardiograma no sean claros o cuando el ecocardiograma muestre aneurismas gigantes y sea necesaria una delimitación anatómica más detallada.
La ATC suele ser la modalidad preferida para la detección y el seguimiento a largo plazo de los aneurismas en la arteria coronaria, pero la elección de la modalidad de estudios por imágenes depende del contexto clínico y la disponibilidad local.[28]Jone PN, Tremoulet A, Choueiter N, et al. Update on diagnosis and management of Kawasaki disease: a scientific statement from the American Heart Association. Circulation. 2024 Dec 3;150(23):e481-500.
https://www.ahajournals.org/doi/10.1161/CIR.0000000000001295
http://www.ncbi.nlm.nih.gov/pubmed/39534969?tool=bestpractice.com
[37]Pilania RK, Basu S, Singh S, et al. Computed tomography coronary angiography for imaging in children with Kawasaki disease: an update. Int J Rheum Dis. 2024 Sep;27(9):e15331.
https://onlinelibrary.wiley.com/doi/10.1111/1756-185X.15331
http://www.ncbi.nlm.nih.gov/pubmed/39285558?tool=bestpractice.com
Para los pacientes con aneurismas en la arteria coronaria gigantes en rápida expansión durante la hospitalización, realizar una ATC inmediatamente antes del alta puede ayudar a mapear la extensión de los aneurismas a corto plazo.[28]Jone PN, Tremoulet A, Choueiter N, et al. Update on diagnosis and management of Kawasaki disease: a scientific statement from the American Heart Association. Circulation. 2024 Dec 3;150(23):e481-500.
https://www.ahajournals.org/doi/10.1161/CIR.0000000000001295
http://www.ncbi.nlm.nih.gov/pubmed/39534969?tool=bestpractice.com
La ATC se puede realizar en niños con una exposición relativamente baja a la radiación si se obtiene en una institución con la experiencia adecuada. La ARM es una modalidad alternativa para la evaluación de las arterias coronarias. La ARM no implica exposición a la radiación, pero los tiempos de exploración suelen ser más largos y menos sensible que la ATC para la identificación de estenosis, calcificaciones, ectasia y arteriopatía coronaria distal.[28]Jone PN, Tremoulet A, Choueiter N, et al. Update on diagnosis and management of Kawasaki disease: a scientific statement from the American Heart Association. Circulation. 2024 Dec 3;150(23):e481-500.
https://www.ahajournals.org/doi/10.1161/CIR.0000000000001295
http://www.ncbi.nlm.nih.gov/pubmed/39534969?tool=bestpractice.com
[37]Pilania RK, Basu S, Singh S, et al. Computed tomography coronary angiography for imaging in children with Kawasaki disease: an update. Int J Rheum Dis. 2024 Sep;27(9):e15331.
https://onlinelibrary.wiley.com/doi/10.1111/1756-185X.15331
http://www.ncbi.nlm.nih.gov/pubmed/39285558?tool=bestpractice.com
[38]Han BK, Rigsby CK, Hlavacek A, et al. Computed tomography imaging in patients with congenital heart disease part I: rationale and utility. An expert consensus document of the Society of Cardiovascular Computed Tomography (SCCT): endorsed by the Society of Pediatric Radiology (SPR) and the North American Society of Cardiac Imaging (NASCI). J Cardiovasc Comput Tomogr. 2015 Nov-Dec;9(6):475-92.
https://www.journalofcardiovascularct.com/article/S1934-5925(15)00224-5/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/26272851?tool=bestpractice.com
La angiografía invasiva rara vez se requiere dada la disponibilidad generalizada de ATC, pero puede usarse en determinados escenarios (p. ej., cuando los resultados de los estudios por imágenes no invasivos son equívocos o cuando se está considerando la revascularización percutánea en el contexto de un infarto agudo de miocardio, angina o prueba de esfuerzo por isquemia inducible).[28]Jone PN, Tremoulet A, Choueiter N, et al. Update on diagnosis and management of Kawasaki disease: a scientific statement from the American Heart Association. Circulation. 2024 Dec 3;150(23):e481-500.
https://www.ahajournals.org/doi/10.1161/CIR.0000000000001295
http://www.ncbi.nlm.nih.gov/pubmed/39534969?tool=bestpractice.com
[39]Crean A, Benson L, Shah A, et al. Imaging the delayed complications of childhood Kawasaki disease. F1000Res. 2022;11:147.
https://pmc.ncbi.nlm.nih.gov/articles/PMC10036956
http://www.ncbi.nlm.nih.gov/pubmed/36970577?tool=bestpractice.com
Se debe tener cuidado al considerar la angiografía invasiva en presencia de inflamación sistémica en curso, ya que las tasas de complicaciones (como el infarto de miocardio relacionado con el catéter) pueden ser más altas. La ARM y el cateterismo cardíaco con angiografía pueden ser difíciles de realizar en niños pequeños <15 kg de peso.
Pruebas emergentes
La prohormona N-terminal del péptido natriurético cerebral (NT-proBNP) se ha propuesto como un biomarcador diagnóstico potencial de la enfermedad de Kawasaki. Un metanálisis que revisó la utilidad diagnóstica del NT-proBNP demostró que, aunque tiene una eficacia moderada para diagnosticar la EK, de forma aislada no resultaba útil para confirmar o refutar el diagnóstico.[40]Wen JX, Bai X, Niu Y, et al. Diagnostic accuracy of N-terminal pro-brain natriuretic peptide for Kawasaki disease: An updated systematic review and meta-analysis. Int J Clin Pract. 2021 Nov;75(11):e14538.
http://www.ncbi.nlm.nih.gov/pubmed/34133819?tool=bestpractice.com
