En los pacientes en que se sospecha de un síndrome coronario agudo (SCA) se requiere una evaluación urgente. Es fundamental establecer si los síntomas son una manifestación de un SCA y, si es así, qué probabilidad hay de que ocurra un evento clínico adverso.[2]Rao SV, O'Donoghue ML, Ruel M, et al. 2025 ACC/AHA/ACEP/NAEMSP/SCAI guideline for the management of patients with acute coronary syndromes: a report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation. 2025 Apr;151(13):e771-862.
https://www.ahajournals.org/doi/full/10.1161/CIR.0000000000001309?rfr_dat=cr_pub++0pubmed&url_ver=Z39.88-2003&rfr_id=ori%3Arid%3Acrossref.org
http://www.ncbi.nlm.nih.gov/pubmed/40014670?tool=bestpractice.com
Primero, los médicos necesitan establecer el riesgo del paciente y seguir las directrices actuales según la evaluación inicial de riesgos para seleccionar una estrategia de manejo adecuada. La evaluación inicial de riesgos incluye los antecedentes, el examen físico, el ECG y los biomarcadores cardíacos.[2]Rao SV, O'Donoghue ML, Ruel M, et al. 2025 ACC/AHA/ACEP/NAEMSP/SCAI guideline for the management of patients with acute coronary syndromes: a report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation. 2025 Apr;151(13):e771-862.
https://www.ahajournals.org/doi/full/10.1161/CIR.0000000000001309?rfr_dat=cr_pub++0pubmed&url_ver=Z39.88-2003&rfr_id=ori%3Arid%3Acrossref.org
http://www.ncbi.nlm.nih.gov/pubmed/40014670?tool=bestpractice.com
[5]Byrne RA, Rossello X, Coughlan JJ, et al. 2023 ESC guidelines for the management of acute coronary syndromes. Eur Heart J. 2023 Oct 12;44(38):3720-826.
https://academic.oup.com/eurheartj/article/44/38/3720/7243210
[86]National Institute for Health and Care Excellence. Recent-onset chest pain of suspected cardiac origin: assessment and diagnosis. November 2016 [internet publication].
https://www.nice.org.uk/guidance/CG95
electrocardiograma (ECG)
El ECG está indicado como primera prueba diagnóstica en todos los pacientes. Se debe realizar e interpretar un ECG de 12 derivaciones en los 10 minutos posteriores al primer contacto médico en cualquier paciente con sospecha de infarto de miocardio sin elevación del segmento ST (IMSEST).[5]Byrne RA, Rossello X, Coughlan JJ, et al. 2023 ESC guidelines for the management of acute coronary syndromes. Eur Heart J. 2023 Oct 12;44(38):3720-826.
https://academic.oup.com/eurheartj/article/44/38/3720/7243210
[87]Writing Committee, Kontos MC, de Lemos JA, et al. 2022 ACC Expert Consensus Decision Pathway on the evaluation and disposition of acute chest pain in the emergency department: A report of the American College of Cardiology Solution Set Oversight Committee. J Am Coll Cardiol. 2022 Nov 15;80(20):1925-60.
https://www.sciencedirect.com/science/article/pii/S0735109722066189?via%3Dihub
http://www.ncbi.nlm.nih.gov/pubmed/36241466?tool=bestpractice.com
Para el manejo inmediato es crítico descartar un infarto de miocardio con elevación del segmento ST (IMCEST). Un infarto de miocardio sin elevación del segmento ST (IMSEST) es indistinguible de otro tipo de síndrome coronario agudo (SCA) (IMCEST o una angina inestable) hasta que están disponibles el ECG y los biomarcadores, debido a que su fisiopatología y presentación son similares.[2]Rao SV, O'Donoghue ML, Ruel M, et al. 2025 ACC/AHA/ACEP/NAEMSP/SCAI guideline for the management of patients with acute coronary syndromes: a report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation. 2025 Apr;151(13):e771-862.
https://www.ahajournals.org/doi/full/10.1161/CIR.0000000000001309?rfr_dat=cr_pub++0pubmed&url_ver=Z39.88-2003&rfr_id=ori%3Arid%3Acrossref.org
http://www.ncbi.nlm.nih.gov/pubmed/40014670?tool=bestpractice.com
Los hallazgos habituales del ECG pueden estar presentes, pero muchos pacientes presentan un ECG normal al inicio y, por lo tanto, se deben realizar ECG en serie, inicialmente en intervalos de 15 a 30 minutos, para detectar la posibilidad de desarrollo de elevación o depresión del segmento ST.[5]Byrne RA, Rossello X, Coughlan JJ, et al. 2023 ESC guidelines for the management of acute coronary syndromes. Eur Heart J. 2023 Oct 12;44(38):3720-826.
https://academic.oup.com/eurheartj/article/44/38/3720/7243210
Cuando están presentes, los hallazgos del ECG en el IMSEST pueden ser muy variables. Por lo general, se observa una depresión del segmento ST >1 mm en 2 o más derivaciones contiguas. Otros posibles hallazgos son las nuevas y dramáticas inversiones de la onda T (ondas de Wellens) o la elevación transitoria del ST. Los cambios en el ECG que muestran elevación del segmento ST o un nuevo bloqueo de la rama izquierda del haz de His deben evaluarse como IMSEST.[Figure caption and citation for the preceding image starts]: ECG que muestra depresión del segmento STDe la colección personal del Dr. Syed W. Yusuf y del Dr. Iyad N. Daher, Departamento de Cardiología, University of Texas, Houston; usado con autorización [Citation ends]. [Figure caption and citation for the preceding image starts]: ECG que muestra depresión del segmento STDe la colección personal del Dr. Syed W. Yusuf y del Dr. Iyad N. Daher, Departamento de Cardiología, University of Texas, Houston; usado con autorización [Citation ends].
[Figure caption and citation for the preceding image starts]: ECG que muestra depresión del segmento STDe la colección personal del Dr. Syed W. Yusuf y del Dr. Iyad N. Daher, Departamento de Cardiología, University of Texas, Houston; usado con autorización [Citation ends].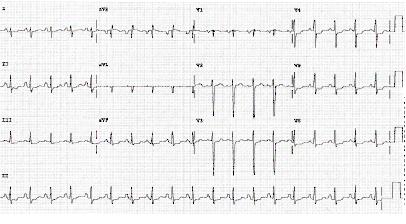
Una monitorización continua del ECG de 12 derivaciones es una alternativa razonable a registros de 12 derivaciones en serie en pacientes cuyo ECG inicial no es diagnóstico.[2]Rao SV, O'Donoghue ML, Ruel M, et al. 2025 ACC/AHA/ACEP/NAEMSP/SCAI guideline for the management of patients with acute coronary syndromes: a report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation. 2025 Apr;151(13):e771-862.
https://www.ahajournals.org/doi/full/10.1161/CIR.0000000000001309?rfr_dat=cr_pub++0pubmed&url_ver=Z39.88-2003&rfr_id=ori%3Arid%3Acrossref.org
http://www.ncbi.nlm.nih.gov/pubmed/40014670?tool=bestpractice.com
Las derivaciones V7 a V9 del ECG suplementario pueden ser útiles en pacientes con ECG iniciales no diagnósticos para descartar un infarto de miocardio (IM) debido a una oclusión de la circunfleja izquierda, y V3R y V4R pueden ser útiles para detectar un IM del ventrículo derecho.[5]Byrne RA, Rossello X, Coughlan JJ, et al. 2023 ESC guidelines for the management of acute coronary syndromes. Eur Heart J. 2023 Oct 12;44(38):3720-826.
https://academic.oup.com/eurheartj/article/44/38/3720/7243210
Con menos frecuencia, el ECG puede revelar una taquiarritmia o una bradiarritmia precipitada por el IM.
Anamnesis y exploración física
Los pacientes que presentan molestias o dolor torácico necesitan una evaluación inmediata de sus antecedentes o historia actual de arteriopatía coronaria (AC) y factores de riesgo tradicionales (p. ej., edad, sexo, diabetes, hipertensión, consumo de cocaína) para clasificarlos como de alta prioridad.[7]Writing Committee Members; Gulati M, Levy PD, Mukherjee D, et al. 2021 AHA/ACC/ASE/CHEST/SAEM/SCCT/SCMR guideline for the evaluation and diagnosis of chest pain: a report of the American College of Cardiology/American Heart Association Joint Committee On Clinical Practice Guidelines. J Am Coll Cardiol. 2021 Nov 30;78(22):e187-285.
https://www.sciencedirect.com/science/article/pii/S0735109721057958
http://www.ncbi.nlm.nih.gov/pubmed/34756653?tool=bestpractice.com
El síndrome coronario agudo (SCA) es altamente probable si existen antecedentes de dolor torácico o dolor en el brazo izquierdo similar al dolor anginoso documentado anteriormente, y antecedentes de AC (incluido IM). Por lo general, el dolor anginoso es un dolor en el pecho o brazo, profundo, que no puede localizarse claramente descrito como una sensación de opresión, pesadez, dolor intenso, ardor, presión o estrujamiento. El dolor con mayor frecuencia es retroesternal y a menudo se puede irradiar al brazo izquierdo a la parte inferior de la mandíbula, al cuello, a ambos brazos, a la espalda y al epigastrio, donde se puede asemejar a la acidez. El dolor anginoso se asocia con el esfuerzo o el estrés emocional (o menos frecuentemente con la exposición al frío) y se alivia con el descanso.[7]Writing Committee Members; Gulati M, Levy PD, Mukherjee D, et al. 2021 AHA/ACC/ASE/CHEST/SAEM/SCCT/SCMR guideline for the evaluation and diagnosis of chest pain: a report of the American College of Cardiology/American Heart Association Joint Committee On Clinical Practice Guidelines. J Am Coll Cardiol. 2021 Nov 30;78(22):e187-285.
https://www.sciencedirect.com/science/article/pii/S0735109721057958
http://www.ncbi.nlm.nih.gov/pubmed/34756653?tool=bestpractice.com
La diaforesis es un síntoma asociado frecuente.[2]Rao SV, O'Donoghue ML, Ruel M, et al. 2025 ACC/AHA/ACEP/NAEMSP/SCAI guideline for the management of patients with acute coronary syndromes: a report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation. 2025 Apr;151(13):e771-862.
https://www.ahajournals.org/doi/full/10.1161/CIR.0000000000001309?rfr_dat=cr_pub++0pubmed&url_ver=Z39.88-2003&rfr_id=ori%3Arid%3Acrossref.org
http://www.ncbi.nlm.nih.gov/pubmed/40014670?tool=bestpractice.com
La disnea también es frecuente y probablemente sea secundaria a la disminución del gasto cardíaco, pero también puede deberse a una congestión pulmonar subyacente. Los pacientes pueden expresar ansiedad o parecer ansiosos. También pueden presentar una sensación de muerte inminente. Habitualmente, los eventos alcanzan su punto máximo en las primeras horas de la mañana, presumiblemente debido al estrés hemodinámico causado por el aumento del cortisol sérico, las hormonas adrenérgicas y la agregación plaquetaria.[88]Manfredini R, Boari B, Salmi R, et al. Twenty-four-hour patterns in occurrence and pathophysiology of acute cardiovascular events and ischemic heart disease. Chronobiol Int. 2013 Mar;30(1-2):6-16.
https://www.tandfonline.com/doi/10.3109/07420528.2012.715843
http://www.ncbi.nlm.nih.gov/pubmed/23002808?tool=bestpractice.com
Los pacientes pueden presentar una serie de síntomas no característicos, cualquiera de los cuales puede ser el único síntoma de presentación. Estos incluyen debilidad, náuseas, vómitos, dolor abdominal y síncope. Son más frecuentes en mujeres, personas de edad avanzada y diabéticos.[5]Byrne RA, Rossello X, Coughlan JJ, et al. 2023 ESC guidelines for the management of acute coronary syndromes. Eur Heart J. 2023 Oct 12;44(38):3720-826.
https://academic.oup.com/eurheartj/article/44/38/3720/7243210
Los hallazgos de la exploración generalmente son inespecíficos, pero pueden revelar hipertensión o hipotensión, la presencia de un tercer y cuarto ruido cardíaco, y el desdoblamiento paradójico del segundo ruido cardíaco. Las señales de insuficiencia cardíaca (aumento de la presión venosa yugular, crepitaciones bilaterales al auscultar los pulmones) o shock cardiógeno también pueden estar presentes, lo que significa un peor pronóstico.
El alivio del dolor torácico con trinitrato de glicerilo sublingual no indica necesariamente el diagnóstico de una isquemia miocárdica y no debe utilizarse como criterio diagnóstico; otras presentaciones (p. ej., el espasmo esofágico) pueden mostrar una respuesta comparable.[7]Writing Committee Members; Gulati M, Levy PD, Mukherjee D, et al. 2021 AHA/ACC/ASE/CHEST/SAEM/SCCT/SCMR guideline for the evaluation and diagnosis of chest pain: a report of the American College of Cardiology/American Heart Association Joint Committee On Clinical Practice Guidelines. J Am Coll Cardiol. 2021 Nov 30;78(22):e187-285.
https://www.sciencedirect.com/science/article/pii/S0735109721057958
http://www.ncbi.nlm.nih.gov/pubmed/34756653?tool=bestpractice.com
El dolor descrito como agudo, fugaz (escasos segundos de duración), o relacionado con la inspiración (pleurítico) o la posición, o que es cambiante en su localización, sugiere una menor probabilidad de isquemia.[7]Writing Committee Members; Gulati M, Levy PD, Mukherjee D, et al. 2021 AHA/ACC/ASE/CHEST/SAEM/SCCT/SCMR guideline for the evaluation and diagnosis of chest pain: a report of the American College of Cardiology/American Heart Association Joint Committee On Clinical Practice Guidelines. J Am Coll Cardiol. 2021 Nov 30;78(22):e187-285.
https://www.sciencedirect.com/science/article/pii/S0735109721057958
http://www.ncbi.nlm.nih.gov/pubmed/34756653?tool=bestpractice.com
Pruebas iniciales (distintas a ECG)
Además del ECG, se deben realizar también las siguientes pruebas en todos los pacientes.
Troponinas cardíacas: un aumento de los niveles de troponinas cardíacas (>99º percentil de la normalidad) es diagnóstico de la enfermedad y el uso de ensayos de troponinas cardíacas de alta sensibilidad ha reducido el intervalo de evaluación.[87]Writing Committee, Kontos MC, de Lemos JA, et al. 2022 ACC Expert Consensus Decision Pathway on the evaluation and disposition of acute chest pain in the emergency department: A report of the American College of Cardiology Solution Set Oversight Committee. J Am Coll Cardiol. 2022 Nov 15;80(20):1925-60.
https://www.sciencedirect.com/science/article/pii/S0735109722066189?via%3Dihub
http://www.ncbi.nlm.nih.gov/pubmed/36241466?tool=bestpractice.com
Esta prueba está fácilmente disponible en la mayoría de los centros médicos. Las troponinas cardíacas son marcadores más sensibles y específicos del daño cardiomiocítico que la creatina-cinasa (CC), su isoenzima de banda miocárdica (CC-MB) y la mioglobina. En los pacientes con IM, los niveles de troponina aumentan rápidamente (por lo general, en la primera hora desde el inicio de los síntomas si se utilizan ensayos de alta sensibilidad) y permanecen elevados durante varios días. Por lo tanto, con la llegada de los ensayos de troponina de alta sensibilidad (hs-cTn), otros biomarcadores (p. ej., CC, CC-MB y mioglobina) ya no son necesarios para el diagnóstico.[4]Thygesen K, Alpert JS, Jaffe AS, et al; Executive Group on behalf of the Joint European Society of Cardiology (ESC)/American College of Cardiology (ACC)/American Heart Association (AHA)/World Heart Federation (WHF) Task Force for the Universal Definition of Myocardial Infarction. Fourth universal definition of myocardial infarction (2018). J Am Coll Cardiol. 2018 Oct 30;72(18):2231-64.
http://www.onlinejacc.org/content/early/2018/08/27/j.jacc.2018.08.1038
http://www.ncbi.nlm.nih.gov/pubmed/30153967?tool=bestpractice.com
[5]Byrne RA, Rossello X, Coughlan JJ, et al. 2023 ESC guidelines for the management of acute coronary syndromes. Eur Heart J. 2023 Oct 12;44(38):3720-826.
https://academic.oup.com/eurheartj/article/44/38/3720/7243210
[7]Writing Committee Members; Gulati M, Levy PD, Mukherjee D, et al. 2021 AHA/ACC/ASE/CHEST/SAEM/SCCT/SCMR guideline for the evaluation and diagnosis of chest pain: a report of the American College of Cardiology/American Heart Association Joint Committee On Clinical Practice Guidelines. J Am Coll Cardiol. 2021 Nov 30;78(22):e187-285.
https://www.sciencedirect.com/science/article/pii/S0735109721057958
http://www.ncbi.nlm.nih.gov/pubmed/34756653?tool=bestpractice.com
Del mismo modo, para fines de diagnóstico inicial, no se recomienda la medición rutinaria de biomarcadores adicionales (p. ej., la proteína de unión a ácidos grasos de tipo cardíaco [h-FABP] o la copeptina) además de la hs-cTn.[5]Byrne RA, Rossello X, Coughlan JJ, et al. 2023 ESC guidelines for the management of acute coronary syndromes. Eur Heart J. 2023 Oct 12;44(38):3720-826.
https://academic.oup.com/eurheartj/article/44/38/3720/7243210
Para la interpretación de la hs-cTn, la Sociedad Europea de Cardiología recomienda utilizar los algoritmos de “confirmación” y “descarte” de 0/1 hora o 0/2 horas, los cuales clasifican a los pacientes en una de tres vías según los resultados de sus valores de hs-cTn a las 0 horas (momento del análisis de sangre inicial) y 1 hora o 2 horas después.[5]Byrne RA, Rossello X, Coughlan JJ, et al. 2023 ESC guidelines for the management of acute coronary syndromes. Eur Heart J. 2023 Oct 12;44(38):3720-826.
https://academic.oup.com/eurheartj/article/44/38/3720/7243210
Vía de descarte: para una hs-cTn inicial muy baja o ningún aumento después de 1/2 hora: estos pacientes pueden ser aptos para el alta temprana y el tratamiento ambulatorio.
Vía de confirmación (“rule-in”): para valores iniciales altos de hs-cTn o un incremento después de 1-2 horas; la mayoría de estos pacientes requerirá ingreso hospitalario y una evaluación adicional.
Vía de observación: si no se cumple ninguno de los criterios anteriores, verificar la hs-cTn a las 3 horas y considerar la realización de una ecocardiografía.
Ecocardiografía: la ecografía cardíaca puede ser útil para el triaje temprano de los pacientes con sospecha de IM.[4]Thygesen K, Alpert JS, Jaffe AS, et al; Executive Group on behalf of the Joint European Society of Cardiology (ESC)/American College of Cardiology (ACC)/American Heart Association (AHA)/World Heart Federation (WHF) Task Force for the Universal Definition of Myocardial Infarction. Fourth universal definition of myocardial infarction (2018). J Am Coll Cardiol. 2018 Oct 30;72(18):2231-64.
http://www.onlinejacc.org/content/early/2018/08/27/j.jacc.2018.08.1038
http://www.ncbi.nlm.nih.gov/pubmed/30153967?tool=bestpractice.com
Siempre se debe realizar un ecocardiograma urgente en pacientes con shock cardiógeno o inestabilidad hemodinámica.[5]Byrne RA, Rossello X, Coughlan JJ, et al. 2023 ESC guidelines for the management of acute coronary syndromes. Eur Heart J. 2023 Oct 12;44(38):3720-826.
https://academic.oup.com/eurheartj/article/44/38/3720/7243210
[89]Edvardsen T, Asch FM, Davidson B, et al. Non-invasive imaging in coronary syndromes: recommendations of the European Association of Cardiovascular Imaging and the American Society of Echocardiography, in collaboration with the American Society of Nuclear Cardiology, Society of Cardiovascular Computed Tomography, and Society for Cardiovascular Magnetic Resonance. Eur Heart J Cardiovasc Imaging. 2022 Jan 24;23(2):e6-33.
https://academic.oup.com/ehjcimaging/article/23/2/e6/6423983
http://www.ncbi.nlm.nih.gov/pubmed/34751391?tool=bestpractice.com
El ecocardiograma transtorácico en el punto de atención también se puede utilizar para buscar alteraciones en la contractilidad regional del ventrículo izquierdo en pacientes con una presentación atípica o un ECG equívoco, buscar complicaciones mecánicas de infarto agudo de miocardio (como función ventricular izquierda, función ventricular derecha, ruptura del tabique ventricular, ruptura de la pared libre del ventrículo izquierdo, insuficiencia mitral aguda, derrame pericárdico, taponamiento cardíaco) y para obtener evidencia que sugiera etiologías alternativas asociadas con dolor torácico (p. ej., enfermedad aórtica aguda, embolia pulmonar).[2]Rao SV, O'Donoghue ML, Ruel M, et al. 2025 ACC/AHA/ACEP/NAEMSP/SCAI guideline for the management of patients with acute coronary syndromes: a report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation. 2025 Apr;151(13):e771-862.
https://www.ahajournals.org/doi/full/10.1161/CIR.0000000000001309?rfr_dat=cr_pub++0pubmed&url_ver=Z39.88-2003&rfr_id=ori%3Arid%3Acrossref.org
http://www.ncbi.nlm.nih.gov/pubmed/40014670?tool=bestpractice.com
[4]Thygesen K, Alpert JS, Jaffe AS, et al; Executive Group on behalf of the Joint European Society of Cardiology (ESC)/American College of Cardiology (ACC)/American Heart Association (AHA)/World Heart Federation (WHF) Task Force for the Universal Definition of Myocardial Infarction. Fourth universal definition of myocardial infarction (2018). J Am Coll Cardiol. 2018 Oct 30;72(18):2231-64.
http://www.onlinejacc.org/content/early/2018/08/27/j.jacc.2018.08.1038
http://www.ncbi.nlm.nih.gov/pubmed/30153967?tool=bestpractice.com
[5]Byrne RA, Rossello X, Coughlan JJ, et al. 2023 ESC guidelines for the management of acute coronary syndromes. Eur Heart J. 2023 Oct 12;44(38):3720-826.
https://academic.oup.com/eurheartj/article/44/38/3720/7243210
[89]Edvardsen T, Asch FM, Davidson B, et al. Non-invasive imaging in coronary syndromes: recommendations of the European Association of Cardiovascular Imaging and the American Society of Echocardiography, in collaboration with the American Society of Nuclear Cardiology, Society of Cardiovascular Computed Tomography, and Society for Cardiovascular Magnetic Resonance. Eur Heart J Cardiovasc Imaging. 2022 Jan 24;23(2):e6-33.
https://academic.oup.com/ehjcimaging/article/23/2/e6/6423983
http://www.ncbi.nlm.nih.gov/pubmed/34751391?tool=bestpractice.com
[90]Steeds RP, Garbi M, Cardim N, et al. EACVI appropriateness criteria for the use of transthoracic echocardiography in adults: a report of literature and current practice review. Eur Heart J Cardiovasc Imaging. 2017 Nov 1;18(11):1191-204.
https://academic.oup.com/ehjcimaging/article-abstract/18/11/1191/3052244
http://www.ncbi.nlm.nih.gov/pubmed/28329307?tool=bestpractice.com
Se indica realizar un ecocardiograma antes del alta en todos los pacientes tras un infarto agudo de miocardio, con el fin de evaluar la función ventricular izquierda después de la terapia de reperfusión coronaria y orientar el pronóstico.[91]National Institute for Health and Care Excellence. Acute coronary syndromes. Nov 2020 [internet publication].
https://www.nice.org.uk/guidance/ng185
[92]Loutfi M, Ashour S, El-Sharkawy E, et al. Identification of high-risk patients with non-ST segment elevation myocardial infarction using strain doppler echocardiography: correlation with cardiac magnetic resonance imaging. Clin Med Insights Cardiol. 2016 May 10;10:51-9.
https://pmc.ncbi.nlm.nih.gov/articles/PMC4863927
http://www.ncbi.nlm.nih.gov/pubmed/27199575?tool=bestpractice.com
Los pacientes con un índice elevado de sospecha que tengan ECG negativos en serie y enzimas cardíacas deben ser controlados detenidamente en una unidad de telemetría o dolor torácico, puesto que puede tardar tiempo hasta que los marcadores cardíacos aumenten.[7]Writing Committee Members; Gulati M, Levy PD, Mukherjee D, et al. 2021 AHA/ACC/ASE/CHEST/SAEM/SCCT/SCMR guideline for the evaluation and diagnosis of chest pain: a report of the American College of Cardiology/American Heart Association Joint Committee On Clinical Practice Guidelines. J Am Coll Cardiol. 2021 Nov 30;78(22):e187-285.
https://www.sciencedirect.com/science/article/pii/S0735109721057958
http://www.ncbi.nlm.nih.gov/pubmed/34756653?tool=bestpractice.com
[93]Amsterdam EA, Wenger NK, Brindis RG, et al. 2014 AHA/ACC guideline for the management of patients with non-ST-elevation acute coronary syndromes: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines. J Am Coll Cardiol. 2014 Dec 23;64(24):e139-228.
https://www.jacc.org/doi/10.1016/j.jacc.2014.09.017
http://www.ncbi.nlm.nih.gov/pubmed/25260718?tool=bestpractice.com
Radiografía de tórax: indicada para descartar causas alternativas de dolor torácico como neumotórax o mediastino ensanchado en la disección aórtica, o complicaciones del SCA como edema pulmonar por insuficiencia cardíaca.[87]Writing Committee, Kontos MC, de Lemos JA, et al. 2022 ACC Expert Consensus Decision Pathway on the evaluation and disposition of acute chest pain in the emergency department: A report of the American College of Cardiology Solution Set Oversight Committee. J Am Coll Cardiol. 2022 Nov 15;80(20):1925-60.
https://www.sciencedirect.com/science/article/pii/S0735109722066189?via%3Dihub
http://www.ncbi.nlm.nih.gov/pubmed/36241466?tool=bestpractice.com
HC: las mediciones de hemoglobina y de hematocrito pueden ayudar a evaluar una causa secundaria de IMSEST (p. ej., sangrado agudo, anemia) y a evaluar trombocitopenia para estimar el riesgo de sangrado.
Urea y creatinina sérica: se debe considerar el aclaramiento de creatinina en pacientes con infarto de miocardio sin elevación del segmento ST (IMSEST), y las dosis de fármacos que son depurados por los riñones se deben ajustar de manera adecuada. En pacientes con una enfermedad renal crónica que se sometan a una angiografía, se puede optar por medios de contraste isosmolares.[94]Neumann FJ, Sousa-Uva M, Ahlsson A, et al; ESC Scientific Document Group. 2018 ESC/EACTS guidelines on myocardial revascularization. Eur Heart J. 2019 Jan 7;40(2):87-165.
https://academic.oup.com/eurheartj/advance-article/doi/10.1093/eurheartj/ehy394/5079120
http://www.ncbi.nlm.nih.gov/pubmed/30165437?tool=bestpractice.com
Electrolitos séricos: los desórdenes electrolíticos pueden predisponer a arritmias cardíacas.
Proteína C reactiva (PCR): la PCR se solicita frecuentemente para descartar otras causas de dolor torácico agudo (p. ej., neumonía).
Pruebas de función hepática: útiles si se considera el tratamiento con fármacos que se someten al metabolismo hepático, y en la evaluación del riesgo de sangrado antes de iniciar la anticoagulación. El deterioro de las pruebas de función hepática también puede sugerir una congestión hepática en pacientes con insuficiencia cardíaca concomitante.
Niveles de glucemia: la hiperglucemia es frecuente en el contexto de un IM agudo, con o sin antecedentes de diabetes.[95]Gholap NN, Mehta RL, Ng L, et al. Is admission blood glucose concentration a more powerful predictor of mortality after myocardial infarction than diabetes diagnosis? A retrospective cohort study. BMJ Open. 2012 Sep 25;2(5):e001596.
https://bmjopen.bmj.com/content/2/5/e001596.long
http://www.ncbi.nlm.nih.gov/pubmed/23015602?tool=bestpractice.com
Existe una controversia con respecto a si un control estrecho de la glucemia puede reducir el riesgo de muerte y morbilidad.[96]de Mulder M, Umans VA, Cornel JH, et al. Intensive glucose regulation in hyperglycemic acute coronary syndrome: results of the randomized BIOMarker study to identify the acute risk of a coronary syndrome-2 (BIOMArCS-2) glucose trial. JAMA Intern Med. 2013 Nov 11;173(20):1896-904.
https://jamanetwork.com/journals/jamainternalmedicine/fullarticle/1735896
http://www.ncbi.nlm.nih.gov/pubmed/24018647?tool=bestpractice.com
Estratificación del riesgo
El tratamiento del SCA requiere una estratificación continua del riesgo de muerte o IM recurrente. El American College of Cardiology/American Heart Association recomiendan que se estratifique el riesgo de los pacientes con sospecha de SCA en función de la probabilidad de SCA y de los resultados adversos, con el fin de realizar un mejor triaje y ayudar a seleccionar las opciones de tratamiento, especialmente en los entornos en los que no se dispone de pruebas de troponina cardíaca de alta sensibilidad.[2]Rao SV, O'Donoghue ML, Ruel M, et al. 2025 ACC/AHA/ACEP/NAEMSP/SCAI guideline for the management of patients with acute coronary syndromes: a report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation. 2025 Apr;151(13):e771-862.
https://www.ahajournals.org/doi/full/10.1161/CIR.0000000000001309?rfr_dat=cr_pub++0pubmed&url_ver=Z39.88-2003&rfr_id=ori%3Arid%3Acrossref.org
http://www.ncbi.nlm.nih.gov/pubmed/40014670?tool=bestpractice.com
[7]Writing Committee Members; Gulati M, Levy PD, Mukherjee D, et al. 2021 AHA/ACC/ASE/CHEST/SAEM/SCCT/SCMR guideline for the evaluation and diagnosis of chest pain: a report of the American College of Cardiology/American Heart Association Joint Committee On Clinical Practice Guidelines. J Am Coll Cardiol. 2021 Nov 30;78(22):e187-285.
https://www.sciencedirect.com/science/article/pii/S0735109721057958
http://www.ncbi.nlm.nih.gov/pubmed/34756653?tool=bestpractice.com
Existen varias puntuaciones de riesgo que incorporan una serie de variables como los antecedentes clínicos, los síntomas de la angina y sus equivalentes, la exploración física, el ECG, la función renal y los niveles de troponina. Estas variables pueden utilizarse para estimar el riesgo de muerte y de eventos isquémicos cardíacos no mortales: por ejemplo, utilizando la escala de riesgo TIMI o el modelo de riesgo del Global Registry of Acute Coronary Events (GRACE).[2]Rao SV, O'Donoghue ML, Ruel M, et al. 2025 ACC/AHA/ACEP/NAEMSP/SCAI guideline for the management of patients with acute coronary syndromes: a report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation. 2025 Apr;151(13):e771-862.
https://www.ahajournals.org/doi/full/10.1161/CIR.0000000000001309?rfr_dat=cr_pub++0pubmed&url_ver=Z39.88-2003&rfr_id=ori%3Arid%3Acrossref.org
http://www.ncbi.nlm.nih.gov/pubmed/40014670?tool=bestpractice.com
[97]Antman EM, Cohen M, Bernink PJ, et al. The TIMI risk score for unstable angina/non-ST elevation MI: a method for prognostication and therapeutic decision making. JAMA. 2000 Aug 16;284(7):835-42.
https://jamanetwork.com/journals/jama/fullarticle/192996
http://www.ncbi.nlm.nih.gov/pubmed/10938172?tool=bestpractice.com
[
Puntuación de trombolisis en el infarto de miocardio (TIMI) para angina inestable o infarto de miocardio sin elevación del segmento ST
Opens in new window
]
[
Puntuación GRACE para el pronóstico del síndrome coronario agudo
Opens in new window
]
La escala de riesgo TIMI está compuesta de 7 indicadores de riesgo clasificados en la presentación. Se otorga un punto por la presencia de cada uno de los siguientes criterios:
edad >65 años
presencia de ≥3 factores de riesgo de arteriopatía coronaria (AC)
estenosis coronaria previa >50%
desviación del segmento ST en el ECG
aumento de los biomarcadores cardíacos séricos
al menos 2 episodios anginales en las últimas 24 horas
uso de aspirina en los últimos 7 días.
Los pacientes con una escala TIMI de 0 a 2 son de bajo riesgo, de 3 a 4 son de riesgo intermedio, y de 5 a 7 son de riesgo alto. La mortalidad por cualquier causa, tasa de IM y tasa de revascularización urgente a los 14 días aumentan en proporción al número de factores de riesgo presentes en la escala TIMI.
El modelo de riesgo GRACE es una herramienta Web que se puede usar para predecir la mortalidad tanto en pacientes hospitalizados como dados de alta o en pacientes con IM tras un AC inicial.
La clasificación de Killip es otra herramienta que se puede usar para la estratificación del riesgo. Este sistema de clasificación estratifica el riesgo de los pacientes con infarto agudo de miocardio según la evidencia clínica de insuficiencia ventricular izquierda:
Clase I: sin evidencia de insuficiencia cardíaca crónica (ICC)
Clase II: presencia de un tercer ruido cardíaco, estertores de base o aumento de la presión venosa yugular.
Clase III: presencia de edema pulmonar.
Clase IV: shock cardiógeno.
La puntuación HEART incorpora elementos de la historia del paciente, ECG, edad, factores de riesgo y troponina, y se usa para pacientes que están en el ámbito de un servicio de urgencias para evaluar el riesgo de infarto agudo de miocardio, intervención coronaria percutánea, injerto de derivación (bypass) de la arteria coronaria (IDAC) y muerte en las 6 semanas posteriores a la presentación inicial.[98]Backus BE, Six AJ, Kelder JC, et al. A prospective validation of the HEART score for chest pain patients at the emergency department. Int J Cardiol. 2013 Oct 3;168(3):2153-8.
https://www.internationaljournalofcardiology.com/article/S0167-5273(13)00315-X/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/23465250?tool=bestpractice.com
[
Puntuación HEART
Opens in new window
]
Pruebas posteriores
Después de un análisis diagnóstico inicial y de la estratificación del riesgo, se podrían considerar distintas pruebas diagnósticas adicionales.
Péptido natriurético cerebral (BNP) y pro-BNP N-terminal (NT-pro-BNP): la medición de BNP o NT-pro-BNP puede considerarse para complementar la evaluación del riesgo global en pacientes con sospecha de SCA, en particular para predecir el riesgo de mortalidad, insuficiencia cardíaca aguda y desarrollo de fibrilación auricular (FA).[5]Byrne RA, Rossello X, Coughlan JJ, et al. 2023 ESC guidelines for the management of acute coronary syndromes. Eur Heart J. 2023 Oct 12;44(38):3720-826.
https://academic.oup.com/eurheartj/article/44/38/3720/7243210
Perfil lipídico: esta prueba se indica durante las primeras 24 horas del ingreso al hospital para evaluar alteraciones en los lípidos y, por lo tanto, la necesidad de cualquier terapia hipolipemiante.
Angiografía: la angiografía urgente e inmediata está indicada si el paciente está clínicamente inestable o presenta características de riesgo muy alto: dolor continuo o recurrente a pesar del tratamiento, inestabilidad hemodinámica (presión arterial baja o shock) o shock cardiógeno, cambios dinámicos recurrentes en el ECG que sugieren isquemia, arritmia potencialmente mortal (taquicardia ventricular o fibrilación ventricular) o paro cardíaco después de la presentación, o complicaciones mecánicas como insuficiencia mitral de nueva aparición.[2]Rao SV, O'Donoghue ML, Ruel M, et al. 2025 ACC/AHA/ACEP/NAEMSP/SCAI guideline for the management of patients with acute coronary syndromes: a report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation. 2025 Apr;151(13):e771-862.
https://www.ahajournals.org/doi/full/10.1161/CIR.0000000000001309?rfr_dat=cr_pub++0pubmed&url_ver=Z39.88-2003&rfr_id=ori%3Arid%3Acrossref.org
http://www.ncbi.nlm.nih.gov/pubmed/40014670?tool=bestpractice.com
[5]Byrne RA, Rossello X, Coughlan JJ, et al. 2023 ESC guidelines for the management of acute coronary syndromes. Eur Heart J. 2023 Oct 12;44(38):3720-826.
https://academic.oup.com/eurheartj/article/44/38/3720/7243210
[99]Lawton JS, Tamis-Holland JE, Bangalore S, et al. 2021 ACC/AHA/SCAI guideline for coronary artery revascularization: a report of the American College of Cardiology/American Heart Association Joint Committee On Clinical Practice Guidelines. Circulation. 2022 Jan 18;145(3):e18-114.
https://www.ahajournals.org/doi/full/10.1161/CIR.0000000000001038
http://www.ncbi.nlm.nih.gov/pubmed/34882435?tool=bestpractice.com
Se debe medicar antes de la angiografía a los pacientes con antecedentes de anafilaxia o alergia al contraste.[Figure caption and citation for the preceding image starts]: Angiografía por TC de 64 cortes (A) y angiografía convencional (B) que muestran una lesión de alto grado en la arteria coronaria media derecha, indicada por las flechas. Las puntas de flecha muestran artefactos que se pueden confundir con lesiones.De: Schussler JM y Grayburn PA. Heart. 2007 Mar;93(3):290-7 [Citation ends].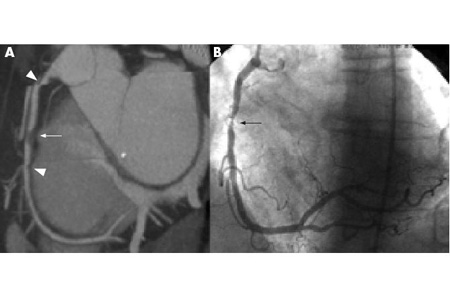 [Figure caption and citation for the preceding image starts]: Angiografía por TC de 64 cortes de un paciente con angina estable que muestra reconstrucción en 3D (A), imágenes reformateadas curvadas (B) y confirmación de una lesión de alto grado en una angiografía convencional (C). Las puntas de flecha muestran placas calcificadas. Dx= diagnósticoDe: Schussler JM y Grayburn PA. Heart. 2007 Mar;93(3):290-7 [Citation ends].
[Figure caption and citation for the preceding image starts]: Angiografía por TC de 64 cortes de un paciente con angina estable que muestra reconstrucción en 3D (A), imágenes reformateadas curvadas (B) y confirmación de una lesión de alto grado en una angiografía convencional (C). Las puntas de flecha muestran placas calcificadas. Dx= diagnósticoDe: Schussler JM y Grayburn PA. Heart. 2007 Mar;93(3):290-7 [Citation ends].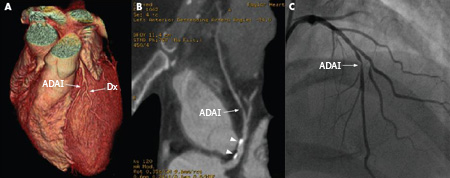
Pruebas de esfuerzo: las pruebas de esfuerzo, incluidas las pruebas de ejercicio en la cinta, podrían ser útiles y se recomiendan en pacientes con probabilidad baja e intermedia previa a la prueba, con un ECG normal y biomarcadores de alta sensibilidad para ayudar a orientar la necesidad de una estrategia invasiva.[93]Amsterdam EA, Wenger NK, Brindis RG, et al. 2014 AHA/ACC guideline for the management of patients with non-ST-elevation acute coronary syndromes: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines. J Am Coll Cardiol. 2014 Dec 23;64(24):e139-228.
https://www.jacc.org/doi/10.1016/j.jacc.2014.09.017
http://www.ncbi.nlm.nih.gov/pubmed/25260718?tool=bestpractice.com
[100]Lindahl B, Andrén B, Ohlsson J, et al. Risk stratification in unstable coronary artery disease. Additive value of troponin T determinations and pre-discharge exercise tests. Eur Heart J. 1997 May;18(5):762-70.
http://www.ncbi.nlm.nih.gov/pubmed/9152646?tool=bestpractice.com
[101]Nyman I, Larsson H, Areskog M, et al. The predictive value of silent ischemia at an exercise test before discharge after an episode of unstable coronary artery disease. Am Heart J. 1992 Feb;123(2):324-31.
http://www.ncbi.nlm.nih.gov/pubmed/1736566?tool=bestpractice.com
La sensibilidad y especificidad de estas pruebas aumenta cuando se combinan con imágenes nucleares para revisar defectos de perfusión miocárdica o con ecocardiografía para evaluar alteraciones en la contractilidad. El hallazgo positivo clave en las pruebas de esfuerzo con imágenes nucleares es la presencia de un defecto reversible. Esto es un área del miocardio que se ve privada de perfusión durante el aumento de demanda miocárdica y reperfusiona al detenerse la actividad. Esto significa estenosis dentro de la circulación coronaria que se puede tratar con intervención coronaria percutánea o IDAC. Las prueba de ejercicio submáximo pueden realizarse en 4-7 días posteriores al infarto de miocardio, mientras que las pruebas limitadas a los síntomas pueden realizarse en 14-21 días después del infarto de miocardio, cuando el paciente ya no presente síntomas isquémicos activos o de insuficiencia cardíaca.[102]Fletcher GF, Ades PA, Kligfield P, et al. Exercise standards for testing and training: a scientific statement from the American Heart Association. Circulation. 2013 Aug 20;128(8):873-934.
https://www.ahajournals.org/doi/full/10.1161/cir.0b013e31829b5b44
http://www.ncbi.nlm.nih.gov/pubmed/23877260?tool=bestpractice.com
Angiografía coronaria por tomografía computarizada (ACTC): puede proporcionar evaluación no invasiva de la anatomía coronaria y la aterosclerosis.[103]Raff GL, Gallagher MJ, O'Neill WW, et al. Diagnostic accuracy of noninvasive coronary angiography using 64-slice spiral computed tomography. J Am Coll Cardiol. 2005 Aug 2;46(3):552-7.
http://www.onlinejacc.org/content/46/3/552
http://www.ncbi.nlm.nih.gov/pubmed/16053973?tool=bestpractice.com
La insuficiencia renal es una contraindicación relativa. Se debe medicar a los pacientes con alergia al contraste antes de la angiografía. Debido al valor predictivo negativo alto de la ACTC, la evidencia sugiere que la ACTC es de utilidad en pacientes con un riesgo bajo a moderado de infarto de miocardio sin elevación del segmento ST (IMSEST). Cuando se compara con la atención estándar de pacientes de bajo riesgo (observación, enzimas seriadas seguidas de una prueba de esfuerzo), la ACTC reduce el tiempo de diagnóstico, el período de permanencia en el servicio de urgencias y tiene una seguridad similar.[104]Hoffmann U, Truong QA, Schoenfeld DA, et al; ROMICAT-II Investigators. Coronary CT angiography versus standard evaluation in acute chest pain. N Engl J Med. 2012 Jul 26;367(4):299-308.
https://www.nejm.org/doi/10.1056/NEJMoa1201161
http://www.ncbi.nlm.nih.gov/pubmed/22830462?tool=bestpractice.com
La ACTC no se indica en pacientes con características de alto riesgo (es decir, cambios isquémicos en el ECG, marcadores cardíacos positivos).[105]Hendel RC, Patel MR, Kramer CM, et al; American College of Cardiology Foundation Quality Strategic Directions Committee Appropriateness Criteria Working Group; American College of Radiology; Society of Cardiovascular Computed Tomography; Society for Cardiovascular Magnetic Resonance; American Society of Nuclear Cardiology; North American Society for Cardiac Imaging; Society for Cardiovascular Angiography and Interventions; Society of Interventional Radiology. ACCF/ACR/SCCT/SCMR/ASNC/NASCI/SCAI/SIR 2006 appropriateness criteria for cardiac computed tomography and cardiac magnetic resonance imaging. J Am Coll Cardiol. 2006 Oct 3;48(7):1475-97.
http://www.onlinejacc.org/content/48/7/1475
http://www.ncbi.nlm.nih.gov/pubmed/17010819?tool=bestpractice.com
[Figure caption and citation for the preceding image starts]: Angiografía por TC de 64 cortes de un paciente con angina estable que muestra reconstrucción en 3D (A), imágenes reformateadas curvadas (B) y confirmación de una lesión de alto grado en una angiografía convencional (C). Las puntas de flecha muestran placas calcificadas. Dx= diagnósticoDe: Schussler JM y Grayburn PA. Heart. 2007 Mar;93(3):290-7 [Citation ends]. [Figure caption and citation for the preceding image starts]: Angiografía por TC de 64 cortes (A) y angiografía convencional (B) que muestran una lesión de alto grado en la arteria coronaria media derecha, indicada por las flechas. Las puntas de flecha muestran artefactos que se pueden confundir con lesiones.De: Schussler JM y Grayburn PA. Heart. 2007 Mar;93(3):290-7 [Citation ends].
[Figure caption and citation for the preceding image starts]: Angiografía por TC de 64 cortes (A) y angiografía convencional (B) que muestran una lesión de alto grado en la arteria coronaria media derecha, indicada por las flechas. Las puntas de flecha muestran artefactos que se pueden confundir con lesiones.De: Schussler JM y Grayburn PA. Heart. 2007 Mar;93(3):290-7 [Citation ends].
 [Figure caption and citation for the preceding image starts]: ECG que muestra depresión del segmento STDe la colección personal del Dr. Syed W. Yusuf y del Dr. Iyad N. Daher, Departamento de Cardiología, University of Texas, Houston; usado con autorización [Citation ends].
[Figure caption and citation for the preceding image starts]: ECG que muestra depresión del segmento STDe la colección personal del Dr. Syed W. Yusuf y del Dr. Iyad N. Daher, Departamento de Cardiología, University of Texas, Houston; usado con autorización [Citation ends].
 [Figure caption and citation for the preceding image starts]: Angiografía por TC de 64 cortes de un paciente con angina estable que muestra reconstrucción en 3D (A), imágenes reformateadas curvadas (B) y confirmación de una lesión de alto grado en una angiografía convencional (C). Las puntas de flecha muestran placas calcificadas. Dx= diagnósticoDe: Schussler JM y Grayburn PA. Heart. 2007 Mar;93(3):290-7 [Citation ends].
[Figure caption and citation for the preceding image starts]: Angiografía por TC de 64 cortes de un paciente con angina estable que muestra reconstrucción en 3D (A), imágenes reformateadas curvadas (B) y confirmación de una lesión de alto grado en una angiografía convencional (C). Las puntas de flecha muestran placas calcificadas. Dx= diagnósticoDe: Schussler JM y Grayburn PA. Heart. 2007 Mar;93(3):290-7 [Citation ends].
 [Figure caption and citation for the preceding image starts]: Angiografía por TC de 64 cortes (A) y angiografía convencional (B) que muestran una lesión de alto grado en la arteria coronaria media derecha, indicada por las flechas. Las puntas de flecha muestran artefactos que se pueden confundir con lesiones.De: Schussler JM y Grayburn PA. Heart. 2007 Mar;93(3):290-7 [Citation ends].
[Figure caption and citation for the preceding image starts]: Angiografía por TC de 64 cortes (A) y angiografía convencional (B) que muestran una lesión de alto grado en la arteria coronaria media derecha, indicada por las flechas. Las puntas de flecha muestran artefactos que se pueden confundir con lesiones.De: Schussler JM y Grayburn PA. Heart. 2007 Mar;93(3):290-7 [Citation ends].