Complicaciones
Las tasas de síndrome compartimental abdominal (SCA) se estiman en aproximadamente 20% después de la reparación abierta de un aneurisma aórtico abdominal roto (AAA).[2][217] En una pequeña revisión retrospectiva, se notificó SCA en 34 % de los pacientes después de la reparación abierta de AAA roto y en 21 % después de la reparación endovascular de un aneurisma (EVAR).[218] En un estudio poblacional a nivel nacional (Swedish Vascular Registry) se observó que después de la reparación de AAA roto, el SCA se desarrolló en un 6.8% después de la reparación abierta en comparación con el 6.9% después de la EVAR.[219] Una revisión sistemática de 46 estudios, que incluyeron 3064 pacientes, mostró que el SCA afecta aproximadamente a 9 % de los pacientes después de la EVAR por rotura de AAA.[220] El SCA se asocia con aumentos significativos en la mortalidad perioperatoria.[220]
Evalúe a los pacientes para el síndrome compartimental abdominal si su afección no mejora después de la EVAR o la reparación quirúrgica abierta de un AAA roto.[42] A los pacientes con síndrome compartimental abdominal después del tratamiento abierto o endovascular de un AAA roto se les debe tratar con laparotomía descompresiva.[2]
El íleo se ha reportado en el 11% de los pacientes, con obstrucción intestinal y la colitis en el 1% de los pacientes que se someten a una reparación abierta.[198] Una revisión informó una prevalencia de isquemia intestinal clínicamente relevante de aproximadamente el 10% después de la cirugía por rotura del aneurisma de aorta abdominal (AAA).[221] Si se sospecha isquemia colónica en pacientes sometidos a tratamiento abierto o endovascular para el AAA, se debe considerar la sigmoidoscopia flexible para confirmar el diagnóstico.[2] La colitis isquémica que requiere colectomía es rara.
Después de la reparación endovascular del aneurisma (EVAR) y la reparación abierta del aneurisma aórtico abdominal (AAA), existe una incidencia significativa de lesión renal aguda (LRA).[222][223][224] En una reparación abierta, esto parece ser transitorio. Sin embargo, después de la EVAR, las causas son multifactoriales, y la disminución de la función renal es significativamente mayor (especialmente, con la fijación suprarrenal) que en la cirugía abierta.[225] El DRA después de EVAR se asocia con un aumento de la morbilidad y la mortalidad a medio plazo.[222] Se debe considerar una estrategia para preservar la función renal mediante la reducción de la dosis de medios de contraste yodados, la retirada de fármacos nefrotóxicos y la garantía de una hidratación adecuada en pacientes sometidos a EVAR de un AAA complejo.[2] También se debe considerar la preservación de las arterias renales accesorias grandes (4 mm).[2] Los datos de pequeños ensayos controlados aleatorizados respaldan el uso potencial de varias intervenciones, incluyendo manitol, suplementos antioxidantes, un abordaje extraperitoneal para reparaciones abiertas y péptido natriurético auricular humano, para reducir la incidencia de LRA después de una reparación electiva de AAA.[226] Sin embargo, los ensayos aleatorios multicéntricos de mayor tamaño y calidad ayudarán a determinar qué intervenciones son efectivas.
El síndrome postimplantacional, una complicación poco conocida de la reparación endovascular de aneurismas (EVAR), ocurre en el período postoperatorio temprano y puede durar hasta 10 días después de EVAR.[227] Son típicos la fiebre, el malestar general y el dolor de espalda, que pueden ser consecuencia de la liberación de citocinas. Los eventos cardiovasculares mayores tempranos son más comunes en pacientes que desarrollan síndrome postimplantacional, aunque no parece haber implicaciones a largo plazo ni impacto en la mortalidad.[227][228]
Las tasas de amputación por isquemia de extremidades fueron muy bajas (0.1% a los 30 días) en una serie de gran tamaño muestral de pacientes (n = 1135) que se sometieron a una reparación abierta.[198] Se debe evaluar inmediatamente a los pacientes con isquemia de las extremidades inferiores de nueva aparición o empeoramiento con el fin de detectar problemas relacionados con el injerto, como torceduras u oclusión de las extremidades.[2]
La isquemia de la médula espinal es poco frecuente después de la reparación endovascular de aneurisma (EVAR), con una incidencia del 0,21 % en el registro de los colaboradores de EUROSTAR.[229] En un análisis retrospectivo del tratamiento endovascular de emergencia para la rotura del aneurisma de aorta abdominal, 4 de 35 pacientes (11,5%) desarrollaron isquemia de la médula espinal después de la operación.[230] Se ha reportado isquemia tardía de la médula espinal (desarrollada 2 días después de la EVAR).[231] El aumento del tiempo quirúrgico, la manipulación intravascular y la anatomía difícil contribuyen a aumentar el riesgo de isquemia de la médula espinal.[232] El reconocimiento temprano es esencial, con un tratamiento que incluye drenajes espinales y la administración de esteroides. Solo el 25% de los casos se recupera, el 25% muestra alguna mejoría y el 50% ninguna mejoría.[232]
El daño a los nervios autónomos (presentes en la bifurcación aortoilíaca) durante la disección, así como la reducción del suministro de sangre en la pelvis, pueden provocar impotencia y eyaculación retrógrada. La reparación endovascular de aneurismas (EVAR) también puede provocar una disfunción eréctil significativa, principalmente debido a la oclusión de la arteria ilíaca interna (IIA). Los estudios que comparan las tasas de disfunción eréctil después de la reparación abierta frente a EVAR han mostrado hallazgos inconsistentes. Una revisión estimó la incidencia de nueva disfunción eréctil entre el 20% y el 83% en el primer año después de la reparación abierta (la variación depende del tipo de ensayo).[233] La incidencia estimada de nueva disfunción eréctil no fue superior al 14.3% después de la reparación endovascular (y fue peor después de la oclusión bilateral en lugar de la unilateral).[233] Sin embargo, un estudio prospectivo de un solo centro no encontró diferencias estadísticamente significativas en la disfunción eréctil de novo entre los grupos de reparación abierta y EVAR.[234] Aproximadamente, el 27% de los pacientes informaron disfunción eréctil antes de la reparación abierta, aumentando al 53% 1 año después de la cirugía. Las frecuencias correspondientes después de la EVAR fueron del 43% y el 59%, respectivamente.[2][234] Para los pacientes tratados por aneurisma de aorta abdominal que están preocupados por una disfunción sexual de nueva aparición postoperatoria, se debería considerar la derivación a equipos especializados.[2]
Una serie de casos informó aneurismas paranastomóticos en el 10% de los pacientes después del injerto de bypass aórtico.[235] La tasa de pseudoaneurisma anastomótico femoral puede ser tan alta como 20% a los 10 años después de la reconstrucción aortobifemoral para el aneurisma de aorta abdominal.[236] Para los pacientes con formación de aneurisma paraanastomótico, se debe considerar la infección como causa subyacente.[2] La infección del injerto puede ser la causa subyacente de la formación de aneurismas secundarios, particularmente dentro de los primeros años después de la reparación.[2] Para los pacientes con formación de aneurisma paraanastomótico aorto-ilíaco no infeccioso después de una reparación previa de un aneurisma aórtico abdominal, se debe considerar preferentemente la reparación endovascular.[2][237]
La dilatación del cuello aórtico ocurrió en el 24,6% de los pacientes con reparación de aneurisma endovascular durante 15 meses a 9 años de seguimiento.[154] Un evento clínico compuesto de endofuga, migración y reintervención fue significativamente más frecuente en este grupo que en los pacientes sin dilatación del cuello aórtico.
Puede ser el resultado de una infección durante la implantación, o de una siembra hematógena después de procedimientos dentales o endoscópicos con biopsia. La incidencia es baja: un estudio de cohorte retrospectivo encontró que la tasa de infección del injerto a 2 años fue del 0,19% después de la reparación abierta frente al 0,16% con la reparación endovascular del aneurisma.[238] La extirpación quirúrgica del endoinjerto infectado es el tratamiento óptimo; existe una alta tasa de mortalidad con el tratamiento médico únicamente.[2][239]
La obstrucción ureteral se relaciona con el atrapamiento de uréteres por una fibrosis perianeurismática inflamatoria de etiología no resuelta más que con una compresión del aneurisma.[240] Más frecuentemente, la compresión ureteral se asocia a un aneurisma aórtico inflamatorio. Adherencias retroperitoneales grandes pueden provocar una obstrucción ureteral en el 18% de los pacientes. La vena cava inferior también puede verse afectada.[241]
La obstrucción duodenal es una consecuencia de la compresión del duodeno en su curso retroperitoneal fijo entre la aorta aneurismal y la arteria mesentérica superior.[240]
Se ha informado que la incidencia de oclusión de la extremidad del injerto hasta 10 años después de la reparación abierta del aneurisma aórtico abdominal está entre el 2,6% y el 3,0%.[242][243] El riesgo de oclusión del injerto es mayor con la reparación endovascular del aneurisma (EVAR), con una incidencia informada de hasta el 7,2% en los estudios de seguimiento.[244] Las torceduras son un factor de riesgo para la oclusión de las extremidades del injerto después de la EVAR.[245]
La endofuga es el flujo sanguíneo persistente fuera del injerto y dentro del saco del aneurisma después de la reparación endovascular del aneurisma (EVAR).[246][247] No es una complicación después de una reparación quirúrgica abierta.
La vigilancia posoperatoria puede detectar endofugas importantes y una expansión de la bolsa de aneurisma.
Solicite una angiografía por TC con contraste si se sospecha endofuga. Use ultrasonido con contraste si la TC con contraste está contraindicada.[42]
El riesgo de endofuga luego de una EVAR es del 24%.[246] Hay cinco tipos de endofuga.
Tipo I:
Fuga en el sitio de inserción (tipo IA en el extremo proximal del endoinjerto u oclusor ilíaco; tipo IB en el extremo distal); por lo general, pueden producirse fugas inmediatas, pero tardías.[Figure caption and citation for the preceding image starts]: Endofuga tipo I en anastomosis distal de la ilíaca izquierda (fuga marcada con un círculo)University of Michigan, específicamente los casos del Dr. Upchurch que reflejan los Departamentos de Cirugía Vascular y Radiología [Citation ends].
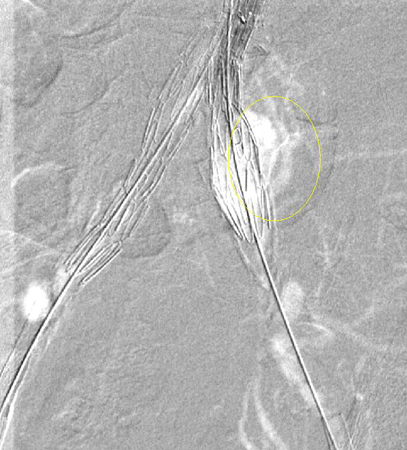
Debe hacerse todo lo posible para reparar la fuga interna de tipo I antes de completar el procedimiento (p. ej., moldeado con balón de la zona de sellado proximal, colocación de un manguito proximal, endostaples, embolización líquida).[248] Para los pacientes con un sellado proximal comprometido después de la reparación endovascular del aneurisma aórtico abdominal, se debe considerar la extensión proximal con dispositivos fenestrados y ramificados.[2] La endofuga persistente de tipo IA puede requerir la conversión a reparación abierta, siempre que el riesgo quirúrgico sea aceptable.[2][77][249][Figure caption and citation for the preceding image starts]: Extensión de endoprótesis expandida para la misma endofuga tipo I (marcada con un círculo)University of Michigan, específicamente los casos del Dr. Upchurch que reflejan los Departamentos de Cirugía Vascular y Radiología [Citation ends].
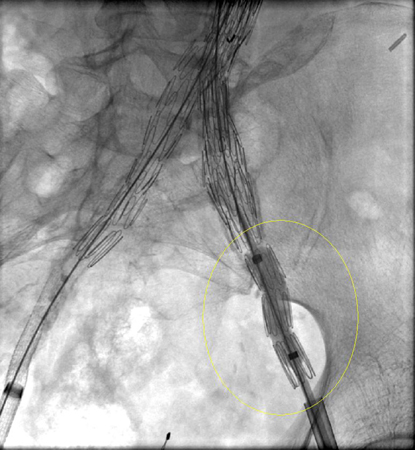 [Figure caption and citation for the preceding image starts]: Resolución de la endofuga tipo I, resuelta con la expansión de la extensiónUniversity of Michigan, específicamente los casos del Dr. Upchurch que reflejan los Departamentos de Cirugía Vascular y Radiología [Citation ends].
[Figure caption and citation for the preceding image starts]: Resolución de la endofuga tipo I, resuelta con la expansión de la extensiónUniversity of Michigan, específicamente los casos del Dr. Upchurch que reflejan los Departamentos de Cirugía Vascular y Radiología [Citation ends].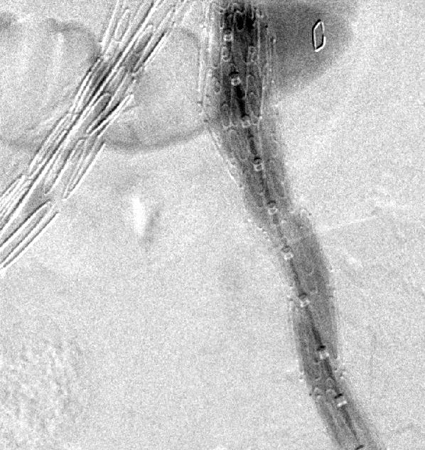
Tipo II:
Fuga persistente de rama.[Figure caption and citation for the preceding image starts]: Endofuga tipo II (marcada con un círculo) descubierta en seguimiento con TCUniversity of Michigan, específicamente los casos del Dr. Upchurch que reflejan los Departamentos de Cirugía Vascular y Radiología [Citation ends].
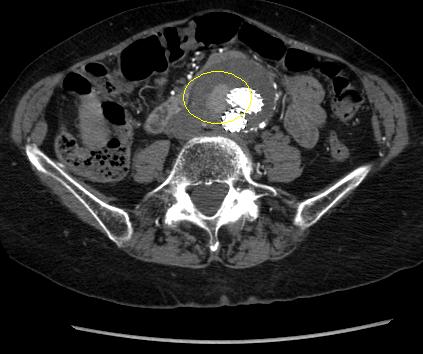
Puede ocurrir una resolución espontánea, aunque la persistencia puede provocar un crecimiento del saco.[250]
Si se observa una endofuga de tipo II u otra alteración preocupante en la imagen por TC con contraste 1 mes después de haber realizado la EVAR, se recomienda realizar un estudio por imágenes postoperatorio a los 6 meses.[77] Alrededor del 50% de las endofugas tipo II se diagnostican antes de los 30 días de seguimiento, el 40% se diagnostican después de 30 días de seguimiento y el 8% se diagnostican después de 12 meses de seguimiento.[251]
El tratamiento solo debe considerarse en presencia de un crecimiento significativo del saco del aneurisma (≥10 mm en comparación con el valor inicial o con el diámetro más pequeño durante el seguimiento utilizando la misma modalidad de imagen y método de medición), principalmente por medios endovasculares, siempre que se hayan excluido causas alternativas, incluidas las endofugas de tipo I o III.[2]
El tratamiento de elección es la embolización transarterial con espiral, aunque también se han reportado la ligadura laparoscópica de ramas colaterales, la punción translumbar directa del saco, la embolización translumbar y la embolización transcaval transcatéter.[247][252][253][254][255][256][257][258][259][260][261][262][263]
Tipo III:
Defecto en el injerto y fuga a través de roturas en el material, desconexión del injerto o desintegración del material.[246][247][264]
Se indica la reparación en el momento de su descubrimiento (extensión de la endoprótesis endovascular).[2][77][253][265]
Tipo IV:
Fuga debido a la porosidad de la pared del injerto.[246][247]
Estas fugas son infrecuentes y se autolimitan con endoprótesis más nuevas.[77][253]
Tipo V (endotensión):
La endotensión es el aumento de presión intrasaco luego de la EVAR. La endofuga no se visualiza en exploraciones tardías por TC con contraste.
La endotensión es menos frecuente con los injertos de nueva generación.[77]
No hay método estandarizado para medir la endotensión ni consenso sobre la terapia indicada en ausencia de agrandamiento de aneurisma; sin embargo, se sugiere realizar un tratamiento de la endotensión para evitar la rotura del aneurisma en pacientes seleccionados con expansión continua de aneurisma.[77][247]
La incidencia es de entre el 3% y el 29%, y por lo general afecta a los dedos (síndrome del dedo del pie azul). Existe un 5% de incidencia de embolización distal que resulta en isquemia crítica de las extremidades, isquemia de los dedos y mionecrosis de pantorrilla.[266]
Los pacientes con enfermedad aneurismática presentan una alta prevalencia de hernias de la pared abdominal y del 11% al 37% tienen hernias incisionales posoperatorias después de la cirugía abdominal.[267] El aumento de malla durante el cierre de la incisión para la reparación abierta de un aneurisma aórtico abdominal puede ayudar a reducir la aparición de hernias incisionales.[2][267]
El uso de este contenido está sujeto a nuestra cláusula de exención de responsabilidad