Recomendaciones
Urgente
El tiempo es cerebro": si sospecha un accidente cerebrovascular, trabaje rápidamente en la evaluación inicial y establezca un objetivo de un acceso rápido a la tomografía computarizada (TC).
El inicio temprano de las estrategias de reperfusión (trombólisis intravenosa o trombectomía mecánica) dentro de las 4.5 horas posteriores al inicio de los síntomas, si no está contraindicado, se asocia con mejores resultados funcionales.[65][66][67]
Sospeche de accidente cerebrovascular en un paciente con síntomas neurológicos focales repentinos (nuevos, inicios agudos o al despertar del sueño):[68]
Debilidad unilateral o parálisis en la cara, el brazo o la pierna
Pérdida sensorial unilateral
Disartria o disfasia expresiva o receptiva
Problemas de visión (p. ej., hemianopsia)
Dolor de cabeza (dolor de cabeza repentino, intenso e inusual)
Dificultad con la coordinación y la marcha
Vértigo o pérdida del equilibrio, especialmente con los signos anteriores.
Descarte la hipoglucemia (un imitador de un accidente cerebrovascular) como la causa de estos síntomas.[69]
Utilice una herramienta validada para ayudar al diagnóstico en personas con sospecha de accidente cerebrovascular:[69]
En el servicio de urgencias: utilice la escala ROSIER (siglas para ´Recognition of Stroke in the Emergency Room´) para establecer el diagnóstico rápidamente.[69]
En la comunidad: use una FAST (prueba del habla cara y brazo) para detectar un accidente cerebrovascular en personas con inicio repentino de síntomas neurológicos.[69]
Ingrese a todas las personas con sospecha de accidente cerebrovascular directamente a una unidad de accidente cerebrovascular hiperagudo (o agudo) lo antes posible; las guías de práctica clínica del Reino Unido recomiendan realizar esta acción dentro de las 4 horas posteriores a la presentación.[69]
Determine el momento de inicio de los síntomas porque este es el factor principal que determinará la elegibilidad para la trombólisis (es decir, dentro de las 4.5 horas posteriores al inicio de la trombólisis intravenosa).[64][69]
Si el inicio no fue presenciado, la definición de inicio de los síntomas es el momento en que se ha visto bien al paciente por última vez.[69]
Solicite estudios por imágenes cerebrales lo antes posible (como máximo en el plazo de 1 hora de su llegada al hospital).[64] La cabeza de TC no realzada es la prueba diagnóstica de elección en el accidente cerebrovascular agudo.
Recuerde que:
El accidente cerebrovascular isquémico es un diagnóstico clínicobasado en signos y síntomas.
Una tomografía computarizada normal no descarta un accidente cerebrovascular; particularmente durante las primeras horas, la tomografía computarizada puede ser normal o mostrar cambios muy sutiles de isquemia.
Principales recomendaciones
Obtenga una breve anamnesis (incluso de testigos o familiares más cercanos) seguida de un examen neurológico abreviado utilizando la Escala de accidentes cerebrovasculares de los Institutos Nacionales de Salud.[70] [ Escala de accidente cerebrovascular del NIH Opens in new window ]
Esta herramienta mide el grado de déficit neurológico. Las puntuaciones más altas indican un accidente cerebrovascular más grave.
Evalúe el nivel de conciencia del paciente mediante la escala de coma de Glasgow. [ Escala de Coma de Glasgow Opens in new window ]
En personas con un nivel alterado de conciencia o coma, descarte la hemorragia y otros imitadores como las convulsiones. Véase diferenciales.
Solicite estudios por imágenes cerebrales lo antes posible (como máximo en el plazo de 1 hora de su llegada al hospital).[64] La TC de cabeza es la prueba diagnóstica de elección en el caso de accidente cerebrovascular agudo.
Considere la posibilidad de obtener estudios por imágenes mediante resonancia magnética (IRM) ponderadas por difusión de la cabeza con secuencias específicas de accidente cerebrovascular (con imágenes ponderadas por susceptibilidad [estudios por imágenes de susceptibilidad magnética (SWI)] o estudios por imágenes ponderadas por T2*) si el diagnóstico sigue siendo incierto a pesar de la radiología.[64]
Los pacientes con accidente cerebrovascular con presentación tardía para los que la reperfusión (trombólisis o trombectomía mecánica) está potencialmente indicada deben someterse a una perfusión por TC o RM lo antes posible (como máximo en el plazo de 1 hora desde la llegada al hospital). Una alternativa para los pacientes que se despiertan con un accidente cerebrovascular es la resonancia magnética que mide el desajuste DWI-FLAIR (resonancia magnética ponderada por difusión y desajuste de resonancia magnética de recuperación de inversión atenuada por líquido).[64]
En pacientes con sospecha de oclusión de vaso grande que son candidatos para trombectomía endovascular, solicite una angiografía por TC después del escáner cerebral inicial.[64]
Los candidatos para la trombectomía por sí sola incluyen pacientes que no pueden recibir trombólisis (p. ej., con contraindicaciones que incluyen cirugía reciente o uso actual de anticoagulantes).[64]
En candidatos a trombectomía además de trombólisis, solicite una angiotomografía computarizada (ATC) o una angiorresonancia magnética (ARM con contraste después (o con) la cabeza de la TC inicial.[69]
No retrase la terapia con trombólisis intravenosa (si está indicada)mientras:
Esperar resultados o esperar para realizar pruebas, a menos que sospeche contraindicaciones que deben descartarse primero (p. ej., hipoglucemia, coagulopatía).[71][72] El tratamiento debe iniciarse dentro de las 4.5 horas posteriores al inicio de los síntomas del accidente cerebrovascular Y después de excluir la hemorragia intracraneal.[64][69]
Esperar para realizar ATC o ARM, o esperar resultados.[71]
Solicite en el caso de todos los pacientes:
Glucosa sérica para descartar hipoglucemia e hiperglucemia antes de administrar trombólisis.[69][70]
Electrolitos séricos para descartar la alteración electrolítica como causa de inicio repentino de signos neurológicos.
Urea y creatinina séricas para descartar la insuficiencia renal porque puede ser una contraindicación potencial para algunas intervenciones de accidente cerebrovascular.
Enzimas cardíacas para descartar el infarto de miocardio concomitante.
Hemograma completo para descartar anemia o trombocitopenia antes de un posible inicio de trombólisis, anticoagulantes o antitrombóticos.
Tiempo de protrombina y tiempo de tromboplastina parcial (con cociente internacional normalizado) para descartar la coagulopatía.
ECG para descartar arritmia cardíaca o isquemia, que son relativamente comunes en el accidente cerebrovascular isquémico.
Considere una prueba de toxicología sérica si sospecha ingestión de sustancias tóxicas. Los signos y síntomas pueden imitar un accidente cerebrovascular.
Sospeche de accidente cerebrovascular en un paciente con síntomas neurológicos focales repentinos (nuevos, de inicio agudo o al despertar del sueño):[68]
Debilidad unilateral o parálisis en la cara, el brazo o la pierna
Pérdida sensorial unilateral
Disartria o disfasia expresiva o receptiva
Problemas de visión (p. ej., hemianopsia)
Dolor de cabeza (dolor de cabeza repentino, intenso e inusual)
Dificultad con la coordinación y la marcha
Vértigo o pérdida del equilibrio, especialmente con los signos anteriores.
Tenga en cuenta que uno o más accidentes isquémicos transitorios (AIT), que pueden ser estereotipados, pueden preceder a un accidente cerebrovascular (como signos o síntomas de advertencia).
Un AIT es una emergencia médica que anuncia un riesgo significativo de accidente cerebrovascular. Los AIT suelen durar unos minutos. Deben ser tratados e investigados con prontitud. Las guías de práctica clínica del Reino Unido recomiendan que las personas que han tenido una sospecha de AIT (sin estratificación del riesgo) deben someterse a una evaluación y prueba diagnóstica especializada en las 24 horas posteriores al inicio de los síntomas.[64][69] Los pacientes con sospecha de AIT deben recibir ácido acetilsalicílico 300 mg inmediatamente, a menos que esté contraindicado.[64] Ver Accidente isquémico transitorio.
Evaluación inicial
El objetivo de la evaluación inicial es reconocer rápidamente un accidente cerebrovascular: "el tiempo es cerebro".
La evaluación inicial rápida y eficiente y el acceso rápido a la exploración por TC (como máximo en el plazo de 1 hora tras la presentación) permiten el inicio temprano de la reperfusión (trombólisis intravenosa o trombectomía mecánica) en las 4,5 horas posteriores al inicio de los síntomas, si no está contraindicado, lo que se asocia con mejores resultados funcionales.[65][66]
En el servicio de urgencias
Utilice la escala ROSIER (Reconocimiento de accidente cerebrovascular en la sala de emergencias) en aquellos con sospecha de accidente cerebrovascular o AIT para establecer el diagnóstico rápidamente.[69][73]
Puntuación -1 punto por cada característica (antecedentes clínicos):
Pérdida del conocimiento o síncope
Actividad convulsiva
Puntuación +1 punto por cada característica (antecedentes neurológicos):
Debilidad asimétrica de la cara
Debilidad asimétrica del brazo
Debilidad asimétrica de las piernas
Alteración del habla
Defecto del campo visual
Una puntuación >0: accidente cerebrovascular probable una puntuación ≤0: accidente cerebrovascular poco probable (pero no descartado).
En el entorno comunitario
Use una herramienta validada como FAST (prueba de cara, brazo y habla) para evaluar a las personas con inicio repentino de síntomas neurológicos (como trastornos visuales o problemas de equilibrio) para un diagnóstico de accidente cerebrovascular:[69][74]
Puntuación 1 punto por cada característica:
Face weakness (debilidad en la cara)
Arm (or leg) weakness (debilidad en el brazo (o pierna))
Speech disturbance (perturbación en el habla)
Sospecha de accidente cerebrovascular si obtiene una puntuación >0; derivar para atención médica de emergencia en el hospital (en ambulancia 999 en el Reino Unido).
Practical tip
Tenga en cuenta que el paciente puede tener déficits neurológicos focales continuos a pesar de un FAST negativo. Continúe manejándolos como lo haría con alguien con un accidente cerebrovascular agudo.[64]
Evidencia: Escalas FAST y ROSIER para identificar el accidente cerebrovascular
A pesar de la evidencia muy limitada, las guías de práctica clínica recomiendan el uso de herramientas de detección validadas para acelerar el acceso a la atención especializada para pacientes con accidente cerebrovascular o AIT en el entorno prehospitalario. Hay menos recomendaciones de guías de práctica clínica sobre el uso de estas herramientas en el entorno del servicio de urgencia (SU).[64][69][75]
[  ]
]
Entorno prehospitalario
La National Clinical Guideline for Stroke de 2023 para el Reino Unido e Irlanda recomienda la prueba Face Arms Speech Time (FAST) en la fase prehospitalaria, pero establece que se requieren más pruebas antes de que se pueda recomendar el reconocimiento de accidente cerebrovascular en la sala de emergencias (ROSIER) para detectar síntomas no FAST en la fase prehospitalaria.[64]
La recomendación sobre el uso de FAST se basa en el consenso del grupo de trabajo y en los resultados de un único estudio de precisión diagnóstica que comparó la aplicación de FAST por parte de paramédicos de ambulancias frente a médicos de atención primaria y frente a derivaciones desde el servicio de urgencias, en un total de 487 personas con sospecha de accidente cerebrovascular remitidas a una unidad de accidentes cerebrovasculares.[74]
El estudio encontró que el diagnóstico de accidente cerebrovascular de los paramédicos de ambulancias utilizando FAST dio un valor predictivo positivo (VPP; es decir, la proporción con una prueba positiva que en realidad tiene la afección o característica) del 78% (IC del 95%: 72% a 84%).[74]
Es posible que FAST no identifique a algunas personas con síntomas de accidente cerebrovascular (p. ej., alteración visual de inicio repentino, disfunción cerebelosa lateral).
Los médicos comunitarios deben continuar tratando a una persona como si tuviera un accidente cerebrovascular sospechoso si sospecha del diagnóstico a pesar de una prueba FAST negativa.
La guía de practica clínica de accidentes cerebrovasculares del National Institute for Health and Care Excellence (NICE) del Reino Unido de 2008 (no modificada en la actualización de 2022) también recomienda usar una herramienta validada, como FAST, fuera del hospital, citando evidencia del mismo estudio de precisión diagnóstica.[69][74]
Una declaración de consenso de la Academia Europea de Neurología y la Organización Europea de Accidentes Cerebrovasculares de 2017 para el manejo prehospitalario del accidente cerebrovascular no recomienda una escala específica, sino que afirma:
Utilizar una escala prehospitalaria simple de accidente cerebrovascular (no se recomienda ninguna específica), a pesar de la falta de evidencia. En su opinión, el beneficio superaría el posible daño y el uso mínimo de recursos.
Tener en cuenta que las escalas (actualmente disponibles en el momento de esta orientación) no son lo suficientemente sensibles como para detectar un accidente cerebrovascular de circulación posterior.
Entorno del servicio de urgencias
NICE recomienda usar una herramienta validada, como ROSIER, en el servicio de urgencias.[69]
Esta recomendación está respaldada por un estudio de validación de la herramienta ROSIER, que incluyó a 343 pacientes con sospecha de accidente cerebrovascular en el servicio de urgencias en la fase de desarrollo y 173 en la fase de validación.[73]
En este estudio, ROSIER mostró un VPP del 90% (IC del 95%: 85% a 95%) cuando fue utilizado por médicos de urgencias.[73]
La National Clinical Guideline for Stroke para el Reino Unido e Irlanda no hace ninguna recomendación específica sobre el uso de ROSIER para detectar el accidente cerebrovascular en el entorno hospitalario de urgencias.[64]
Síntomas/signos según la localización del infarto
Accidente cerebrovascular de circulación anterior
Asociado con isquemia relacionada con la oclusión de las arterias de circulación anterior: el territorio carotídeo, incluidas las arterias cerebrales anterior y media y sus ramas.[76] Los accidentes cerebrovasculares de la circulación anterior son los más comunes de todos los accidentes cerebrovasculares isquémicos.[77]
Busque uno o más de los siguientes síntomas/signos:[76]
Debilidad facial o de extremidades
La pérdida completa o parcial de la fuerza muscular en el rostro, los brazos o las piernas; una presentación habitual en casos de accidente cerebrovascular.
La debilidad en la cara, los brazos y las piernas (los tres al mismo tiempo) sugiere una afectación hemisférica profunda, aunque esto puede no diferenciar el mecanismo del accidente cerebrovascular.
Disfasia expresiva y/o receptiva
Pérdida sensorial (entumecimiento) en la cara y las extremidades superiores y/o inferiores
Los pacientes a menudo describen una pérdida sensorial y parestesias como "entumecimiento".
Es posible que la pérdida sensorial unilateral en el momento del examen neurológico abarque alguna o todas las modalidades primarias.
La pérdida sensorial cortical generalmente afecta las habilidades de procesamiento sensorial fino, como la discriminación de dos puntos, la grafestesia o la estereognosia.
Pérdida de visión por un ojo o un déficit en el campo visual
Puede haber pérdida de la visión monocular y a menudo es transitoria.[78] Es una señal de advertencia precoz que se presenta con frecuencia en casos de estenosis carotídea cervical. Puede presentarse en forma de amaurosis fugax o infarto retininano (oclusión de la arteria central de la retina o de alguna rama); reconozca e investigue estos síntomas con la misma urgencia. Ver Estenosis de la arteria carótida.
Paresia de la mirada (a menudo horizontal y unidireccional): en el accidente cerebrovascular, los ojos mirarán el lado afectado del cerebro
Considere las convulsiones en personas con desviación ocular en sentido contrario (es decir, desviación de la mirada del lado de la lesión cerebral, hacia el lado hemiparético).
Perturbaciones visoespaciales/negligencia
Cuadrantanopía homónima.
Practical tip
El coma es inusual; es más común en personas con isquemia del tronco cerebral.
Accidente cerebrovascular de circulación posterior
Asociado con isquemia relacionada con la oclusión de las arterias de circulación posterior: las arterias vertebrales del cuello, las arterias vertebrales intracraneales, basilares y cerebrales posteriores, y sus ramas.[76]
Busque uno o más de los siguientes síntomas/signos:[76]
Visión doble
Déficits motores y/o sensoriales
Déficits motores: debilidad, torpeza o parálisis de cualquier combinación de brazos y piernas, hasta cuadriplejia, cambiando a veces de un lado a otro en diferentes ataques.
Déficits sensoriales: entumecimiento, incluida la pérdida de sensibilidad o parestesia en cualquier combinación de extremidades, que a veces incluye las cuatro extremidades o ambos lados de la cara o la boca.
Vértigo, con o sin náuseas y vómitos
Por lo general, se informa como una sensación giratoria; también puede describirse como sentirse como estar "en un barco en mares agitados".
A menudo se asocia con nistagmo.
Ataxia o desequilibrio
Disartria.
disfagia
Déficits específicos de los pares craneales (p. ej., debilidad unilateral de la lengua, diplopia)
Síndrome de Horner (tríada hemilateral de miosis, ptosis y anhidrosis facial).
Hemianopsia homónima (es decir, pérdida del campo visual en el lado izquierdo o derecho de la línea media vertical en el mismo lado de ambos ojos)
Síndromes 'cruzados':
Signos de los nervios craneales ipsilaterales
Disfunción de un tracto motor o sensitivo contralateral
Alteración del nivel de conciencia y coma.
Practical tip
El accidente cerebrovascular de la circulación posterior sigue siendo más difícil de reconocer y tratar de manera eficaz que otros tipos de accidente cerebrovascular. Tomar una historia clínica cuidadosa ayudará a identificar a los pacientes con accidente cerebrovascular de circulación posterior, que pueden presentar síntomas recurrentes, tartamudeantes o progresivos, que pueden incluir un nivel alterado de conciencia (no es un síntoma típico de accidente cerebrovascular, pero se observa en la isquemia talámica bilateral).[76]
Síndromes de accidente cerebrovascular lacunar
El accidente cerebrovascular isquémico lacunar se define como una combinación de hallazgos clínicos que sugieren un accidente cerebrovascular agudo debido a una pequeña lesión isquémica subcortical (que puede o no ser visible en las imágenes cerebrales) que se cree que se debe a una enfermedad de los vasos arteriales pequeños cerebrales (es decir, sin una causa arterial grande / cardioembólica obvia).[79] Las siguientes características clínicas y hallazgos de la exploración física son característicos del tipo de síndrome lacunar:[79]
Hemiparesia motora pura. |
|
Accidente cerebrovascular sensorial puro |
|
Hemiparesia atáxica |
|
Accidente cerebrovascular sensoriomotor |
|
Síndrome de la mano con disartria y torpeza |
|
Tome una anamnesis cuidadosa. Asegúrese de establecer contacto con testigos o familiares más cercanos, no solo para obtener un historial preciso, sino también para solicitar el consentimiento para pruebas o tratamientos invasivos, si son necesarios.
Determine el momento de inicio de los síntomas porque este es el factor principal que determinará la elegibilidad para la trombólisis.
Si el inicio no fue presenciado, el momento del inicio de los síntomas es cuando el paciente fue visto por última vez bien.[69]
Pregunte sobre el inicio (repentino o gradual), la duración, la intensidad y la fluctuación de los síntomas.
Los síntomas y signos del accidente cerebrovascular isquémico aparecen repentinamente y son máximos al inicio.
Los pacientes con accidente cerebrovascular de circulación posterior pueden presentar síntomas recurrentes, tartamudeantes o progresivos, que pueden incluir un nivel alterado de conciencia.[76]
Pregunte específicamente sobre la historia clínica previa relevante que influirá en el manejo. Esto incluye (breve historia):
Accidente cerebrovascular reciente
Convulsión o epilepsia
Infarto de miocardio
Fibrilación auricular
Cirugía reciente
Traumatismo reciente
Sangrado
Accidente cerebrovascular hemorrágico
Comorbilidades (específicamente, hipertensión y diabetes)
Consumo actual o pasado de drogas ilícitas
Medicamentos (específicamente, anticoagulantes, insulina y antihipertensivos)
Practical tip
No siempre es fácil de determinar el momento del inicio, en especial si no hay testigos del inicio y el paciente no es capaz de comunicarse; si los síntomas son leves y no se pueden detectar de inmediato, o bien, si se observa tartamudeo o una evolución fluctuante.
Tenga en cuenta los factores de riesgo clave para el accidente cerebrovascular isquémico:
Edad ≥55 años
Un fuerte factor de riesgo no modificable, incluso después de controlar otras afecciones relacionadas con la edad, como la hipertensión.[12]
antecedentes de accidente isquémico transitorio (AIT)
Los pacientes con antecedentes de AIT, particularmente un AIT reciente, tienen un riesgo significativo de accidente cerebrovascular posterior. La mayoría de estos accidentes cerebrovasculares se producen a los pocos días del AIT. Se ha informado una tasa de accidentes cerebrovasculares de 1.5%, 2.1%, 2.8%, 3.7%, y 5.1% en los días 2, 7, 30, 90, y 365, respectivamente, después del AIT.[23] Los estudios muestran que la tasa de ictus tras un AIT podría haber disminuido ligeramente desde 1999, probablemente relacionado con los avances en la prevención del riesgo cardiovascular.[24][25]
antecedentes de accidentes cerebrovasculares isquémicos
Indica que el paciente puede tener más accidentes cerebrovasculares isquémicos en el futuro (particularmente si no se corrigen los factores de riesgo como la hipertensión).[80]
Antecedentes familiares de accidente cerebrovascular a una edad temprana
Son poco frecuentes los trastornos genéticos que causan accidentes cerebrovasculares con herencia mendeliana. Los estudios de gemelos sugieren una pequeña contribución genética al accidente cerebrovascular; los estudios epidemiológicos muestran que los antecedentes familiares de accidente cerebrovascular son un factor de riesgo.[21]
Hipertensión
Fuertemente asociado con un mayor riesgo de accidente cerebrovascular isquémico.[81]
Tabaquismo
Fuertemente asociado con un mayor riesgo de accidente cerebrovascular isquémico.[27]
Diabetes mellitus
Fuertemente asociado con un mayor riesgo de accidente cerebrovascular isquémico.[28]
Fibrilación auricular
Causa al menos una quinta parte de los accidentes cerebrovasculares isquémicos y es uno de los factores de riesgo de accidente cerebrovascular individuales más fuertes.[82]
enfermedades cardiacas concurrentes
Incluye infarto de miocardio, enfermedad valvular, foramen oval permeable con o sin aneurisma interauricular, válvula cardíaca protésica y miocardiopatía.[30]
Anemia falciforme
Se asocia con estenosis vascular, isquemia cerebral y enfermedad de Moyamoya (oclusión vascular que afecta al polígono de Willis).
Dislipidemia
El aumento del colesterol total se asocia con un mayor riesgo de accidente cerebrovascular isquémico. El riesgo de accidente cerebrovascular isquémico disminuye con un colesterol elevado de lipoproteínas de alta densidad (HDL).[83]
Descarte imitadores de accidentes cerebrovasculares comohipoglucemia, tumores cerebrales, convulsiones, sepsis o migraña para garantizar un tratamiento oportuno. Ver diferenciales.
Tenga en cuenta las características clínicas claveque pueden ayudar a distinguir entre accidente cerebrovascular e imitaciones (p. ej., convulsiones, hipoglucemia) en la evaluación inicial a pie de cama:
Sugestivo de imitación | Sugestivo de accidente cerebrovascular |
|
|
Practical tip
El accidente cerebrovascular isquémico es un diagnóstico clínico basado en síntomas y signos. Por lo tanto, distinguir un accidente cerebrovascular verdadero de los imitadores es una habilidad esencial que no puede ser reemplazada solo por estudios por imágenes.
Evalúe el nivel de conciencia del paciente mediante la escala de coma de Glasgow. [ Escala de Coma de Glasgow Opens in new window ]
En personas con un nivel alterado de conciencia o coma, descarte la hemorragia y otros imitadores como las convulsiones. Véase diferenciales.
Considere las convulsiones (paresia de Todd) en personas con conciencia reducida.
Practical tip
El accidente cerebrovascular hemorrágico se asocia con mayor frecuencia con convulsiones, disminución del nivel de conciencia y signos de aumento de la presión intracraneal que el accidente cerebrovascular isquémico.
Realice un examen neurológico abreviadoutilizando la Escala de accidentes cerebrovasculares de los Institutos Nacionales de Salud.[70] [ Escala de accidente cerebrovascular del NIH Opens in new window ]
Esta herramienta mide el grado de déficits neurológicos. Las puntuaciones más altas indican un accidente cerebrovascular más grave.
Verificar si hay evidencia de arritmias cardíacas (p. ej., fibrilación auricular) o patología valvular.
Auscultar el corazón.
Las arritmias, los soplos y el edema pulmonar se asocian con comorbilidades cardíacas, que predisponen a los pacientes a sufrir un accidente cerebrovascular.
Transferir a todas las personas con sospecha de accidente cerebrovascular directamente a una unidad de accidente cerebrovascular hiperagudo (o agudo, según disponibilidad) lo antes posible; las guías de práctica clínica del Reino Unido recomiendan hacer esto dentro en las 4 horas posteriores a la presentación en el hospital.[69]
TC craneal
Solicite estudios por imágenes cerebrales lo antes posible (como máximo en el plazo de 1 hora de su llegada al hospital).[64] La TC de cabeza no realzada es la prueba diagnóstica de elección en el accidente cerebrovascular agudo.
Utilizar la exploración por TC para diferenciar entre accidente cerebrovascular isquémico y accidente cerebrovascular hemorrágico; lo que debe hacerse antes de iniciar la trombólisis en el accidente cerebrovascular isquémico y antes de revertir la anticoagulación en la hemorragia intracerebral inducida por la anticoagulación.[64]
Solo los profesionales de salud con capacitación adecuada deben interpretar los estudios por imágenes de un accidente cerebrovascular agudo para las decisiones de trombólisis o trombectomía.[64]
Recuerde que el accidente cerebrovascular isquémico es un diagnóstico clínico basado en signos y síntomas; una exploración por TC normal no descarta un accidente cerebrovascular, particularmente en las primeras horas, la exploración por TC puede ser normal o mostrar cambios isquémicos muy sutiles. Es muy probable que una resonancia magnética (IRM) en presencia de síntomas continuos muestre el accidente cerebrovascular. Una IRM ponderada en difusión normal es muy poco probable si el paciente ha tenido un accidente cerebrovascular.[85]
Practical tip
Llame a un radiólogo de guardia para aconsejarle una exploración inmediata; hable con el radiólogo para asegurarse de que el paciente tenga el próximo intervalo de tiempo disponible.
Trate de obtener antecedentes colaterales de los familiares con respecto a los medicamentos /historia clínica previa mientras el paciente se somete al escáner.
[Figure caption and citation for the preceding image starts]: Exploración por tomografía computarizada (TC) sin contraste del cerebro en que se observa infarto subagudo ganglionar basal izquierdo aislado con efecto de masa del asta frontal izquierdaCortesía de BMJ Case Reports 2009; doi:10.1136/bcr.10.2008.1139 [Citation ends].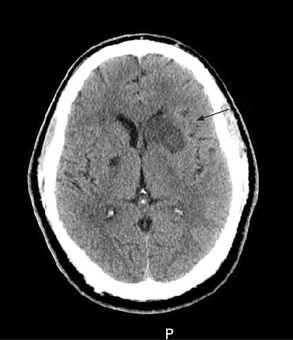
IRM ponderada en difusión
Considere la IRM ponderada en difusión de la cabeza con secuencias específicas de accidente cerebrovascular (DWI con imágenes ponderadas en SWI o T2*) si el diagnóstico sigue siendo incierto a pesar de la TC de la cabeza.[64]
Practical tip
Es muy probable que una IRM en presencia de síntomas continuos muestre el accidente cerebrovascular. Una IRM normal es muy poco probable si el paciente ha tenido un accidente cerebrovascular.[85]
[Figure caption and citation for the preceding image starts]: (A) IRM ponderada en T1 sin contraste. (B) IRM ponderada en T1 poscontraste en que se observa un aumento mínimo de los vasos leptomeníngeos en la región frontal derecha. (C) Imagen ponderada en difusión (DWI) en que se observa un área hiper intensa en la región frontal derecha. (D) En el mapa de coeficiente de difusión aparente (ADC) se observa una lesión hipointensa, que indica difusión restringida que se correlaciona con alta intensidad en DWI y difusión exponencial. (E) El valor de ADC es 0.22 x 10³ mm²/segundo, correspondiente a un infarto hiperagudoDe la colección personal de Eric E. Smith; usado con autorización [Citation ends].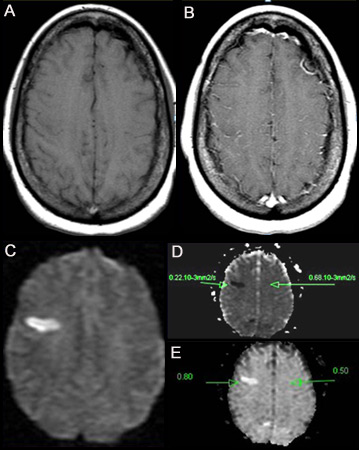
En candidatos a trombectomía endovascular
Los pacientes que se presentan en las 6 a 24 horas posteriores al inicio de los síntomas (es decir, desde la última vez que se supo que estaban bien) pueden ser candidatos potenciales para la trombectomía endovascular.[69]
La selección de los pacientes para la trombectomía mecánica (intervención endovascular) debe ser realizada por médicos con experiencia en el uso de la trombólisis para el accidente cerebrovascular y en la interpretación de estudios por imágenes relevantes. El procedimiento solo debe ser llevado a cabo por especialistas debidamente capacitados con experiencia regular en intervenciones endovasculares intracraneales, con instalaciones adecuadas y apoyo neurocientífico.[86]
Angiografía por TC (ATC)
En pacientes con sospecha de oclusión de vasos grandes que son candidatos para trombectomía, solicite una ATC después de la TC inicial no realzada.[64][69]
No retrase la terapia con trombólisis intravenosa (si está indicada) mientras espera realizar una ATC o espera los resultados.[71] En la práctica, los hospitales que realizan ATC de forma rutinaria en el accidente cerebrovascular agudo administran trombólisis sin esperar el informe de la ATC; revisan la TC simple inicial al mismo tiempo que realizan la ATC.[71]
Use la ATC preferentemente sobre la ARM porque la ATC brinda resultados más rápidos.[69]
En candidatos a trombectomía endovascular además de trombólisis
ATC con contraste
Si el paciente es un candidato potencial para la trombectomía además de la trombólisis, solicite ATC con contraste después (o con) la cabeza inicial de la TC o la IRM para confirmar la oclusión de la circulación anterior o posterior proximal.[64][69]
Estudios por imágenes de perfusión por TC (o equivalente en RM)
Agregue imágenes de perfusión por TC (o equivalente de RM) (como máximo en el plazo de 1 hora de la llegada al hospital)en pacientes con accidente cerebrovascular con una presentación tardía para quienes la reperfusión está potencialmente indicada.[64] Los estudios han respaldado el uso de la exploración de perfusión en pacientes para extender la ventana de trombectomía por encima de las 6 horas.[87][88][89] Una alternativa para los pacientes que se despiertan con un accidente cerebrovascular es la resonancia magnética que mide el desajuste DWI-FLAIR.[64]
[Figure caption and citation for the preceding image starts]: Imagen de etiquetado de espín arterial de IRM en que se observa la hipoperfusión de gran extensión en el hemisferio cerebral derecho. Existe una discordancia clara entre difusión y perfusiónDe la colección personal de Eric E. Smith; usado con autorización [Citation ends].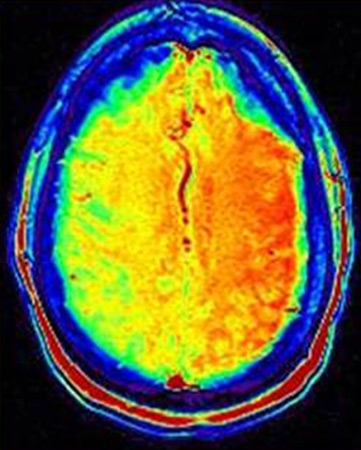
Las guías de práctica clínica del Reino Unido recomiendan la trombectomía (trombólisis ±) en pacientes que se supo por última vez que estaban bien entre 6 horas y 24 horas antes (incluidos los accidentes cerebrovasculares al despertar) con oclusión confirmada de la circulación anterior o posterior proximal, si existe la posibilidad de salvar tejido cerebral como lo muestran los estudios por imágenes de perfusión.[64]
En caso de sospecha de estenosis carotídea: ecografía dúplex carotídea o angiografía por TC o angiografía por RM
Los pacientes con accidente cerebrovascular isquémico que después de la evaluación de un especialista se consideran candidatos para la intervención carotídea deben someterse a estudios por imágenes carotídeas en las 24 horas posteriores a la evaluación. Esto incluye la ecografía dúplex carotídea o la angiografía por TC o la angiografía por RM.[64] Consulte su protocolo local sobre la elección de la investigación. La ecografía dúplex carotídea es la más utilizada.
Ver Estenosis de la arteria carótida.
Practical tip
Solicitar una radiografía de tórax en pacientes con signos o síntomas cardiopulmonares para detectar otras afecciones relevantes como cardiomegalia, disección aórtica o neumonía.
Ecocardiograma
Si sospecha una embolia cardioaórtica, considere la posibilidad de realizar una ecocardiografía transtorácica (ETT) con contraste para evaluar las fuentes cardíacas y aórticas de émbolo.[90] Si no se identifica ninguna fuente en la ETT, use ecocardiografía transesofágica con contraste (TOE) en pacientes seleccionados.[90]
No retrase la trombólisis intravenosa (si está dentro del período de tiempo autorizado y no está contraindicado) mientras espera los resultados o espera para realizar pruebas, a menos que sospeche contraindicaciones que deban descartarse primero (por ejemplo, hipoglucemia, coagulopatía).[71][72]
Análisis de sangre
Mientras se organiza el traslado para la TC/RM, insertar un catéter intravenoso y realizar toma de muestras de sangre.[64]
Solicite en el caso de todos los pacientes:
Glucosa sérica
Electrolitos séricos
Descartar la alteración electrolítica (p. ej., hiponatremia) como causa de la aparición repentina de signos neurológicos.
urea y creatinina séricas
Descartar la insuficiencia renal porque puede ser una contraindicación potencial para algunas intervenciones de accidente cerebrovascular.
Enzimas cardíacas
Descartar el infarto de miocardio concomitante.
Hemograma completo
Descartar anemia o trombocitopenia antes del posible inicio de trombólisis, anticoagulantes o antitrombóticos.
Tiempo de protrombina y tiempo de tromboplastina parcial (con ratio internacional normalizado)
Para descartar la coagulopatía.
No retrase la trombólisis (p. ej., esperando los resultados de las pruebas) si el paciente no tiene antecedentes de uso de anticoagulantes, coagulopatía o una afección que pueda conducir a la coagulopatía.[70]
Considere la posibilidad de realizar una prueba de toxicología sérica si sospecha la ingesta de sustancias tóxicas. Los signos y síntomas pueden imitar un ictus.
electrocardiograma (ECG)
Realizar un ECG en todos los pacientespara descartar arritmia cardíaca (como fibrilación auricular) o isquemia, que son relativamente comunes en el accidente cerebrovascular isquémico.[82]
La fibrilación auricular es un factor de riesgo independiente para el accidente cerebrovascular isquémico e indica un pronóstico más desfavorable.[29] Ver Fibrilación auricular de inicio reciente.
En personas que serían elegibles para el tratamiento de prevención secundaria para la fibrilación auricular o el aleteo:[64]
Realizar una monitorización prolongada del ECG(al menos 24 horas)
Considere la monitorización prolongada secuencial o continua del ECG con un parche externo, un registrador portátil o un registrador en bucle implantable en aquellos en quienes no se ha encontrado otra causa de accidente cerebrovascular, particularmente si tienen un patrón de isquemia cerebral en los estudios por imágenes cerebrales que sugiere cardioembolia.
Practical tip
La fibrilación auricular es una de las principales causas prevenibles de accidente cerebrovascular isquémico. Monitorizar a todos los pacientes con sospecha de accidente cerebrovascular para detectar fibrilación auricular y otras arritmias.[64] Véase el apartado Fibrilación auricular de inicio reciente.
La presencia de fibrilación auricular paroxística se ha subestimado anteriormente, y la última orientación en el Reino Unido es considerar un monitoreo más prolongado y dispositivos implantables en más pacientes.[64][92]
El uso de este contenido está sujeto a nuestra cláusula de exención de responsabilidad