Etiologia
O Trypanosoma cruzi apresenta ciclos silváticos (ocorrência em animais selvagens), peridomésticos e domésticos. O ciclo doméstico é incubado em triatomíneos adaptados às moradias humanas, os quais transmitem o parasita entre os animais domésticos e os seres humanos e destes entre si.[12][44][45] O ciclo silvático é incubado em triatomíneos e em animais selvagens. No período peridoméstico, a infecção persiste em animais domésticos nas áreas circundantes a moradias humanas, em triatomíneos peridomésticos (e eventualmente por meio de troca com o ciclo silvático, como cães e gatos que caçam animais selvagens ou animais selvagens que invadem as áreas circundantes a moradias humanas).[46][47][48][49] Pássaros e animais de sangue frio são resistentes à infecção.
A forma clássica de transmissão do T cruzi é pelo contato com as fezes ou urina de insetos triatomíneos hematófagos (conhecidos como barbeiros), que normalmente atacam à noite.[30][50] Mais de 150 espécies de triatomíneos foram descritas em áreas endêmicas e incluem a espécie Alberprosenia; espécie Belminus; espécie Eratyrus; espécie Microtriatoma; espécie Panstrongylus; espécie Psammolestes; espécie Rhodnius; espécie Triatoma.[44][51][52][53] O principal vetor nos EUA é o T. sanguisuga.[54][55] Há muito poucos relatos de transmissão por vetores em humanos nos EUA. No entanto, o aumento da presença de vetores domésticos, a globalização e a potencial elevação futura da temperatura despertaram a conscientização de que a transmissão por vetor pode se tornar estabelecida nos EUA.[41][56]
CDC: information on species of triatomine bugs in the United States Opens in new window
Os outros modos primários de transmissão incluem transfusões de sangue, consumo de alimentos ou bebidas contaminados e transmissão vertical (causando doença congênita). As formas secundárias de transmissão incluem os transplantes de órgãos, os acidentes em laboratórios, manuseio de animais infectados, atividade sexual (por meio de feridas, esperma ou fluidos menstruais) e infecção dolosa (por inoculação ou oral).[9][44][57][58] É importante observar que a transmissão sexual é possível no caso da doença de Chagas aguda devido ao elevado nível de parasitemia mas, ao contrário dos outros mecanismos, esta via não ocorre no contexto da doença crônica.
Tem-se observado um aumento no número de casos e microepidemias de transmissão oral em países da América Latina (principalmente, na região da Amazônia no Brasil). Vários surtos da doença de Chagas aguda envolvendo grupos de pessoas, muitas vezes famílias, foram relatados como originários de áreas endêmicas. Com maior frequência, a ingestão oral ocorre através de açaí, de outros produtos de palmeiras e de garapa (caldo de cana) feitos em casa. No entanto, a ingestão oral também pode ocorrer após a ingestão de água contaminada com sucos de frutas e após o consumo de carne crua de animais silváticos.[9]
[Figure caption and citation for the preceding image starts]: Triatoma sanguisuga: espécie de vetor com ampla distribuição nos EUACléber Galvão, PhD, Laboratório Nacional e Internacional de Referência em Taxonomia de Triatomíneos, Instituto Oswaldo Cruz, Rio de Janeiro, Brasil (uso autorizado) [Citation ends].
Fisiopatologia
O parasita é classicamente transmitido por um inseto triatomíneo infectado. Os triatomíneos se escondem nos ninhos ou nos locais de descanso de animais selvagens e se alimentam de sangue enquanto o animal está dormindo (ciclo silvático). Algumas dessas espécies de insetos se adaptaram a moradias humanas, onde se escondem em fendas, saindo à noite para o seu repasto sanguíneo (ciclo doméstico). No interior do intestino do vetor, o Trypanosoma cruzi passa por vários estágios sucessivos de desenvolvimento, o último dos quais é uma forma flagelada residente no reto do vetor. A ingestão do repasto sanguíneo faz o vetor defecar e depositar fezes contendo tripomastigotas metacíclicos infecciosos na pele da vítima, próximo à ferida da picada. Ao acordar, a vítima geralmente fricciona a região da picada em que há prurido, forçando as fezes carregadas de tripanossomos para o interior da ferida da picada ou para a conjuntiva. Os tripomastigotas metacíclicos entram na corrente sanguínea da vítima através da ferida da picada ou penetram membranas mucosas como a conjuntiva (resultando no sinal de Romaña). Isso desencadeia o estágio agudo da doença.[4][26][44] Essa forma infecciosa do parasita invade os macrófagos e se transforma em amastigotas intracelulares. Os amastigotas se multiplicam por fissão binária e são liberados como tripomastigotas na corrente sanguínea e nos tecidos.[4][12][26]
O período de incubação varia de acordo com a forma de transmissão. O período de incubação após a transmissão vetorial é de 4 a 15 dias; após a transmissão transfusional, o período é 30 dias ou mais (até 4 meses); após a ingestão de alimentos ou bebidas contaminados, de 3 a 22 dias; e após a transmissão acidental, de até 20 dias. A transmissão vertical pode ocorrer em qualquer período da gestação ou durante o parto.[59][60][61][62][63]
Os tripomastigotas infectam células novas de vários tecidos (por exemplo, sistema reticuloendotelial, miocárdio, músculos e sistema nervoso), transformando-se em amastigotas intracelulares. Após a infecção, ocorrem respostas inflamatórias, lesões celulares e fibrose de forma sequencial (principalmente no coração, no esôfago e no cólon). Na fase aguda, ocorrem vários ciclos de multiplicação do parasita intracelular. Isto leva a uma alta parasitemia que amplifica ainda mais a inflamação e as lesões celulares, embora este processo seja menos intenso durante a doença de Chagas crônica.
Os miócitos e os neurônios (causando denervação autonômica) são geralmente afetados. A destruição direta ocorre por parasitismo intracelular, necrose relacionada com a inflamação e outros mecanismos citotóxicos. A fibrose devida à cardiomiopatia de Chagas é mais intensa que a fibrose relacionada com todas as demais cardiopatias. O comprometimento cardíaco na fase crônica é causado pela destruição do sistema de condução, dos miócitos e dos nervos cardíacos parassimpáticos. A síndrome arrítmica é originada a partir disso, e também em associação com o surgimento de focos arritmogênicos elétricos nas áreas inflamatórias.[4][64][65][66][67] A hipertrofia dos miócitos e a fibrose intensa, com substituição das células destruídas, predispõem a dilatação e a insuficiência cardíacas. A parede ventricular esquerda fica mais fina, tipicamente permitindo a formação de um aneurisma apical. Com frequência aparecem trombos nestes aneurismas, facilmente explicando a ocorrência comum de tromboembolismos sistêmicos e pulmonares.[4][14][66]
A denervação parassimpática intramural é observada de forma irregular no âmbito do sistema gastrointestinal, afetando principalmente o esôfago e o cólon (com maior frequência o cólon sigmoide). O intestino afetado pode se apresentar normal em termos macroscópicos, apesar do distúrbio peristáltico funcional, podendo ainda se dilatar, resultando em megaesôfago ou megacólon. O volvo do cólon sigmoide é uma complicação rara observada nos casos avançados, correlacionando-se com um alto risco de necrose intestinal.[68][69][70][71][72]
Os fatores que predispõem os pacientes na fase indeterminada de infecção por T. cruzi a desenvolverem doença sintomática permanecem indefinidos. Vários fatores podem contribuir nesse sentido.[73][74] Eles incluem: exposição à reinfecção por T. cruzi em áreas com transmissão sustentada com vetor; sexo masculino; carga parasitária; fatores genéticos do hospedeiro; estado nutricional; contexto social e qualidade de vida do paciente; e presença de comorbidades (importante na patogênese da doença de Chagas determinada/sintomática crônica).[74]
[Figure caption and citation for the preceding image starts]: Ciclo de vida do Trypanosoma cruzi, o parasita causador da doença de ChagasCentros de Controle e Prevenção de Doenças, Atlanta, GA, EUA: Biblioteca de Imagens de Saúde Pública (Public Health Image Library) ID # 3384 (Alexander J. da Silva, PhD/Melanie Moser, 2002) [Citation ends].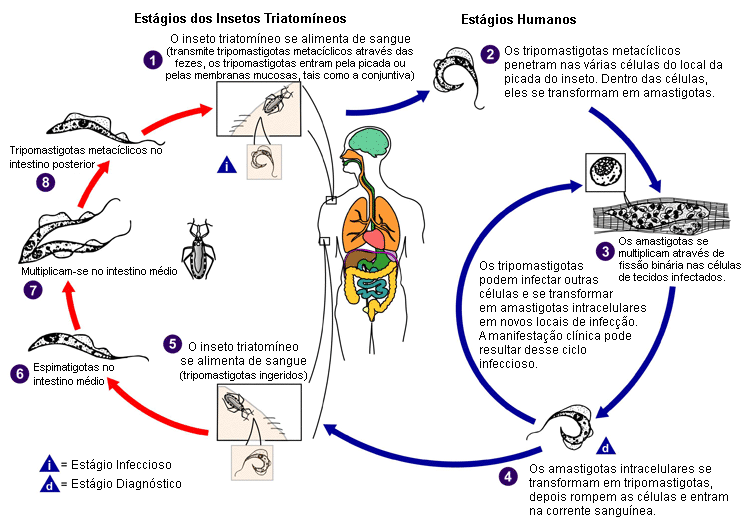
Classificação
Fases clínicas da infecção
Fase aguda
Geralmente dura 3-8 semanas (até 12 semanas em alguns casos) e é definida pela evidência de Trypanosoma cruzi no sangue periférico. Caso não sejam tratados durante essa fase, os pacientes permanecem infectados pelo resto da vida. A maioria dos pacientes não apresenta sintomas, apresenta sintomas leves ou uma síndrome febril inespecífica. Raramente, eles podem apresentar sintomas mais graves como miocardite ou meningoencefalite.[9][10]
Fase crônica
Ele se desenvolve após várias décadas caso o tratamento adequado não seja aplicado durante a fase aguda. Cerca de 60% a 70% dos indivíduos infectados permanecem assintomáticos ao longo de toda a vida, enquanto de 20% a 30% dos pacientes desenvolvem doença sintomática.[2][11] A doença assintomática evolui para doença sintomática crônica em uma taxa de 1.85% a 7.00% ao ano.[2]
As diferentes formas clínicas da doença podem ocorrer de forma separada ou simultânea:
Forma indeterminada: essa é a forma mais comum. Os pacientes podem ficar assintomáticos por décadas após a fase aguda. Embora a sorologia seja positiva para T. cruzi, esses pacientes apresentam resultados de raio-x anatomicamente e fisiologicamente normais do coração, esôfago e cólon, e nenhuma alteração anormal à ecocardiografia.[12]
Forma cardíaca: ocorre entre a 2ª e a 4ª década de vida, geralmente 5-15 anos após a infecção inicial, e afeta até 30% dos pacientes.[4][13][14]
Forma gastrointestinal: incomum em países ao norte do equador. A esofagopatia afeta 5% a 10% dos pacientes, ao passo que a colopatia afeta 3% a 5% dos pacientes.[13]
Forma mista (cardíaca e gastrointestinal).
Fase de reativação
A doença crônica pode se tornar aguda em pacientes imunocomprometidos (por exemplo, AIDS, cânceres hematológicos, após transplante de órgão, terapia imunossupressora com alta dosagem) devido à reativação do T. cruzi.[15] Geralmente, os pacientes apresentam meningoencefalite ou miocardite; no entanto, podem ocorrer manifestações dermatológicas também.[8][16]
A reativação da doença de Chagas faz parte dos critérios de diagnóstico para AIDS no Brasil.[17][18]
O uso deste conteúdo está sujeito ao nosso aviso legal