Abordagem
O tratamento bem-sucedido da gangrena infecciosa requer uma combinação de desbridamento cirúrgico, antibióticos adequados e cuidados de suporte intensivos.[16][22][44]
A gangrena isquêmica requer a revascularização para obstrução e tromboembolismo, junto com o tratamento de quaisquer doenças subjacentes. Medidas para prevenir infecção sobreposta também devem ser usadas.
Amputação do membro
Em casos de sepse grave do membro, é obrigatória a amputação: trata-se de um procedimento em dois estágios que começa com amputação por guilhotina e, posteriormente, quando a infecção cessar, é aconselhável uma amputação definitiva e o fechamento da ferida operatória.[45]
Os pacientes com membros não viáveis (isto é, grandes quantidades de necrose estabelecida, anestesia profunda, paralisia profunda e pulsação inaudível no Doppler), devem ser submetidos a amputação imediata. O nível da amputação é determinado por achados clínicos e pela viabilidade dos tecidos no momento da cirurgia. Todo esforço deve ser feito para preservar o máximo possível de articulações, a fim de diminuir o trabalho de movimentação com prótese e aumentar as chances de reabilitação com sucesso.[39]
Fasciite necrosante
Tipo I (polimicrobiana)
As infecções do tipo I são infecções mistas com anaeróbios. Os organismos podem incluir, por exemplo, Bacteroides ou Peptostreptococcus associado a um anaeróbio facultativo, como Enterobacteriaceae Escherichia coli, Enterobacter, Klebsiella ou Proteus; ou estreptococos não pertencentes ao grupo A. Ela ocorre com mais frequência após procedimentos cirúrgicos e em pacientes com diabetes, alcoolismo, imunossupressão, uso de droga intravenosa (IV) ou doença vascular periférica. A gangrena de Fournier é uma fasciite necrosante do tipo I da região perineal e genital, decorrente de infecção polimicrobiana sinérgica.[4][Figure caption and citation for the preceding image starts]: Fasciite necrosante do subtipo I envolvendo região genital e perineal; imagem feita após extenso desbridamento cirúrgicoAcervo de Jose Contreras-Ruiz (Clinica del Cuidado Integral de Heridas y Estomas) [Citation ends].
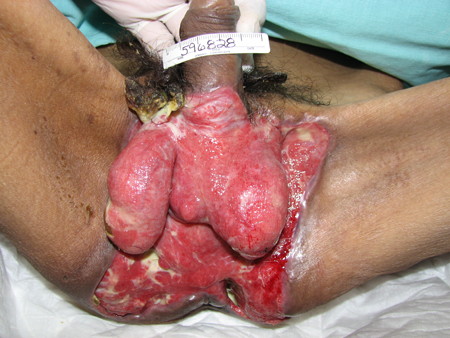
Cuidado cirúrgico: ampla excisão de todo tecido necrótico, colocação de drenos e desbridamento cirúrgico adequado são necessários para o diagnóstico e o tratamento.[44] Após o desbridamento cirúrgico, muitos cirurgiões usam irrigação local com soro fisiológico infundido em bacitracina. Pode ser necessária a amputação.
Antibioticoterapia: para tratamento empírico de infecções mistas do tipo I, a Infectious Diseases Society of America (IDSA) recomenda agentes com eficácia frente a aeróbios (incluindo Staphylococcus aureus resistente à meticilina [MRSA]) e anaeróbios.[16] As opões incluem vancomicina ou linezolida combinada com: piperacilina/tazobactam; um carbapenêmico; ceftriaxona associada a metronidazol; ou uma fluoroquinolona associada a metronidazol. Para pacientes alérgicos à penicilina, podem ser usados clindamicina ou metronidazol com um aminoglicosídeo ou uma fluoroquinolona. Quando informações mais detalhadas estiverem disponíveis e o agente etiológico tiver sido determinado, a antibioticoterapia deve ser alterada para focar no agente específico. Como não há ensaios clínicos atuais definitivos, a IDSA recomenda continuar com antibioticoterapia até que o desbridamento cirúrgico adicional deixe de ser necessário, o paciente melhore clinicamente e a febre esteja ausente por 48 a 72 horas.[16] A Food and Drug Administration (FDA) dos EUA e a European Medicines Agency (EMA) aprovaram a delafloxacina, uma fluoroquinolona antibacteriana, para o tratamento de infecções de pele bacteriana aguda e da estrutura da pele (IPBAEP) causadas por bactérias designadas suscetíveis.[46] A delafloxacina tem suposta atividade contra MRSA e Pseudomonas aeruginosa. Em um ensaio clínico randomizado duplo-cego de fase 2 sobre pacientes com uma IPBAEP, os índices de cura com a delafloxacina foram significativamente maiores que com a vancomicina e comparáveis aos da linezolida.[47]
Em novembro de 2018, a EMA concluiu uma revisão dos efeitos adversos graves, incapacitantes e potencialmente irreversíveis associados aos antibióticos fluoroquinolonas sistêmicos e por via inalatória. Entre os efeitos adversos estão tendinite, ruptura de tendão, artralgia, neuropatias e outros efeitos sobre os sistemas musculoesquelético ou nervoso. Em consequência desta revisão, a EMA agora recomenda restringir o uso dos antibióticos fluoroquinolonas somente a casos de infecção bacteriana grave e com risco de vida. Além disso, ela recomenda que as fluoroquinolonas não sejam usadas para infecções leves a moderadas, a menos que outros antibióticos adequados à infecção específica não possam ser usados; e que também não sejam usadas para tratar infeções não graves, não bacterianas ou autolimitadas. Pacientes mais idosos e os que apresentam comprometimento renal ou que sofreram transplante de órgãos sólidos e aqueles tratados com corticosteroides têm maior risco de danos a tendões. Deve-se evitar a coadministração de uma fluoroquinolona e um corticosteroide.[48] A Medicines and Healthcare Products Regulatory Agency (MHRA) do Reino Unido respalda esta recomendação.[49]
A FDA dos EUA emitiu uma comunicação de segurança semelhante em 2016, restringindo o uso de fluoroquinolonas em casos de sinusite aguda, bronquite aguda e infecções do trato urinário não complicadas.[50] Além dessas restrições, a FDA emitiu avisos sobre o aumento do risco de dissecção de aorta, hipoglicemia significativa e efeitos adversos para a saúde mental em pacientes que tomam fluoroquinolonas.[51][52]
Tipo II (monomicrobiana)
A fasciite necrosante tipo II é uma infecção monomicrobiana, uma forma rara de gangrena mais comumente causada por estreptococos do grupo A (ou C ou G). Geralmente, desenvolve-se em um local de trauma em um membro.[1] Pode também ser causada por MRSA.
Cuidado cirúrgico: a exploração cirúrgica imediata é necessária, usando incisões longitudinais através da fáscia profunda e estendendo-se além das áreas prejudicadas e gangrenosas envolvidas. As áreas de necrose cutânea são excisadas, e a fáscia não viável é desbridada. Em geral, a reexploração é realizada em 24 horas.[22][44] Pode ser necessária a amputação.
Antibioticoterapia: em associação com desbridamento cirúrgico urgente, penicilina associada a clindamicina deve ser administrada para tratar estreptococos do grupo A e inibir sua capacidade de sintetizar toxinas.[16] A clindamicina é usada porque demonstra ser superior à penicilina para o tratamento de fasciite necrosante com indução experimental ou mionecrose causada por estreptococos do grupo A, pois:[22]
Ela reduz a liberação in vitro de exotoxina pirogênica estreptocócica A
Ela não é afetada pelo tamanho do inóculo ou por seu estágio de crescimento
Ela facilita a fagocitose de Streptococcus pyogenes ao inibir a síntese da proteína M
Ela suprime a produção de elementos regulatórios que controlam a síntese da parede celular
Ela tem efeito pós-antibiótico longo.
Se houver alguma dúvida relativa ao agente etiológico (por exemplo, possivelmente Staphylococcus aureus em vez de um Streptococcus do grupo A), deve-se usar nafcilina em vez de penicilina.[1]
Em pacientes alérgicos à penicilina, a vancomicina, a daptomicina ou a linezolida (caso haja alergia coexistente a vancomicina) em monoterapia pode substituir a combinação penicilina-clindamicina ou nafcilina-clindamicina.[16]
A IDSA recomenda uma combinação de doxiciclina associada à ceftriaxona ou cefotaxima para a fasciite necrosante devida ao Vibrio vulnificus, ou uma combinação de doxiciclina associada à ceftriaxona ou ao ciprofloxacino para Aeromonas hydrophila.[16]
A adição de imunoglobulina intravenosa (IGIV) também pode ser considerada, mas os dados sobre eficácia são conflitantes. Alguns estudos observacionais sugerem um modesto benefício, mas um pequeno ensaio clínico duplo-cego controlado por placebo (prematuramente encerrado em decorrência do recrutamento lento de pacientes) e uma grande análise retrospectiva do efeito da IGIV em pacientes com fasciite necrosante desbridada (com choque causado por estreptococos do grupo A ou Staphylococcus aureus) revelaram que a IGIV adjuvante não estava associada à melhora da sobrevida.[53][54][55][56][57] As diretrizes da IDSA não incluem nenhuma recomendação em relação ao uso de IGIV em pacientes com fasciite necrosante com síndrome do choque tóxico estreptocócico, citando a necessidade de estudos adicionais sobre eficácia.[16] Uma revisão Cochrane de 2018 sobre intervenções para infecções necrosantes de tecidos moles em adultos mostrou não haver diferença entre a IVIG (administrada ao longo de 3 dias) e o placebo em termos de mortalidade dentro de 30 dias, nem em eventos adversos graves apresentados na UTI (evidências de baixa certeza).[58] As diretrizes da World Society of Emergency Surgery defendem a consideração da IGIV em pacientes com fasciite necrosante causada por estreptococos do grupo A e evidências de disfunção de órgãos (recomendação fraca), embora reconheçam que o uso de IGIV para o tratamento de infecções necrosantes dos tecidos moles permanece controverso.[12]
A oxigenoterapia hiperbárica (OHB) pode ser considerada como terapia adjuvante após o desbridamento imediato em pacientes com infecções necrosantes dos tecidos moles se não se verificar nenhuma melhora do quadro clínico.[12] É administrada com oxigênio a 100%, com 2 a 3 vezes a pressão atmosférica. Embora não tenham sido publicados ensaios randomizados prospectivos, uma análise retrospectiva mostrou melhora na mortalidade apesar do maior custo de hospitalização e tempo de permanência.[59] Faltam evidências válidas e de alta qualidade para os efeitos da OHB na cicatrização de feridas. Ela não deve protelar a exploração cirúrgica imediata e/ou a antibioticoterapia empírica.
Gangrena gasosa
O tratamento da gangrena gasosa requer uma combinação de desbridamento cirúrgico e antibioticoterapia. A terapia com oxigenoterapia hiperbárica (OHB) não é mais recomendada, pois não apresenta vantagem comprovada ao paciente e pode protelar a ressuscitação e o tratamento.[16]
Cuidado cirúrgico: é obrigatório o desbridamento cirúrgico completo e agressivo para aumentar a sobrevida, preservar os membros e prevenir complicações.[1][6][22] Em pacientes com envolvimento de membros, pode ser necessária a fasciotomia para tratar síndrome compartimental, e ela deve ser realizada imediatamente após o diagnóstico. O desbridamento diário é necessário, sendo extremamente importante remover todo tecido necrótico e infectado. Também é importante considerar a amputação do membro quando necessário, pois essa medida pode salvar vidas.
Antibioticoterapia: atualmente, uma combinação de penicilina e clindamicina é amplamente usada.[16] Alguns estudos demonstraram que inibidores da síntese proteica (por exemplo, clindamicina, cloranfenicol, rifampicina, tetraciclina) podem ser mais eficazes que a penicilina, pois estes inibem a síntese de exotoxinas clostrídicas e diminuem os efeitos tóxicos sistêmicos e locais dessas proteínas.[60] Para pacientes alérgicos à penicilina, uma boa opção é a combinação de clindamicina e metronidazol.
Gangrena isquêmica
Para isquemia aguda dos membros, a menos que contraindicado, todos os pacientes devem receber imediatamente heparina em bolus intravenoso, seguida por infusão contínua de heparina.[61][62] Após o início da heparina, o tratamento varia dependendo da viabilidade do membro. As seguintes características podem ajudar a categorizar a viabilidade de membro agudamente isquêmico:
Viável: sem risco imediato; sem perda sensorial nem fraqueza muscular; sinais arteriais e venosos audíveis por Doppler.
Marginalmente em risco: recuperável se tratado imediatamente; sem ou com mínima perda sensorial (pododáctilos); sem fraqueza muscular; sinais arteriais muitas vezes inaudíveis por Doppler; sinais venosos audíveis por Doppler.
Imediatamente em risco: recuperável com revascularização imediata; perda sensorial além dos pododáctilos acompanhada por dor em repouso; fraqueza muscular leve à moderada; sinais arteriais geralmente inaudíveis por Doppler; sinais venosos audíveis por Doppler.
Irreversível/inviável: perda importante de tecido e/ou dano permanente ao nervo; anestesia profunda; paralisia profunda (rigidez); sinais venosos e arteriais inaudíveis por Doppler.
As opções de tratamento incluem cirurgia, angioplastia transluminal percutânea (ATP) e terapia trombolítica.
Cirurgia
Pacientes com membro ameaçado, mas viável (ou seja, demonstrando dor em repouso, perda sensorial ou fraqueza muscular leve, mas sem áreas consideráveis de necrose) devem submeter-se à revascularização cirúrgica com urgência após anticoagulação com heparina. A maioria desses pacientes terá sofrido um evento embólico, e alterações irreversíveis podem ocorrer dentro de 4 a 6 horas da isquemia profunda. Enquanto a trombólise farmacológica pode dissolver com êxito um êmbolo, o tempo necessário geralmente é muito longo para permitir que essa seja uma alternativa aceitável em comparação à cirurgia.[62]
Em 2010, o resultado do ensaio Bypass versus Angioplasty in Severe Ischaemia of the Leg (BASIL), sobre o teste de bypass versus angioplastia na isquemia grave da perna, foi publicado com base na análise do primeiro tratamento recebido.[63] Os desfechos avaliados foram sobrevida livre de amputação (SLA) e sobrevida global (SG). Ele também comparou a cirurgia de revascularização protética com a venosa, e a angioplastia por balão subíntima com a transluminal, e examinou os desfechos da cirurgia de revascularização após a angioplastia por balão malsucedida. O autor concluiu que a angioplastia por balão estava associada a uma taxa de falha precoce significativamente mais alta que a cirurgia de revascularização. A maioria dos pacientes de angioplastia por balão acabaram precisando de cirurgia. Além disso, os desfechos da cirurgia de revascularização após uma angioplastia por balão malsucedida são significativamente piores que a da cirurgia de revascularização realizada como primeira tentativa de revascularização. A cirurgia de revascularização com veia oferece a melhor SLA e SG em longo prazo e, no geral, a angioplastia por balão parece ser superior à cirurgia de revascularização protética.
ATP
No ensaio BASIL, 450 pacientes com isquemia grave dos membros em consequência de doença infrainguinal foram atribuídos aleatoriamente à ATP ou à cirurgia de revascularização.[64] Após 30 dias, não houve diferença em mortalidade entre os grupos, mas a cirurgia estava associada a uma taxa de morbidade significativamente mais alta (57% versus 41%). Na análise da intenção de tratamento, não houve diferença no objetivo primário (sobrevivência sem amputação) em 1 ano e 3 anos, e a cirurgia estava associada a uma taxa de reintervenção significativamente menor (18% versus 26%). Com base nesses achados, os autores recomendam que a ATP deve ser oferecida primeiro aos pacientes com comorbidades significativas que não têm expectativa de vida maior que 2 anos. Para pacientes com expectativa de vida maior que 2 anos, os benefícios da cirurgia de revascularização podem superar o aumento da morbidade em curto prazo.
Terapia trombolítica
Em pacientes altamente selecionados, a terapia trombolítica intra-arterial com cateter pode ser uma alternativa à cirurgia ou à intervenção percutânea no manejo da isquemia crítica dos membros.[39]
A flegmasia cerulea dolens é uma condição rara, na qual ocorre a obstrução total ou quase total da drenagem venosa de um membro, e pode ser tratada por terapia trombolítica intravenosa para ajudar a prevenir o início e a evolução da gangrena venosa.[65]
Cuidados de suporte intensivos
Em pacientes com tipos infecciosos de gangrena, hipotensão intratável e extravasamento capilar difuso são frequentes, e quantidades maciças de fluidoterapia intravenosa (10-20 L por dia) são geralmente necessárias. Em alguns pacientes, a pressão arterial melhora com fluidoterapia intravenosa somente. Os vasoconstritores podem ser úteis, mas existe pouca informação de ensaios clínicos controlados ou estudos experimentais sobre essa afecção específica. Embora vasoconstritores potentes como a adrenalina possam melhorar a pressão arterial, existe a possibilidade de decorrência de gangrena simétrica, em parte como resultado do medicamento e em parte como resultado da perfusão insuficiente causada pela bactéria, por toxinas e por mediadores endógenos.[16][22]
O uso deste conteúdo está sujeito ao nosso aviso legal