As mulheres com miomas uterinos, em sua maioria, são assintomáticas e não requerem investigação ou tratamento adicional, a menos que seja notado crescimento rápido ou haja outras razões para suspeitar de malignidade pélvica.[2]Bradley LD, Falcone T. Myomectomy. In: Handa VL, Van Le L, eds. Te Linde's operative gynecology. 12th ed. Philadelphia, PA: Lippincott Williams & Wilkins; 2019:325-47.[9]American College of Obstetricians and Gynecologists. ACOG practice bulletin no. 228: management of symptomatic uterine leiomyomas. Jun 2021 [internet publication].
https://www.acog.org/clinical/clinical-guidance/practice-bulletin/articles/2021/06/management-of-symptomatic-uterine-leiomyomas
Os objetivos do tratamento devem estar centrados na segurança e na melhora eficaz dos sintomas e na minimização de persistência ou recorrência dos sintomas, ao mesmo tempo em que lida com o desejo de fertilidade futura e o desejo da paciente quanto à preservação uterina.
Para a finalidade de seleção do tratamento, as pacientes podem ser subagrupadas nas que desejam preservação uterina para fertilidade futura ou outras considerações e nas para as quais a preservação uterina não é uma consideração. Infelizmente, faltam evidências de alta qualidade na literatura para a eficácia da maioria das intervenções para o tratamento de miomas uterinos sintomáticos.[81]Hartmann KE, Fonnesbeck C, Surawicz T, et al. Management of uterine fibroids: comparative effectiveness review No. 195. AHRQ publication no. 17(18)-EHC028-EF. Rockville, MD: Agency for Healthcare Research and Quality; 2017.
https://effectivehealthcare.ahrq.gov/products/uterine-fibroids/research-2017
A Food and Drug Administration (FDA) dos EUA emitiu um comunicado de segurança alertando contra o uso de morcelamento elétrico laparoscópico durante a histerectomia ou miomectomia para o tratamento de mulheres com miomas uterinos. Isso ocorreu porque o morcelamento elétrico apresenta o risco de disseminação de um sarcoma uterino não diagnosticado, com consequente agravamento do prognóstico.[82]US Food and Drug Administration. FDA updated assessment of the use of laparoscopic uterine power morcellators to treat uterine fibroids. Dec 2017 [internet publication].
https://www.fda.gov/downloads/medicaldevices/productsandmedicalprocedures/surgeryandlifesupport/ucm584539.pdf
[83]American College of Obstetricians and Gynecologists. Committee opinion no. 822: uterine morcellation for presumed leiomyomas. Mar 2021 [internet publication].
https://www.acog.org/clinical/clinical-guidance/committee-opinion/articles/2021/03/uterine-morcellation-for-presumed-leiomyomas
O sarcoma uterino é uma doença rara, particularmente na situação de miomas uterinos de longa duração presentes na maioria das pacientes.
Terapias medicamentosas
Entre as pacientes que solicitam preservação uterina, diversas terapias medicamentosas têm sido empregadas e praticamente todos os efeitos salutares cessam ao descontinuar a terapia. As terapias medicamentosas para miomas sintomáticos são reversíveis (assim como seus efeitos salutares) e por isso poupam a fertilidade.[9]American College of Obstetricians and Gynecologists. ACOG practice bulletin no. 228: management of symptomatic uterine leiomyomas. Jun 2021 [internet publication].
https://www.acog.org/clinical/clinical-guidance/practice-bulletin/articles/2021/06/management-of-symptomatic-uterine-leiomyomas
Esses agentes são eficazes na melhora temporária dos principais sintomas associados aos miomas uterinos, como queixas relacionadas a volume e sangramento intenso.[84]Tropeano G, Amoroso S, Scambia G. Non-surgical management of uterine fibroids. Hum Reprod Update. 2008 May-Jun;14(3):259-74.
https://academic.oup.com/humupd/article/14/3/259/684493
http://www.ncbi.nlm.nih.gov/pubmed/18344356?tool=bestpractice.com
Todavia, os efeitos adversos associados ao uso prolongado limitam sua utilidade à curta duração (3 a 6 meses).[85]Cheng MH, Wang PH. Uterine myoma: a condition amenable to medical therapy? Expert Opin Emerg Drugs. 2008 Mar;13(1):119-33.
http://www.ncbi.nlm.nih.gov/pubmed/18321152?tool=bestpractice.com
Embora os contraceptivos orais possam ser usados quando o sangramento menstrual associado a miomas for uma preocupação, a combinação de contraceptivos orais reduz significativamente o sangramento após o uso em longo prazo. Mas não há consenso geral sobre os benefícios e o efeito sobre o crescimento de miomas.[86]Sayed GH, Zakherah MS, El-Nashar SA, et al. A randomized clinical trial of a levonorgestrel-releasing intrauterine system and a low-dose combined oral contraceptive for fibroid-related menorrhagia. Int J Gynaecol Obstet. 2011 Feb;112(2):126-30.
https://www.doi.org/10.1016/j.ijgo.2010.08.009
http://www.ncbi.nlm.nih.gov/pubmed/21092958?tool=bestpractice.com
Os agonistas do hormônio liberador de gonadotrofina (GnRH) (por exemplo, leuprorrelina) rapidamente induzem um estado de baixo estrogênio com amenorreia e resultam em 35% a 65% de redução do mioma, com retorno ao tamanho pré-tratamento pouco depois da cessação do tratamento.[87]Olive DL, Lindheim SR, Pritts EA. Non-surgical management of leiomyoma: impact on fertility. Curr Opin Obstet Gynecol. 2004 Jun;16(3):239-43.
http://www.ncbi.nlm.nih.gov/pubmed/15129053?tool=bestpractice.com
Em virtude dos sintomas vasomotores e da perda óssea observados com o uso prolongado desses agentes, eles não são práticos para uso, exceto se usados no pré-operatório para reverter a anemia e estabilizar o hematócrito antes de miomectomia ou histerectomia.[72]Wallach EE, Vlahos NF. Uterine myomas: an overview of development, clinical features, and management. Obstet Gynecol. 2004 Aug;104(2):393-406.
http://www.ncbi.nlm.nih.gov/pubmed/15292018?tool=bestpractice.com
[87]Olive DL, Lindheim SR, Pritts EA. Non-surgical management of leiomyoma: impact on fertility. Curr Opin Obstet Gynecol. 2004 Jun;16(3):239-43.
http://www.ncbi.nlm.nih.gov/pubmed/15129053?tool=bestpractice.com
O uso de "terapia add-back" com terapia de reposição hormonal pode evitar os efeitos colaterais vasomotores e os efeitos ósseos da terapia com análogos do GnRH.[88]Morris EP, Rymer J, Robinson J, et al. Efficacy of tibolone as "add-back therapy" in conjunction with a gonadotropin-releasing hormone analogue in the treatment of uterine fibroids. Fertil Steril. 2008 Feb;89(2):421-8.
http://www.ncbi.nlm.nih.gov/pubmed/17572410?tool=bestpractice.com
[89]Lethaby AE, Vollenhoven BJ. An evidence-based approach to hormonal therapies for premenopausal women with fibroids. Best Pract Res Clin Obstet Gynaecol. 2008 Apr;22(2):307-31.
http://www.ncbi.nlm.nih.gov/pubmed/17905660?tool=bestpractice.com
A mifepristona é um antiprogestágeno que demonstrou reduzir miomas em cerca de 50% ao longo de um período de 6 meses e melhorar os sintomas relacionados ao mioma. Embora nenhuma perda óssea seja observada com esse tratamento, os sintomas vasomotores e, ainda mais importante, o desenvolvimento de hiperplasia do endométrio limitam bastante sua utilidade.
[  ]
What are the effects of selective progesterone receptor modulators (SPRMs) for premenopausal women with uterine fibroids?/cca.html?targetUrl=http://cochraneclinicalanswers.com/doi/10.1002/cca.1784/fullMostre-me a resposta Pode causar elevações transitórias nas transaminases.[90]Chwalisz K, Garg R, Brenner R, et al. Role of nonhuman primate models in the discovery and clinical development of selective progesterone receptor modulators (SPRMs). Reprod Biol Endocrinol. 2006;4 Suppl 1:S8.
https://www.doi.org/10.1186/1477-7827-4-S1-S8
http://www.ncbi.nlm.nih.gov/pubmed/17118172?tool=bestpractice.com
[91]Sabry M, Al-Hendy A. Medical treatment of uterine leiomyoma. Reprod Sci. 2012 Apr;19(4):339-53.
https://www.doi.org/10.1177/1933719111432867
http://www.ncbi.nlm.nih.gov/pubmed/22378865?tool=bestpractice.com
]
What are the effects of selective progesterone receptor modulators (SPRMs) for premenopausal women with uterine fibroids?/cca.html?targetUrl=http://cochraneclinicalanswers.com/doi/10.1002/cca.1784/fullMostre-me a resposta Pode causar elevações transitórias nas transaminases.[90]Chwalisz K, Garg R, Brenner R, et al. Role of nonhuman primate models in the discovery and clinical development of selective progesterone receptor modulators (SPRMs). Reprod Biol Endocrinol. 2006;4 Suppl 1:S8.
https://www.doi.org/10.1186/1477-7827-4-S1-S8
http://www.ncbi.nlm.nih.gov/pubmed/17118172?tool=bestpractice.com
[91]Sabry M, Al-Hendy A. Medical treatment of uterine leiomyoma. Reprod Sci. 2012 Apr;19(4):339-53.
https://www.doi.org/10.1177/1933719111432867
http://www.ncbi.nlm.nih.gov/pubmed/22378865?tool=bestpractice.com
O dispositivo contraceptivo intrauterino de levonorgestrel diminui significativamente o sangramento em mulheres com menorragia intensa associada a miomas.[92]Grigorieva V, Chen-Mok M, Tarasova M, et al. Use of a levonorgestrel-releasing intrauterine system to treat bleeding related to uterine leiomyomas. Fertil Steril. 2003 May;79(5):1194-8.
http://www.ncbi.nlm.nih.gov/pubmed/12738516?tool=bestpractice.com
[93]Varma R, Sinha D, Gupta JK. Non-contraceptive uses of levonorgestrel-releasing hormone system (LNG-IUS): a systematic enquiry and overview. Eur J Obstet Gynecol Reprod Biol. 2006 Mar 1;125(1):9-28.
http://www.ncbi.nlm.nih.gov/pubmed/16325993?tool=bestpractice.com
É recomendada como tratamento de primeira linha para mulheres com sangramento menstrual intenso associado a miomas com menos de 3 cm de diâmetro que não estejam causando distorção da cavidade uterina.[61]National Institute for Health and Care Excellence. Heavy menstrual bleeding: assessment and management. May 2021 [internet publication].
https://www.nice.org.uk/guidance/ng88
[Evidência C]ed9b9e12-da18-4dd4-9e60-a91e56892f9fguidelineCQuais são os efeitos de um dispositivo intrauterino contraceptivo com levonorgestrel como tratamento para mulheres com sangramento menstrual intenso associado a mioma?[61]National Institute for Health and Care Excellence. Heavy menstrual bleeding: assessment and management. May 2021 [internet publication].
https://www.nice.org.uk/guidance/ng88
Foi demonstrado que os antagonistas do hormônio liberador de gonadotrofina (por exemplo, elagolix, relugolix) reduzem a menorragia intensa em mulheres com miomas uterinos. Esses medicamentos são administrados em combinação com a "terapia add-back" hormonal. O antagonista oral do GnRH elagolix demonstrou reduzir significativamente a menorragia intensa em mulheres com miomas.[94]Schlaff WD, Ackerman RT, Al-Hendy A, et al. Elagolix for heavy menstrual bleeding in women with uterine fibroids. N Engl J Med. 2020 Jan 23;382(4):328-40.
https://www.nejm.org/doi/full/10.1056/NEJMoa1904351
http://www.ncbi.nlm.nih.gov/pubmed/31971678?tool=bestpractice.com
Esquemas suplementares de baixa dose reduziram substancialmente o rubor associado ao tratamento com elagolix.[94]Schlaff WD, Ackerman RT, Al-Hendy A, et al. Elagolix for heavy menstrual bleeding in women with uterine fibroids. N Engl J Med. 2020 Jan 23;382(4):328-40.
https://www.nejm.org/doi/full/10.1056/NEJMoa1904351
http://www.ncbi.nlm.nih.gov/pubmed/31971678?tool=bestpractice.com
[95]Archer DF, Stewart EA, Jain RI, et al. Elagolix for the management of heavy menstrual bleeding associated with uterine fibroids: results from a phase 2a proof-of-concept study. Fertil Steril. 2017 Jul;108(1):152-160.e4.
https://www.doi.org/10.1016/j.fertnstert.2017.05.006
http://www.ncbi.nlm.nih.gov/pubmed/28579415?tool=bestpractice.com
Elagolix (em uma formulação combinada com estradiol e noretisterona) está aprovado pela FDA para o manejo do sangramento menstrual intenso associado a miomas uterinos em mulheres na pré-menopausa.[94]Schlaff WD, Ackerman RT, Al-Hendy A, et al. Elagolix for heavy menstrual bleeding in women with uterine fibroids. N Engl J Med. 2020 Jan 23;382(4):328-40.
https://www.nejm.org/doi/full/10.1056/NEJMoa1904351
http://www.ncbi.nlm.nih.gov/pubmed/31971678?tool=bestpractice.com
O relugolix é outro antagonista oral do GnRH. Está aprovado (também em formulação combinada com estradiol e norestisterona) pela FDA e pela European Medicines Agency (EMA) para o manejo de sintomas associados a miomas uterinos em mulheres na pré-menopausa. A aprovação teve respaldo de vários ensaios clínicos de fase 3 que mostraram que o medicamento era eficaz na redução do sangramento menstrual e era bem tolerado.[96]Barra F, Seca M, Della Corte L, et al. Relugolix for the treatment of uterine fibroids. Drugs Today (Barc). 2019 Aug;55(8):503-512.
https://www.doi.org/10.1358/dot.2019.55.8.3020179
http://www.ncbi.nlm.nih.gov/pubmed/31461087?tool=bestpractice.com
[97]Osuga Y, Enya K, Kudou K, et al. Oral gonadotropin-releasing hormone antagonist relugolix compared with leuprorelin injections for uterine leiomyomas: a randomized controlled trial. Obstet Gynecol. 2019 Mar;133(3):423-33.
https://www.doi.org/10.1097/AOG.0000000000003141
http://www.ncbi.nlm.nih.gov/pubmed/30741797?tool=bestpractice.com
[98]Al-Hendy A, Lukes AS, Poindexter AN 3rd, et al. Treatment of uterine fibroid symptoms with relugolix combination therapy. N Engl J Med. 2021 Feb 18;384(7):630-42.
https://www.doi.org/10.1056/NEJMoa2008283
http://www.ncbi.nlm.nih.gov/pubmed/33596357?tool=bestpractice.com
Os anti-inflamatórios não esteroidais foram testados empiricamente no tratamento clínico de sangramento excessivo, dismenorreia e dor pélvica. Esses agentes reduzem significativamente o sangramento e aliviam a dor em comparação com o placebo, mas são menos eficazes em diminuir o sangramento em comparação com o dispositivo intrauterino de levonorgestrel ou ácido tranexâmico.[99]Bofill Rodriguez M, Lethaby A, Farquhar C. Non-steroidal anti-inflammatory drugs for heavy menstrual bleeding. Cochrane Database Syst Rev. 2019 Sep 19;9:CD000400.
https://www.doi.org/10.1002/14651858.CD000400.pub4
http://www.ncbi.nlm.nih.gov/pubmed/31535715?tool=bestpractice.com
[100]Milsom I, Andersson K, Andersch B, et al. A comparison of flurbiprofen, tranexamic acid, and a levonorgestrel-releasing intrauterine contraceptive device in the treatment of idiopathic menorrhagia. Am J Obstet Gynecol. 1991 Mar;164(3):879-83.
https://www.doi.org/10.1016/s0002-9378(11)90533-x
http://www.ncbi.nlm.nih.gov/pubmed/1900665?tool=bestpractice.com
O ácido tranexâmico é um agente antifibrinolítico oral que reduz significativamente o sangramento menstrual em comparação com o placebo e pode reduzir a menorragia intensa em mulheres com miomas. Um estudo relatou uma taxa mais elevada de necrose em miomas em pacientes que receberam ácido tranexâmico em comparação com pacientes não tratadas.[101]Ip PP, Lam KW, Cheung CL, et al. Tranexamic acid-associated necrosis and intralesional thrombosis of uterine leiomyomas: a clinicopathologic study of 147 cases emphasizing the importance of drug-induced necrosis and early infarcts in leiomyomas. Am J Surg Pathol. 2007 Aug;31(8):1215-24.
http://www.ncbi.nlm.nih.gov/pubmed/17667546?tool=bestpractice.com
Os efeitos colaterais do tratamento com ácido tranexâmico incluem dor pélvica e febre, mas são necessários estudos mais qualificados para estabelecer a eficácia terapêutica do ácido tranexâmico em mulheres com miomas uterinos sintomáticos e definir melhor o papel do fármaco em relação ao tipo, tamanho e localização dos miomas.[102]Peitsidis P, Koukoulomati A. Tranexamic acid for the management of uterine fibroid tumors: a systematic review of the current evidence. World J Clin Cases. 2014 Dec 16;2(12):893-8.
https://www.wjgnet.com/2307-8960/full/v2/i12/893.htm
http://www.ncbi.nlm.nih.gov/pubmed/25516866?tool=bestpractice.com
Miomectomia para preservar a fertilidade
Existem também tratamentos cirúrgicos conservadores que permitem a preservação uterina.
O único procedimento cirúrgico que preserva a fertilidade e melhora eficazmente os sintomas relacionados a miomas é a miomectomia. Para mulheres com baixo desfecho reprodutivo prévio ou infertilidade nas quais o único achado seja cavidade uterina distorcida oriunda da presença de um ou mais miomas uterinos (mais comumente miomas submucosos), a miomectomia pode promover fertilidade e sucesso no desfecho de gravidez.
Para serem candidatas a miomectomia, as pacientes devem ter um ou mais dos seguintes sintomas:[72]Wallach EE, Vlahos NF. Uterine myomas: an overview of development, clinical features, and management. Obstet Gynecol. 2004 Aug;104(2):393-406.
http://www.ncbi.nlm.nih.gov/pubmed/15292018?tool=bestpractice.com
[103]Jin C, Hu Y, Chen XC, et al. Laparoscopic versus open myomectomy: a meta-analysis of randomized controlled trials. Eur J Obstet Gynecol Reprod Biol. 2009 Jul;145(1):14-21.
http://www.ncbi.nlm.nih.gov/pubmed/19398260?tool=bestpractice.com
Sangramento uterino excessivo que não responda a tratamentos conservadores
Infertilidade com distorção da cavidade endometrial ou obstrução tubária
Perda gestacional recorrente com distorção da cavidade endometrial
Sintomas de dor ou pressão que interfiram com a qualidade de vida
Sintomas do trato urinário (polaciúria e/ou sintomas de obstrução)
Anemia ferropriva secundária a sangramento crônico.
A via da miomectomia - abdominal, laparoscópica, robótica ou histeroscópica - depende em grande parte do tamanho, localização e quantidade de miomas. Os fatores de risco para recorrência de miomas uterinos incluem idade 30 a 40 anos e a presença de vários miomas; quanto mais miomas no momento da cirurgia, maior o risco de recorrência. As taxas de reintervenção de 5 anos para miomectomias abdominais, laparoscópicas e histeroscópicas em comparação com outras opções de tratamento de preservação uterina são 17%, 20% e 28%, respectivamente.[104]Davis MR, Soliman AM, Castelli-Haley J, et al. Reintervention Rates After Myomectomy, Endometrial Ablation, and Uterine Artery Embolization for Patients with Uterine Fibroids. J Womens Health (Larchmt). 2018 Oct;27(10):1204-1214.
https://www.doi.org/10.1089/jwh.2017.6752
http://www.ncbi.nlm.nih.gov/pubmed/30085898?tool=bestpractice.com
É importante reconhecer que a recorrência de miomas não indica recorrência dos sintomas nem a necessidade de reintervenção. Uma hemorragia significativa, como complicação da miomectomia, pode resultar em histerectomia de emergência em um pequeno número de casos.[105]Kongnyuy EJ, van den Broek N, Wiysonge CS. A systematic review of randomized controlled trials to reduce hemorrhage during myomectomy for uterine fibroids. Int J Gynaecol Obstet. 2008 Jan;100(1):4-9.
http://www.ncbi.nlm.nih.gov/pubmed/17894936?tool=bestpractice.com
[106]Iverson RE Jr, Chelmow D, Strohbehn K, et al. Relative morbidity of abdominal hysterectomy and myomectomy for management of uterine leiomyomas. Obstet Gynecol. 1996 Sep;88(3):415-9.
http://www.ncbi.nlm.nih.gov/pubmed/8752251?tool=bestpractice.com
Miomectomia por laparotomia: a miomectomia abdominal por laparotomia está associada a maior tempo de cirurgia e maior sangramento, quando comparada com a histerectomia, e está associada a 15% de taxa de recorrência de miomas uterinos. Dez por cento das mulheres submetidas a miomectomia por meio de incisão abdominal serão subsequentemente submetidas a histerectomia em 5 a 10 anos por sintomas persistentes.[107]Lefebvre G, VIlos G, Allaire C, et al. The management of uterine leiomyomas. J Obstet Gynaecol Can. 2003 May;25(5):396-418.
http://www.ncbi.nlm.nih.gov/pubmed/12738981?tool=bestpractice.com
Os riscos cirúrgicos normais são aplicáveis, incluindo sangramento, infecção, lesão a órgão contíguo e histerectomia não intencional. Foram relatados na literatura casos de ruptura uterina em gestações subsequentes a miomectomia. Algumas autoridades recomendam o manejo de pacientes com história de miomectomia como seria feito para candidatas a parto vaginal após parto cesáreo. As pacientes devem ser aconselhadas com respeito a esse baixo risco de ruptura uterina em gestações subsequentes após a miomectomia, independente da via de remoção.
Miomectomia por laparoscopia: a abordagem abdominal aberta foi a via mais comum utilizada para miomectomia. No entanto, com o advento de técnicas cirúrgicas minimamente invasivas, a miomectomia laparoscópica passou a ser mais amplamente realizada e aceita por muitos como a abordagem 'padrão-ouro 'para miomectomia.[108]Herrmann A, De Wilde R L. Laparoscopic myomectomy—the gold standard. Gynecol Minim Invasive Ther. 2014 May;3(2):31-8.
https://www.sciencedirect.com/science/article/pii/S2213307014000069
Essa cirurgia minimamente invasiva é realizada por meio de várias pequenas incisões abdominais. A seleção cuidadosa da paciente com base no tamanho, na localização e no número de miomas é importante para decidir se ela é candidata a miomectomia laparoscópica. Se a massa tiver entre 5 e 7 centímetros de diâmetro, a abordagem laparoscópica poderá ser mais apropriada e a recuperação será mais rápida que com a abordagem abdominal. No entanto, o risco de recorrência é maior, particularmente em casos com miomas múltiplos.[109]Ming X, Ran XT, Li N, et al. Risk of recurrence of uterine leiomyomas following laparoscopic myomectomy compared with open myomectomy. Arch Gynecol Obstet. 2020 Jan;301(1):235-42.
http://www.ncbi.nlm.nih.gov/pubmed/31781891?tool=bestpractice.com
[110]Kotani Y, Tobiume T, Fujishima R, et al. Recurrence of uterine myoma after myomectomy: open myomectomy versus laparoscopic myomectomy. J Obstet Gynaecol Res. 2018 Feb;44(2):298-302.
https://obgyn.onlinelibrary.wiley.com/doi/full/10.1111/jog.13519
http://www.ncbi.nlm.nih.gov/pubmed/29227004?tool=bestpractice.com
[Figure caption and citation for the preceding image starts]: Laparoscopia mostrando a presença de grande mioma subseroso posterolateral direito; observe a grande proximidade desse mioma uterino do ovário direito (potencial para erro de diagnóstico como massa anexial)Do acervo pessoal de Dr M.F. Mitwally and Dr R.J. Fischer; usado com permissão [Citation ends].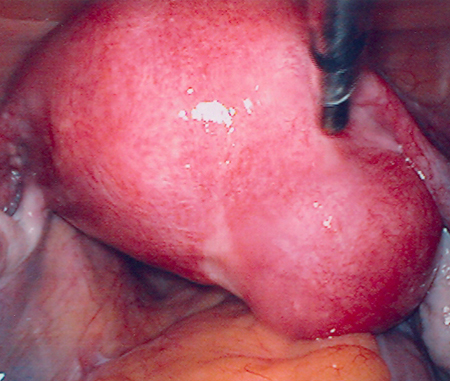
Miomectomia robótica: essa técnica foi desenvolvida para superar as dificuldades da miomectomia laparoscópica e ampliar o número pacientes candidatas à abordagem cirúrgica minimamente invasiva.[111]Laveaux SM, Advincula AP. Robot-assisted laparoscopic myomectomy (RALM). In: El-Ghobashy A, Ind T, Persson J, et al, eds. Textbook of gynecologic robotic surgery. Cham: Springer; 2018. A miomectomia laparoscópica pode ser realizada com assistência robótica. Vários estudos têm demonstrado a segurança, eficácia e viabilidade da miomectomia robótica.[112]Lonnerfors C. Robot-assisted myomectomy. Best Pract Res Clin Obstet Gynaecol. 2018 Jan;46:113-119.
https://www.doi.org/10.1016/j.bpobgyn.2017.09.005
http://www.ncbi.nlm.nih.gov/pubmed/29103894?tool=bestpractice.com
[113]Iavazzo C, Mamais I, Gkegkes ID. Robotic assisted vs laparoscopic and/or open myomectomy: systematic review and meta-analysis of the clinical evidence. Arch Gynecol Obstet. 2016 Jul;294(1):5-17.
http://www.ncbi.nlm.nih.gov/pubmed/26969650?tool=bestpractice.com
Tanto a miomectomia robótica quanto a miomectomia laparoscópica são opções cirúrgicas minimamente invasivas e associadas a menos sangramento, menos tempo de internação hospitalar, menos tempo de recuperação, menos complicações e custos mais altos que a laparotomia.[113]Iavazzo C, Mamais I, Gkegkes ID. Robotic assisted vs laparoscopic and/or open myomectomy: systematic review and meta-analysis of the clinical evidence. Arch Gynecol Obstet. 2016 Jul;294(1):5-17.
http://www.ncbi.nlm.nih.gov/pubmed/26969650?tool=bestpractice.com
[114]Behbehani S, Suarez-Salvador E, Buras M, et al. Mortality Rates in Benign Laparoscopic and Robotic Gynecologic Surgery: A Systematic Review and Meta-analysis. J Minim Invasive Gynecol. 2020 Mar - Apr;27(3):603-612.e1.
https://www.doi.org/10.1016/j.jmig.2019.10.005
http://www.ncbi.nlm.nih.gov/pubmed/31627007?tool=bestpractice.com
[115]Sheu BC, Huang KJ, Huang SC, et al. Comparison of uterine scarring between robot-assisted laparoscopic myomectomy and conventional laparoscopic myomectomy. J Obstet Gynaecol. 2020 Oct;40(7):974-980.
https://www.doi.org/10.1080/01443615.2019.1678015
http://www.ncbi.nlm.nih.gov/pubmed/31790613?tool=bestpractice.com
Os benefícios da miomectomia robótica e da miomectomia laparoscópica em comparação com a miomectomia abdominal aberta estão bem documentados. Além disso, não há diferença significativa nos desfechos das pacientes em comparação com a miomectomia laparoscópica. A seleção de candidatas à miomectomia robótica é feita de modo a garantir o sucesso do procedimento e minimizar o risco de conversão para outros procedimentos cirúrgicos.[116]Unger CA, Lachiewicz MP, Ridgeway B. Risk factors for robotic gynecologic procedures requiring conversion to other surgical procedures. Int J Gynaecol Obstet. 2016 Dec;135(3):299-303.
https://www.doi.org/10.1016/j.ijgo.2016.06.016
http://www.ncbi.nlm.nih.gov/pubmed/27591050?tool=bestpractice.com
[117]Dubuisson JB, Fauconnier A, Fourchotte V, et al. Laparoscopic myomectomy: predicting the risk of conversion to an open procedure. Hum Reprod. 2001 Aug;16(8):1726-31.
https://www.doi.org/10.1093/humrep/16.8.1726
http://www.ncbi.nlm.nih.gov/pubmed/11473973?tool=bestpractice.com
[118]American College of Obstetricians and Gynecologists. Committee opinion no. 810: robot-assisted surgery for noncancerous gynecologic conditions. Sep 2020 [internet publication].
https://www.acog.org/clinical/clinical-guidance/committee-opinion/articles/2020/09/robot-assisted-surgery-for-noncancerous-gynecologic-conditions
Para as miomectomias laparoscópica e robótica, a localização, o tamanho e o número de miomas, a compleição da paciente e o tamanho do útero relativo ao comprimento do tronco da paciente são fatores que devem ser considerados. A RNM pré-operatória é expressamente recomendada para mapeamento de miomas e para descartar a presença de adenomiose. A miomectomia robótica geralmente não é oferecida a pacientes com miomas >15 cm, um único mioma >15 cm ou se o útero estiver <5 dedos acima do umbigo.[111]Laveaux SM, Advincula AP. Robot-assisted laparoscopic myomectomy (RALM). In: El-Ghobashy A, Ind T, Persson J, et al, eds. Textbook of gynecologic robotic surgery. Cham: Springer; 2018.
Miomectomia por histeroscopia: a miomectomia histeroscópica é um procedimento minimamente invasivo que é o tratamento de primeira linha para miomas do tipo 0, 1 e 2 com intracavidades segundo a International Federation of Gynecology and Obstetrics (FIGO). A ultrassonografia e/ou a sono-histerografia pré-operatórias são obrigatórias para determinar a localização do mioma em relação à parede uterina e a extensão da protrusão para a cavidade uterina.[119]Fernandez H, Sefrioui O, Virelizier C, et al. Hysteroscopic resection of submucosal myomas in patients with infertility. Hum Reprod. 2001 Jul;16(7):1489-92.
http://www.ncbi.nlm.nih.gov/pubmed/11425835?tool=bestpractice.com
[120]Bajekal N, Li TC. Fibroids, infertility and pregnancy wastage. Hum Reprod Update. 2000 Nov-Dec;6(6):614-20.
http://www.ncbi.nlm.nih.gov/pubmed/11129696?tool=bestpractice.com
[121]Di Spiezio Sardo A, Mazzon I, Bramante S, et al. Hysteroscopic myomectomy: a comprehensive review of surgical techniques. Hum Reprod Update. 2008 Mar-Apr;14(2):101-19.
https://academic.oup.com/humupd/article/14/2/101/609051
http://www.ncbi.nlm.nih.gov/pubmed/18063608?tool=bestpractice.com
Para o sucesso da miomectomia histeroscópica, é preciso considerar o tamanho, o número e a localização dos miomas. Além disso, com lesões tipo 2, deve-se conhecer a relação do aspecto mais profundo dos miomas com a serosa uterina. As diretrizes recomendam que miomas até 4-5 cm sejam removidos por cirurgiões experientes para melhorar a chance de sucesso da ressecção.[122]American Association of Gynecologic Laparoscopists (AAGL): Advancing Minimally Invasive Gynecology Worldwide. AAGL practice report: practice guidelines for the diagnosis and management of submucous leiomyomas. J Minim Invasive Gynecol. 2012 Mar-Apr;19(2):152-71.
https://www.doi.org/10.1016/j.jmig.2011.09.005
http://www.ncbi.nlm.nih.gov/pubmed/22381967?tool=bestpractice.com
É importante salientar que os miomas do tipo 2 são mais propensos a necessitar de procedimentos em vários estágios em comparação com miomas do tipo 0 e 1. Se um mioma intracavitário atravessar o miométrio e se estender até a serosa uterina, a miomectomia histeroscópica será considerada insegura e não deverá ser realizada.
Independentemente da técnica utilizada para miomectomia histeroscópica (ressectoscópio ou morcelador), há evidências que sugerem que o risco de sobrecarga hídrica está diretamente relacionado à duração do procedimento, ao diâmetro do leiomioma e à proporção do mioma que está no miométrio.[123]Emanuel MH, Hart A, Wamsteker K, et al. An analysis of fluid loss during transcervical resection of submucous myomas. Fertil Steril. 1997 Nov;68(5):881-6.
https://www.doi.org/10.1016/s0015-0282(97)00335-x
http://www.ncbi.nlm.nih.gov/pubmed/9389820?tool=bestpractice.com
Outros riscos significativos, mas raros, da miomectomia histeroscópica incluem perfuração uterina, queimaduras elétricas nos órgãos genitais e intestino, bem como sangramento intenso, o que pode exigir uma histerectomia de emergência.[124]Royal College of Obstetricians and Gynaecologists (RCOG); British Society for Gynaecological Endoscopy. Best practice in outpatient hysteroscopy. Green-top guideline no. 59. Mar 2011 [internet publication].
https://www.rcog.org.uk/globalassets/documents/guidelines/gtg59hysteroscopy.pdf
Se a histeroscopia não for viável, pode-se considerar uma abordagem abdominal, laparoscópica ou robótica.
Embolização da artéria uterina
Pacientes com obesidade significativa, diabetes ou hipertensão e as com disfunção cardíaca ou pulmonar grave representam grupo de alto risco para cirurgia de grande porte e podem não ser candidatas para histerectomia.[48]American Congress of Obstetricians and Gynecologists. ACOG practice bulletin number 65: management of endometrial cancer. Obstet Gynecol. 2006 Apr;107(4):952.
http://www.ncbi.nlm.nih.gov/pubmed/16582139?tool=bestpractice.com
A embolização da artéria uterina (EAU) demonstrou proporcionar bom alívio em curto prazo de sintomas relacionados a volume e redução da menorragia associada a miomas uterinos. Seu impacto sobre a fertilidade futura e o desfecho de gestação futura, bem como eficácia em longo prazo, atualmente são desconhecidos e, portanto, o desejo de fertilidade futura é contraindicação relativa para esse procedimento.[125]American Congress of Obstetricians and Gynecologists. ACOG committee opinion: uterine artery embolization. Obstet Gynecol. 2004 Feb;103(2):403-4.
http://www.ncbi.nlm.nih.gov/pubmed/14754718?tool=bestpractice.com
No tratamento de sintomas relacionados a miomas, é similar à taxa de resposta observada após miomectomia (87.5% para EAU versus 93.3% para miomectomia). Contudo, há maior probabilidade de cirurgia de acompanhamento após EAU para miomas sintomáticos persistentes.
A EAU só deve ser considerada em mulheres que não desejem fertilidade futura. No entanto, é conhecido que gestações que ocorrem após a EAU apresentam desfechos obstétricos adversos significativos, em especial taxas de aborto espontâneo significativamente maiores, bem como outros eventos adversos, incluindo hemorragia pós-parto e aumento do risco de parto cesáreo.[126]Homer H, Saridogan E. Uterine artery embolization for fibroids is associated with an increased risk of miscarriage. Fertil Steril. 2010 Jun;94(1):324-30.
http://www.ncbi.nlm.nih.gov/pubmed/19361799?tool=bestpractice.com
[127]Carranza-Mamane B, Havelock J, Hemmings R, et al; Society of Obstetricians and Gynaecologists of Canada. The management of uterine fibroids in women with otherwise unexplained infertility. J Obstet Gynaecol Can. 2015 Mar;37(3):277-85.
https://www.jogc.com/article/S1701-2163(15)30318-2/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/26001875?tool=bestpractice.com
Portanto, é importante garantir que as mulheres estejam cientes disso e que contraceptivos sejam oferecidos, se necessário.
Comparada com a histerectomia e a miomectomia, a EAU está associada com redução na duração da internação e retorno mais rápido às atividades diárias normais. Além disso, uma revisão Cochrane constatou que a satisfação da paciente com o desfecho (em 2 anos de acompanhamento) é semelhante para a EAU, a histerectomia e a miomectomia. Embora tenha havido mais complicações leves (corrimento vaginal, hematoma pós-punção e síndrome pós-embolização) relacionadas à EAU, não houve diferenças significativas em complicações graves/em longo prazo entre a miomectomia e a EAU. No entanto, houve um aumento da probabilidade de necessidade de mais intervenção cirúrgica em 2 a 5 anos de EAU, e isso pode equilibrar qualquer vantagem de custo inicial da EAU.[128]Gupta JK, Sinha A, Lumsden MA, et al. Uterine artery embolization for symptomatic uterine fibroids. Cochrane Database Syst Rev. 2014 Dec 26;(12):CD005073.
http://cochranelibrary-wiley.com/doi/10.1002/14651858.CD005073.pub4/full
http://www.ncbi.nlm.nih.gov/pubmed/25541260?tool=bestpractice.com
[  ]
Is there RCT evidence to support the use of uterine artery embolization (UAE) in women with symptomatic uterine fibroids?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.2387/fullMostre-me a resposta
]
Is there RCT evidence to support the use of uterine artery embolization (UAE) in women with symptomatic uterine fibroids?/cca.html?targetUrl=https://www.cochranelibrary.com/cca/doi/10.1002/cca.2387/fullMostre-me a resposta
Faltam estudos sobre a EAU em longo prazo; no entanto, em 1 estudo comparando desfechos de EAU e miomectomia abdominal, a primeira resultou em taxa de 29% de terapia invasiva adicional durante os 3 a 5 anos de acompanhamento comparada com 3% no grupo da miomectomia.[73]Broder MS, Goodwin S, Chen G, et al. Comparison of long-term outcomes of myomectomy and uterine artery embolization. Obstet Gynecol. 2002 Nov;100(5 Pt 1):864-8.
http://www.ncbi.nlm.nih.gov/pubmed/12423842?tool=bestpractice.com
Os riscos desse procedimento incluem sangramento, infecção, reações alérgicas ao agente de contraste iodado, hematomas no local de punção da artéria femoral, oclusão incompleta da artéria uterina e embolização inadvertida de outros órgãos. A maioria das complicações da EAU tende a ocorrer mais de 30 dias após o procedimento. Complicações tardias incluem corrimento vaginal, expulsão de material fibroide e infecção.[129]Royal College of Obstetricians and Gynaecologists; Royal College of Radiologists. Clinical recommendations on the use of uterine artery embolisation (UAE) in the management of fibroids. Dec 2013 [internet publication].
https://www.rcog.org.uk/guidance/browse-all-guidance/other-guidelines-and-reports/uterine-artery-embolisation-in-the-management-of-fibroids
Além disso, tem havido uma crescente preocupação com o risco de embolização não intencional da circulação uterovariana, o que causa a redução do suprimento de sangue ovariano com subsequente comprometimento da reserva ovariana. No entanto, uma revisão sistemática mostrou que a EAU para miomas uterinos não parece afetar a reserva ovariana.[130]El Shamy T, Amer SAK, Mohamed AA, et al. The impact of uterine artery embolization on ovarian reserve: A systematic review and meta-analysis. Acta Obstet Gynecol Scand. 2020 Jan;99(1):16-23.
https://www.doi.org/10.1111/aogs.13698
http://www.ncbi.nlm.nih.gov/pubmed/31370100?tool=bestpractice.com
Histerectomia quando a fertilidade não for mais necessária
A histerectomia é o tratamento definitivo e mais comum para miomas uterinos sintomáticos, principalmente porque proporciona cura absoluta sem possibilidade de recorrência.[9]American College of Obstetricians and Gynecologists. ACOG practice bulletin no. 228: management of symptomatic uterine leiomyomas. Jun 2021 [internet publication].
https://www.acog.org/clinical/clinical-guidance/practice-bulletin/articles/2021/06/management-of-symptomatic-uterine-leiomyomas
É indicada em mulheres que não desejem preservar a fertilidade, que sejam boas candidatas à cirurgia e que tenham sido adequadamente aconselhadas quanto aos riscos e alternativas; a histerectomia está associada a alto nível de satisfação e eficácia.[107]Lefebvre G, VIlos G, Allaire C, et al. The management of uterine leiomyomas. J Obstet Gynaecol Can. 2003 May;25(5):396-418.
http://www.ncbi.nlm.nih.gov/pubmed/12738981?tool=bestpractice.com
Não há evidências de que a histerectomia interfira com a sexualidade ou o orgasmo durante o coito. Além dos riscos cirúrgicos normais, a histerectomia para miomas uterinos traz risco relativamente pequeno de dano ao trato urinário, intestino e vagina, bem como desenvolvimento tardio de prolapso da cúpula vaginal.[72]Wallach EE, Vlahos NF. Uterine myomas: an overview of development, clinical features, and management. Obstet Gynecol. 2004 Aug;104(2):393-406.
http://www.ncbi.nlm.nih.gov/pubmed/15292018?tool=bestpractice.com
Geralmente, há quatro abordagens cirúrgicas reconhecidas para histerectomia para doenças benignas do útero, como os leiomiomas uterinos.
Histerectomia abdominal: a abordagem abdominal envolve incisão relativamente grande através da parede abdominal.
Histerectomia vaginal: é realizada somente por meio de incisão na parte superior da vagina.
Histerectomia laparoscópica: esta técnica facilita a abordagem do útero por incisão vaginal (histerectomia vaginal assistida por laparoscopia) ou é completamente alcançada por meio de várias incisões pequenas (aproximadamente 1 cm) no abdome (histerectomia laparoscópica total).
Histerectomia robótica: semelhante à histerectomia vaginal e laparoscópica, esta abordagem é uma opção minimamente invasiva para histerectomia. A histerectomia robótica é completamente realizada por meio de uma série de pequenas incisões, como na histerectomia laparoscópica total.
A escolha da abordagem depende de inúmeros fatores, incluindo o tamanho e a mobilidade do útero, a experiência e a especialidade do cirurgião, e o estado clínico e a preferência da paciente. Foram identificadas inúmeras vantagens da histerectomia vaginal sobre a histerectomia abdominal, inclusive menor tempo de permanência hospitalar, retorno mais rápido às atividades normais e menos infecções inespecíficas ou episódios febris. Foram notadas vantagens similares para a histerectomia laparoscópica; no entanto, essa abordagem está associada a tempo de operação mais longo e mais lesões vesicais e ureterais quando comparada com a histerectomia abdominal. O uso da histerectomia com assistência robótica para condições ginecológicas benignas tem aumentado. No entanto, o papel da robótica na histerectomia benigna ainda não foi claramente definido.[118]American College of Obstetricians and Gynecologists. Committee opinion no. 810: robot-assisted surgery for noncancerous gynecologic conditions. Sep 2020 [internet publication].
https://www.acog.org/clinical/clinical-guidance/committee-opinion/articles/2020/09/robot-assisted-surgery-for-noncancerous-gynecologic-conditions
Em 2015, o American College of Obstetricians and Gynecologists (ACOG) reafirmou uma declaração, feita em 2009, endossando a abordagem vaginal como a via preferencial para histerectomia benigna por causa das menores taxas de complicações e vantagens bem documentadas.[131]American College of Obstetricians and Gynecologists. Committee opinion no. 628: robotic surgery in gynecology. Obstet Gynecol. 2015 Mar;125(3):760-7.
http://www.ncbi.nlm.nih.gov/pubmed/25730256?tool=bestpractice.com
[132]American College of Obstetricians and Gynecologists. ACOG Committee Opinion No. 444: choosing the route of hysterectomy for benign disease. Obstet Gynecol. 2009 Nov;114(5):1156-1158.
https://www.doi.org/10.1097/AOG.0b013e3181c33c72
http://www.ncbi.nlm.nih.gov/pubmed/20168127?tool=bestpractice.com
O ACOG e a American Association of Gynecologic Laparoscopists recomendam uma abordagem laparoscópica como abordagem alternativa quando a via vaginal não é viável.[133]AAGL Advancing Minimally Invasive Gynecology Worldwide. AAGL position statement: route of hysterectomy to treat benign uterine disease. J Minim Invasive Gynecol. 2011 Jan-Feb;18(1):1-3.
https://www.doi.org/10.1016/j.jmig.2010.10.001
http://www.ncbi.nlm.nih.gov/pubmed/21059487?tool=bestpractice.com
O principal objetivo dessas recomendações é evitar a morbidade da laparotomia, sempre que possível.
[  ]
In women with benign gynecological disease, how do different approaches to hysterectomy compare at improving outcomes?/cca.html?targetUrl=https://cochranelibrary.com/cca/doi/10.1002/cca.1225/fullMostre-me a resposta
]
In women with benign gynecological disease, how do different approaches to hysterectomy compare at improving outcomes?/cca.html?targetUrl=https://cochranelibrary.com/cca/doi/10.1002/cca.1225/fullMostre-me a resposta
A falta de clareza em relação à robótica se deve à escassez de evidências na literatura que comprovem seu papel na histerectomia pelas rotas laparoscópica e vaginal. Uma revisão da Cochrane de 2019 sobre cirurgia robótica em ginecologia concluiu, com relação à histerectomia benigna, que a eficácia e a segurança da robótica em comparação com a laparoscopia têm baixo grau da certeza, mas que as taxas de complicações cirúrgicas entre ambas as vias são comparáveis.[134]Lawrie TA, Liu H, Lu D, et al. Robot-assisted surgery in gynaecology. Cochrane Database Syst Rev. 2019 Apr 15;4:CD011422.
https://www.doi.org/10.1002/14651858.CD011422.pub2
http://www.ncbi.nlm.nih.gov/pubmed/30985921?tool=bestpractice.com
A maior duração da cirurgia e o custo da cirurgia robótica são dois pontos de grande controvérsia e debate. Em relação à duração da cirurgia, estudos comparativos entre a abordagem robótica e a laparoscópica geralmente mostram que a duração da cirurgia é equivalente ou maior na abordagem robótica. Fora isso, não há diferenças clínicas ou estatisticamente significativas entre ambas as abordagens.[135]Martínez-Maestre MA, Gambadauro P, González-Cejudo C, et al. Total laparoscopic hysterectomy with and without robotic assistance: a prospective controlled study. Surg Innov. 2014 Jun;21(3):250-5.
https://www.doi.org/10.1177/1553350613492023
http://www.ncbi.nlm.nih.gov/pubmed/23833240?tool=bestpractice.com
[136]Paraiso MF, Ridgeway B, Park AJ, et al. A randomized trial comparing conventional and robotically assisted total laparoscopic hysterectomy. Am J Obstet Gynecol. 2013 May;208(5):368.e1-7.
https://www.doi.org/10.1016/j.ajog.2013.02.008
http://www.ncbi.nlm.nih.gov/pubmed/23395927?tool=bestpractice.com
[137]Sarlos D, Kots L, Stevanovic N, et al. Robotic compared with conventional laparoscopic hysterectomy: a randomized controlled trial. Obstet Gynecol. 2012 Sep;120(3):604-11.
https://www.doi.org/10.1097/AOG.0b013e318265b61a
http://www.ncbi.nlm.nih.gov/pubmed/22914470?tool=bestpractice.com
Estudos comparativos entre os custos da histerectomia cirúrgica minimamente invasiva - robótica versus laparoscópica versus vaginal - mostram resultados mistos.[138]Swenson CW, Kamdar NS, Harris JA, et al. Comparison of robotic and other minimally invasive routes of hysterectomy for benign indications. Am J Obstet Gynecol. 2016 Nov;215(5):650.e1-650.e8.
https://www.doi.org/10.1016/j.ajog.2016.06.027
http://www.ncbi.nlm.nih.gov/pubmed/27343568?tool=bestpractice.com
[139]Lönnerfors C, Reynisson P, Persson J. A randomized trial comparing vaginal and laparoscopic hysterectomy vs robot-assisted hysterectomy. J Minim Invasive Gynecol. 2015 Jan;22(1):78-86.
https://www.doi.org/10.1016/j.jmig.2014.07.010
http://www.ncbi.nlm.nih.gov/pubmed/25045857?tool=bestpractice.com
Na tentativa de lidar com essas questões de custo, estão sendo implementadas estratégias por cirurgiões robóticos para maximizar a custo-efetividade da cirurgia robótica, inclusive minimizar o número de vias de acesso e instrumentos robóticos usados por caso, treinamento de equipes robóticas especiais para melhorar a eficiência do fluxo de trabalho e reduzir a duração da cirurgia.[140]Bogliolo S, Ferrero S, Cassani C, et al. Single-site Versus Multiport Robotic Hysterectomy in Benign Gynecologic Diseases: A Retrospective Evaluation of Surgical Outcomes and Cost Analysis. J Minim Invasive Gynecol. 2016 May-Jun;23(4):603-9.
https://www.doi.org/10.1016/j.jmig.2016.02.006
http://www.ncbi.nlm.nih.gov/pubmed/26898895?tool=bestpractice.com
 ]
Pode causar elevações transitórias nas transaminases.[90][91]
]
Pode causar elevações transitórias nas transaminases.[90][91]
 ]
]
 ]
]