O diagnóstico de SMD requer uma história médica e exame físico detalhados, e avaliação patológica do sangue periférico e da medula óssea.
A SMD é uma doença heterogênea com apresentações variadas. Normalmente, os pacientes estão assintomáticos à apresentação, e a suspeita de SMD é levantada após um exame de sangue que mostre citopenia (mais comumente, anemia).[47]Garcia-Manero G. Myelodysplastic syndromes: 2023 update on diagnosis, risk-stratification, and management. Am J Hematol. 2023 Aug;98(8):1307-25.
https://www.doi.org/10.1002/ajh.26984
http://www.ncbi.nlm.nih.gov/pubmed/37288607?tool=bestpractice.com
Alguns pacientes apresentam sintomas relacionados com a citopenia (por exemplo, fadiga, infecções, hematomas).
Anamnese e exame físico
A idade mediana ao diagnóstico é de 70-75 anos de idade, mas a doença pode ocorrer em qualquer idade e deve ser considerada em pacientes mais jovens que tiverem tido exposição prévia a quimioterapia ou radioterapia, ou que tiverem uma doença congênita (por exemplo, síndrome de Fanconi, síndrome de Bloom, síndrome de Down).[9]Sekeres MA, Taylor J. Diagnosis and treatment of myelodysplastic syndromes: a review. JAMA. 2022 Sep 6;328(9):872-80.
http://www.ncbi.nlm.nih.gov/pubmed/36066514?tool=bestpractice.com
[10]Roman E, Smith A, Appleton S, et al. Myeloid malignancies in the real-world: occurrence, progression and survival in the UK's population-based Haematological Malignancy Research Network 2004-15. Cancer Epidemiol. 2016 Jun;42:186-98.
https://www.sciencedirect.com/science/article/pii/S1877782116300364
http://www.ncbi.nlm.nih.gov/pubmed/27090942?tool=bestpractice.com
[15]National Comprehensive Cancer Network. NCCN clinical practice guidelines in oncology: myelodysplastic syndromes [internet publication].
https://www.nccn.org/guidelines/category_1
[16]Fenaux P, Haase D, Santini V, et al; ESMO Guidelines Committee. Myelodysplastic syndromes: ESMO clinical practice guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2021 Feb;32(2):142-56.
https://www.annalsofoncology.org/article/S0923-7534(20)43129-1/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/33221366?tool=bestpractice.com
[18]Sperling AS, Gibson CJ, Ebert BL. The genetics of myelodysplastic syndrome: from clonal haematopoiesis to secondary leukaemia. Nat Rev Cancer. 2017 Jan;17(1):5-19.
http://www.ncbi.nlm.nih.gov/pubmed/27834397?tool=bestpractice.com
[26]Oetjen KA, Levoska MA, Tamura D, et al. Predisposition to hematologic malignancies in patients with xeroderma pigmentosum. Haematologica. 2020 Apr;105(4):e144-6.
https://www.doi.org/10.3324/haematol.2019.223370
http://www.ncbi.nlm.nih.gov/pubmed/31439674?tool=bestpractice.com
[27]Aktas D, Koc A, Boduroglu K, et al. Myelodysplastic syndrome associated with monosomy 7 in a child with Bloom syndrome. Cancer Genet Cytogenet. 2000 Jan;116(1):44-6.
http://www.ncbi.nlm.nih.gov/pubmed/10616531?tool=bestpractice.com
[36]Sill H, Olipitz W, Zebisch A, et al. Therapy-related myeloid neoplasms: pathobiology and clinical characteristics. Br J Pharmacol. 2011 Feb;162(4):792-805.
https://bpspubs.onlinelibrary.wiley.com/doi/10.1111/j.1476-5381.2010.01100.x
http://www.ncbi.nlm.nih.gov/pubmed/21039422?tool=bestpractice.com
[37]Kaplan H, Malmgren J, De Roos AJ. Risk of myelodysplastic syndrome and acute myeloid leukemia post radiation treatment for breast cancer: a population-based study. Breast Cancer Res Treat. 2013 Feb;137(3):863-7.
http://www.ncbi.nlm.nih.gov/pubmed/23274844?tool=bestpractice.com
[48]Sallman DA, Padron E. Myelodysplasia in younger adults: outlier or unique molecular entity? Haematologica. 2017 Jun;102(6):967-8.
https://www.doi.org/10.3324/haematol.2017.165993
http://www.ncbi.nlm.nih.gov/pubmed/28566339?tool=bestpractice.com
[49]Hirsch CM, Przychodzen BP, Radivoyevitch T, et al. Molecular features of early onset adult myelodysplastic syndrome. Haematologica. 2017 Jun;102(6):1028-34.
https://www.doi.org/10.3324/haematol.2016.159772
http://www.ncbi.nlm.nih.gov/pubmed/28255022?tool=bestpractice.com
A anamnese deve incluir uma avaliação detalhada de exposições prévias a quimioterapia e/ou radioterapia; infecções ou episódios de sangramento prévios; presença de comorbidades; história familiar de doenças hematológicas; estado nutricional (deficiências nutricionais); uso de bebidas alcoólicas; e exposição a produtos químicos tóxicos.[11]Killick SB, Wiseman DH, Quek L, et al. British Society for Haematology guidelines for the diagnosis and evaluation of prognosis of adult myelodysplastic syndromes. Br J Haematol. 2021 Jul;194(2):282-93.
https://onlinelibrary.wiley.com/doi/10.1111/bjh.17621
http://www.ncbi.nlm.nih.gov/pubmed/34137023?tool=bestpractice.com
[15]National Comprehensive Cancer Network. NCCN clinical practice guidelines in oncology: myelodysplastic syndromes [internet publication].
https://www.nccn.org/guidelines/category_1
Um exame físico detalhado é necessário, pois pode identificar sinais e sintomas relacionados a citopenias, como palidez, fadiga, intolerância a exercícios, infecções (geralmente bacterianas), hematomas e sangramentos (petéquias, púrpura).
Doenças autoimunes (por exemplo, vasculite, doença do tecido conjuntivo, artrite inflamatória) são relatadas em aproximadamente 25% dos pacientes com SMD.[6]Wolach O, Stone R. Autoimmunity and inflammation in myelodysplastic syndromes. Acta Haematol. 2016;136(2):108-17.
https://www.doi.org/10.1159/000446062
http://www.ncbi.nlm.nih.gov/pubmed/27337745?tool=bestpractice.com
[7]Komrokji RS, Kulasekararaj A, Al Ali NH, et al. Autoimmune diseases and myelodysplastic syndromes. Am J Hematol. 2016 May;91(5):E280-3.
https://www.doi.org/10.1002/ajh.24333
http://www.ncbi.nlm.nih.gov/pubmed/26875020?tool=bestpractice.com
[8]Enright H, Jacobs HS, Vercellotti G, et al. Paraneoplastic autoimmune phenomena in patients with myelodysplastic syndromes: response to immunosuppressive therapy. Br J Haematol. 1995 Oct;91(2):403-8.
http://www.ncbi.nlm.nih.gov/pubmed/8547082?tool=bestpractice.com
A esplenomegalia, a hepatomegalia e a 'linfadenopatia raramente ocorrem na SMD. Elas podem ocorrer na leucemia mielomonocítica crônica (LMC), uma neoplasia mieloide com características patológicas e moleculares que se sobrepõem à SMD.[1]Khoury JD, Solary E, Abla O, et al. The 5th edition of the World Health Organization classification of haematolymphoid tumours: myeloid and histiocytic/dendritic neoplasms. Leukemia. 2022 Jul;36(7):1703-19.
https://www.doi.org/10.1038/s41375-022-01613-1
http://www.ncbi.nlm.nih.gov/pubmed/35732831?tool=bestpractice.com
Exames iniciais
Os exames iniciais devem ser um hemograma completo com diferencial e um esfregaço de sangue periférico. O hemograma completo mostrará uma ou mais citopenias (mais comumente, anemia) que são sustentadas (por exemplo, >4 meses).[11]Killick SB, Wiseman DH, Quek L, et al. British Society for Haematology guidelines for the diagnosis and evaluation of prognosis of adult myelodysplastic syndromes. Br J Haematol. 2021 Jul;194(2):282-93.
https://onlinelibrary.wiley.com/doi/10.1111/bjh.17621
http://www.ncbi.nlm.nih.gov/pubmed/34137023?tool=bestpractice.com
[15]National Comprehensive Cancer Network. NCCN clinical practice guidelines in oncology: myelodysplastic syndromes [internet publication].
https://www.nccn.org/guidelines/category_1
[16]Fenaux P, Haase D, Santini V, et al; ESMO Guidelines Committee. Myelodysplastic syndromes: ESMO clinical practice guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2021 Feb;32(2):142-56.
https://www.annalsofoncology.org/article/S0923-7534(20)43129-1/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/33221366?tool=bestpractice.com
O esfregaço de sangue periférico mostrará citopenias e displasia (por exemplo, granulócitos hipolobulados e hipogranulares [pseudoanomalia de Pelger-Huet]).[16]Fenaux P, Haase D, Santini V, et al; ESMO Guidelines Committee. Myelodysplastic syndromes: ESMO clinical practice guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2021 Feb;32(2):142-56.
https://www.annalsofoncology.org/article/S0923-7534(20)43129-1/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/33221366?tool=bestpractice.com
Os exames laboratoriais adicionais incluem contagem de reticulócitos, folato eritrocitário, vitamina B12 sérica e perfil de ferro (ferro sérico, capacidade total de ligação do ferro, ferritina).[11]Killick SB, Wiseman DH, Quek L, et al. British Society for Haematology guidelines for the diagnosis and evaluation of prognosis of adult myelodysplastic syndromes. Br J Haematol. 2021 Jul;194(2):282-93.
https://onlinelibrary.wiley.com/doi/10.1111/bjh.17621
http://www.ncbi.nlm.nih.gov/pubmed/34137023?tool=bestpractice.com
[15]National Comprehensive Cancer Network. NCCN clinical practice guidelines in oncology: myelodysplastic syndromes [internet publication].
https://www.nccn.org/guidelines/category_1
[16]Fenaux P, Haase D, Santini V, et al; ESMO Guidelines Committee. Myelodysplastic syndromes: ESMO clinical practice guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2021 Feb;32(2):142-56.
https://www.annalsofoncology.org/article/S0923-7534(20)43129-1/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/33221366?tool=bestpractice.com
Devem ser realizados para descartar outras causas de citopenias. A contagem de reticulócitos normalmente está baixa na SMD.[50]Juneja SK, Imbert M, Jouault H, et al. Haematological features of primary myelodysplastic syndromes (PMDS) at initial presentation: a study of 118 cases. J Clin Pathol. 1983 Oct;36(10):1129-35.
https://jcp.bmj.com/content/jclinpath/36/10/1129.full.pdf
http://www.ncbi.nlm.nih.gov/pubmed/6619310?tool=bestpractice.com
Testes para infecções virais (por exemplo, HIV, hepatite B, C e E; citomegalovírus; parvovírus) podem ser realizados se houver fatores de risco para exposições prévias.[11]Killick SB, Wiseman DH, Quek L, et al. British Society for Haematology guidelines for the diagnosis and evaluation of prognosis of adult myelodysplastic syndromes. Br J Haematol. 2021 Jul;194(2):282-93.
https://onlinelibrary.wiley.com/doi/10.1111/bjh.17621
http://www.ncbi.nlm.nih.gov/pubmed/34137023?tool=bestpractice.com
[15]National Comprehensive Cancer Network. NCCN clinical practice guidelines in oncology: myelodysplastic syndromes [internet publication].
https://www.nccn.org/guidelines/category_1
[16]Fenaux P, Haase D, Santini V, et al; ESMO Guidelines Committee. Myelodysplastic syndromes: ESMO clinical practice guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2021 Feb;32(2):142-56.
https://www.annalsofoncology.org/article/S0923-7534(20)43129-1/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/33221366?tool=bestpractice.com
A infecção por HIV pode causar alterações displásicas na medula óssea similares àquelas observadas na SMD.[51]Katsarou O, Terpos E, Patsouris E, et al. Myelodysplastic features in patients with long-term HIV infection and haemophilia. Haemophilia. 2001 Jan;7(1):47-52.
https://onlinelibrary.wiley.com/doi/abs/10.1111/j.1365-2516.2001.00445.x?sid=nlm%3Apubmed
http://www.ncbi.nlm.nih.gov/pubmed/11136381?tool=bestpractice.com
[Figure caption and citation for the preceding image starts]: Esfregaço que mostra neutrófilos normais (direita) e neutrófilos displásicos com citoplasma agranular e núcleo hipolobuladoImagem usada com permissão do BMJ 1997;314:883 [Citation ends].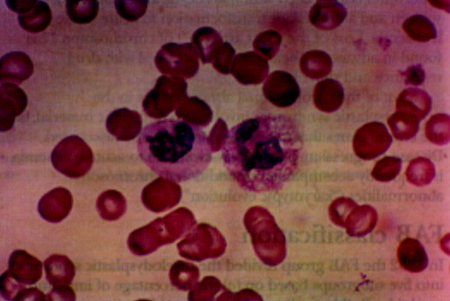
Avaliação da medula óssea
A aspiração da medula óssea (com coloração para ferro) e a punção por agulha grossa (core biopsy) são necessárias para análises morfológicas, citogenéticas, mutacionais e por citometria de fluxo.[15]National Comprehensive Cancer Network. NCCN clinical practice guidelines in oncology: myelodysplastic syndromes [internet publication].
https://www.nccn.org/guidelines/category_1
[47]Garcia-Manero G. Myelodysplastic syndromes: 2023 update on diagnosis, risk-stratification, and management. Am J Hematol. 2023 Aug;98(8):1307-25.
https://www.doi.org/10.1002/ajh.26984
http://www.ncbi.nlm.nih.gov/pubmed/37288607?tool=bestpractice.com
Essas investigações confirmam o diagnóstico de SMD e orientam a estratificação de risco e o tratamento.[15]National Comprehensive Cancer Network. NCCN clinical practice guidelines in oncology: myelodysplastic syndromes [internet publication].
https://www.nccn.org/guidelines/category_1
[47]Garcia-Manero G. Myelodysplastic syndromes: 2023 update on diagnosis, risk-stratification, and management. Am J Hematol. 2023 Aug;98(8):1307-25.
https://www.doi.org/10.1002/ajh.26984
http://www.ncbi.nlm.nih.gov/pubmed/37288607?tool=bestpractice.com
[52]van de Loosdrecht AA, Kern W, Porwit A, et al. Clinical application of flow cytometry in patients with unexplained cytopenia and suspected myelodysplastic syndrome: a report of the European LeukemiaNet International MDS-Flow Cytometry Working Group. Cytometry B Clin Cytom. 2023 Jan;104(1):77-86.
https://onlinelibrary.wiley.com/doi/10.1002/cyto.b.22044
http://www.ncbi.nlm.nih.gov/pubmed/34897979?tool=bestpractice.com
O diagnóstico de SMD pode ser feito em um paciente com citopenia persistente, na presença de um dos três critérios a seguir: displasia de medula óssea significativa (≥10% em uma ou mais das três principais linhagens da medula óssea); blastos no sangue periférico e/ou medula óssea (<20%); ou anormalidade citogenética clonal ou mutação somática.[1]Khoury JD, Solary E, Abla O, et al. The 5th edition of the World Health Organization classification of haematolymphoid tumours: myeloid and histiocytic/dendritic neoplasms. Leukemia. 2022 Jul;36(7):1703-19.
https://www.doi.org/10.1038/s41375-022-01613-1
http://www.ncbi.nlm.nih.gov/pubmed/35732831?tool=bestpractice.com
[2]Arber DA, Orazi A, Hasserjian RP, et al. International Consensus Classification of myeloid neoplasms and acute leukemias: integrating morphologic, clinical, and genomic data. Blood. 2022 Sep 15;140(11):1200-28.
https://www.doi.org/10.1182/blood.2022015850
http://www.ncbi.nlm.nih.gov/pubmed/35767897?tool=bestpractice.com
[11]Killick SB, Wiseman DH, Quek L, et al. British Society for Haematology guidelines for the diagnosis and evaluation of prognosis of adult myelodysplastic syndromes. Br J Haematol. 2021 Jul;194(2):282-93.
https://onlinelibrary.wiley.com/doi/10.1111/bjh.17621
http://www.ncbi.nlm.nih.gov/pubmed/34137023?tool=bestpractice.com
As características biológicas são mais importantes que o valor de corte rigoroso de blastos.[15]National Comprehensive Cancer Network. NCCN clinical practice guidelines in oncology: myelodysplastic syndromes [internet publication].
https://www.nccn.org/guidelines/category_1
Os pacientes com blastos ≥20% devem ser avaliados quanto a leucemia mieloide aguda. Consulte Leucemia mieloide aguda.
[Figure caption and citation for the preceding image starts]: Grandes megacariócitos mononucleares na medula óssea de paciente com SMD-del(5q)Imagem usada com permissão do BMJ 1997;314:883 [Citation ends].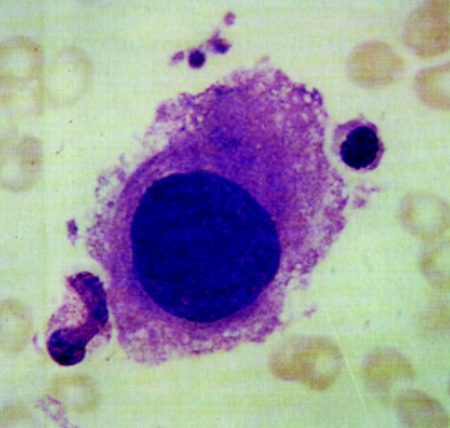
Teste genético
Os testes genéticos para anormalidades citogenéticas associadas à SMD (por exemplo, -5, del(5q), -7, del(7q), del(11q), del(12p), -17, del(17p), del(20q)) e mutações somáticas (por exemplo, DNMT3A, TET2, ASXL1, TP53, SF3B1) fundamentam o diagnóstico e a estratificação de risco prognóstica.[11]Killick SB, Wiseman DH, Quek L, et al. British Society for Haematology guidelines for the diagnosis and evaluation of prognosis of adult myelodysplastic syndromes. Br J Haematol. 2021 Jul;194(2):282-93.
https://onlinelibrary.wiley.com/doi/10.1111/bjh.17621
http://www.ncbi.nlm.nih.gov/pubmed/34137023?tool=bestpractice.com
[15]National Comprehensive Cancer Network. NCCN clinical practice guidelines in oncology: myelodysplastic syndromes [internet publication].
https://www.nccn.org/guidelines/category_1
A presença de certas anormalidades citogenéticas ou mutações somáticas (por exemplo, -7/del(7q), del(5q) e SF3B1) pode estabelecer um diagnóstico sem displasia.[1]Khoury JD, Solary E, Abla O, et al. The 5th edition of the World Health Organization classification of haematolymphoid tumours: myeloid and histiocytic/dendritic neoplasms. Leukemia. 2022 Jul;36(7):1703-19.
https://www.doi.org/10.1038/s41375-022-01613-1
http://www.ncbi.nlm.nih.gov/pubmed/35732831?tool=bestpractice.com
[2]Arber DA, Orazi A, Hasserjian RP, et al. International Consensus Classification of myeloid neoplasms and acute leukemias: integrating morphologic, clinical, and genomic data. Blood. 2022 Sep 15;140(11):1200-28.
https://www.doi.org/10.1182/blood.2022015850
http://www.ncbi.nlm.nih.gov/pubmed/35767897?tool=bestpractice.com
Os testes genéticos podem ser realizados no sangue periférico, se a testagem da medula óssea não for possível.
Os pacientes com displasia significativa que não têm anormalidade citogenética clonal ou mutação somática devem ser submetidos a avaliações adicionais para descartar uma causa não maligna de displasia.
Exames subsequentes
Quando o diagnóstico for estabelecido, os seguintes exames adicionais podem ser úteis em determinadas situações.
Níveis de eritropoetina sérica: podem ser medidos para orientar o tratamento com agentes estimuladores da eritropoese.[15]National Comprehensive Cancer Network. NCCN clinical practice guidelines in oncology: myelodysplastic syndromes [internet publication].
https://www.nccn.org/guidelines/category_1
[16]Fenaux P, Haase D, Santini V, et al; ESMO Guidelines Committee. Myelodysplastic syndromes: ESMO clinical practice guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2021 Feb;32(2):142-56.
https://www.annalsofoncology.org/article/S0923-7534(20)43129-1/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/33221366?tool=bestpractice.com
[53]de Witte T, Bowen D, Robin M, et al. Allogeneic hematopoietic stem cell transplantation for MDS and CMML: recommendations from an international expert panel. Blood. 2017 Mar 30;129(13):1753-62.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5524528
http://www.ncbi.nlm.nih.gov/pubmed/28096091?tool=bestpractice.com
Geralmente a eritropoetina sérica está elevada na SMD, exceto na insuficiência renal concomitante, em cujo caso ela estará baixa.
Lactato desidrogenase: tem valor prognóstico e pode ser medida para fundamentar a estratificação de risco e o tratamento.[15]National Comprehensive Cancer Network. NCCN clinical practice guidelines in oncology: myelodysplastic syndromes [internet publication].
https://www.nccn.org/guidelines/category_1
[16]Fenaux P, Haase D, Santini V, et al; ESMO Guidelines Committee. Myelodysplastic syndromes: ESMO clinical practice guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2021 Feb;32(2):142-56.
https://www.annalsofoncology.org/article/S0923-7534(20)43129-1/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/33221366?tool=bestpractice.com
A lactato desidrogenase elevada está associada a desfechos desfavoráveis.[54]Wimazal F, Sperr WR, Kundi M, et al. Prognostic value of lactate dehydrogenase activity in myelodysplastic syndromes. Leuk Res. 2001 Apr;25(4):287-94.
https://www.doi.org/10.1016/s0145-2126(00)00140-5
http://www.ncbi.nlm.nih.gov/pubmed/11248325?tool=bestpractice.com
[55]Germing U, Hildebrandt B, Pfeilstöcker M, et al. Refinement of the international prognostic scoring system (IPSS) by including LDH as an additional prognostic variable to improve risk assessment in patients with primary myelodysplastic syndromes (MDS). Leukemia. 2005 Dec;19(12):2223-31.
http://www.ncbi.nlm.nih.gov/pubmed/16193087?tool=bestpractice.com
Tipagem de antígeno leucocitário humano (HLA): é útil se o paciente for um candidato a transplante de células-tronco hematopoiéticas, ou se transfusões extensas de plaquetas forem necessárias ou previstas.[53]de Witte T, Bowen D, Robin M, et al. Allogeneic hematopoietic stem cell transplantation for MDS and CMML: recommendations from an international expert panel. Blood. 2017 Mar 30;129(13):1753-62.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5524528
http://www.ncbi.nlm.nih.gov/pubmed/28096091?tool=bestpractice.com
Citometria de fluxo: pode contribuir para o diagnóstico (ao identificar características displásicas e blastos) e para prognóstico. Pode ser usada (em conjunto com o teste para a mutação STAT3) para a avaliação de um clone de hemoglobinúria paroxística noturna concomitante, e possível leucemia linfocítica granular grande.[3]Steensma DP, Bennett JM. The myelodysplastic syndromes: diagnosis and treatment. Mayo Clin Proc. 2006 Jan;81(1):104-30.
http://www.ncbi.nlm.nih.gov/pubmed/16438486?tool=bestpractice.com
[15]National Comprehensive Cancer Network. NCCN clinical practice guidelines in oncology: myelodysplastic syndromes [internet publication].
https://www.nccn.org/guidelines/category_1

