Anamnesis y examen
Principales factores de diagnóstico
común
presencia de factores de riesgo
Los fuertes factores de riesgo incluyen tumores cerebrales, irradiación craneal, síndrome de McCune-Albright, hiperplasia suprarrenal congénita y tumores gonadales secretores de esteroides sexuales.
chicos: testículos ≥4 mL
El tamaño testicular se documenta a través de la medición del eje más largo o por el volumen testicular utilizando el orquidómetro de Prader. Un volumen de ≥4 ml, o una longitud de 2.5 cm, define el inicio de la pubertad.[2]
[Figure caption and citation for the preceding image starts]: Orquidómetro de PraderCreado por BMJ Knowledge Centre [Citation ends]. [Figure caption and citation for the preceding image starts]: Método para comparar el tamaño testicular utilizando el orquidómetro de PraderDe la colección del Dr. A. Mehta [Citation ends].
[Figure caption and citation for the preceding image starts]: Método para comparar el tamaño testicular utilizando el orquidómetro de PraderDe la colección del Dr. A. Mehta [Citation ends].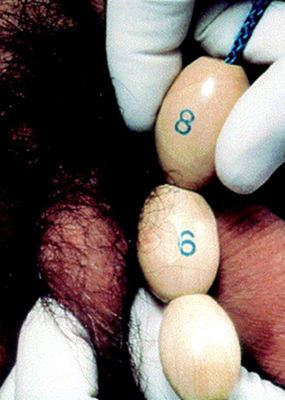
niñas: desarrollo mamario
El primer signo demostrable de pubertad en las niñas es el desarrollo mamario.[1]
vello púbico/axilar
En las mujeres, el vello púbico y axilar, el acné y el olor corporal se desarrollan como resultado de andrógenos secretados por las glándulas suprarrenales, y en parte por los ovarios. El inicio del vello axilar ocurre generalmente en la etapa media de la pubertad.
El vello púbico o axilar en ausencia de desarrollo mamario en las niñas o el agrandamiento testicular en los niños es típico en la adrenarquia precoz o prematura, y con escasa frecuencia puede ser un signo de hiperplasia suprarrenal congénita, tumores de las glándulas suprarrenales o de síndrome de Cushing.
menarquia
La menarquia se utiliza como evidencia documentada y bien definida de pubertad en niñas. Suele aparecer en el estadio 4 de la pubertad en la mayoría de las niñas normales, entre 2 y 3 años después del inicio del desarrollo mamario.
velocidad de crecimiento aumentada
Los estrógenos, ya sean ováricos o aromatizados de la testosterona testicular, son el factor que media la respuesta aumentada a la hormona del crecimiento (GH) durante la pubertad.[41][42] La secreción prematura de esteroides gonadales en niños es la causa de la situación paradójica de una estatura alta durante la infancia, debido a una tasa acelerada de crecimiento lineal y una eventual estatura baja en la edad adulta debido a la fusión temprana de las placas de crecimiento epifisarias.
La velocidad de crecimiento aumenta entre mediados y finales de la pubertad en los niños y entre principios y mediados de la pubertad en las niñas.
Por término medio, la pubertad contribuye a aumentar 25 cm la estatura de las mujeres y 30 cm la de los hombres.
estatura alta
La secreción prematura de esteroides gonadales en niños es la causa de la situación paradójica de una estatura alta durante la infancia, debido a una tasa acelerada de crecimiento lineal y una eventual estatura baja en la edad adulta debido a la fusión temprana de las placas de crecimiento epifisarias.
Otros factores de diagnóstico
infrecuente
manchas color café con leche
El examen de la piel debe ayudar a identificar las manchas café con leche presentes en la neurofibromatosis tipo 1 (NF1), que presentan bordes regulares, y en el síndrome de McCune-Albright (MAS), que suele tener bordes irregulares.
La NF1 (con un alto riesgo de gliomas ópticos) presenta una pubertad precoz central; el SMA da lugar a una pubertad precoz independiente de las gonadotropinas.[Figure caption and citation for the preceding image starts]: Niña con pubertad precoz independiente de gonadotropinas (PPGI) y máculas hiperpigmentadas de color café como parte del síndrome de McCune-Albright (SMA)De la colección del Dr. A. Mehta; usado con autorización [Citation ends].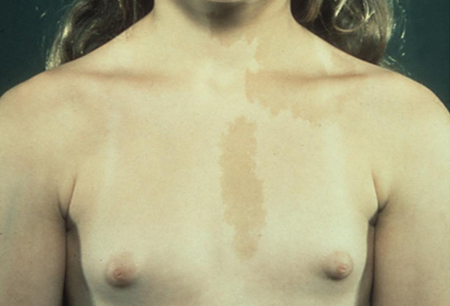
síntomas de otra hiperfunción endocrina autónoma
Sugiere el síndrome de McCune-Albright (SMA). Los síntomas de otras afectaciones endocrinas incluyen tirotoxicosis (hiperplasia nodular tiroidea), síndrome de Cushing (nódulos hiperplásicos suprarrenales múltiples), gigantismo o acromegalia (adenoma hipofisario y exceso de hormona del crecimiento (GH)) y galactorrea (debido a hiperprolactinemia).
displasia fibrosa poliostótica
Componente del síndrome de McCune-Albright; enfermedad ósea de progresión lenta que puede afectar cualquier hueso, se presenta frecuentemente con asimetría facial e hiperostosis de la base del cráneo.
neurofibromas, pecas axilares y cifoescoliosis
Los neurofibromas plexiformes, las pecas axilares, la cifoescoliosis y los antecedentes familiares positivos son indicativos de neurofibromatosis tipo 1 causante de pubertad precoz central.[Figure caption and citation for the preceding image starts]: Pecas axilares en neurofibromatosis tipo 1De la colección del Dr. A. Mehta; usado con autorización [Citation ends].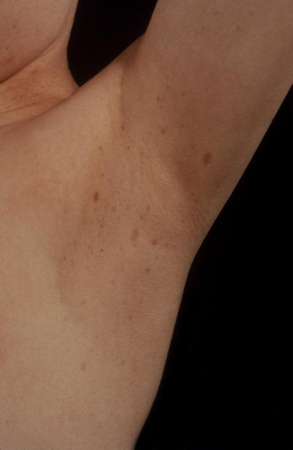
dismorfia facial
La presencia de rasgos dismórficos puede revelar síndromes multisistémicos, como anormalidades faciales de la línea media en holoprosencefalia y en displasia septoóptica. Se puede observar asimetría facial en el síndrome de McCune-Albright.
clitoromegalia
Sugiere una hiperplasia suprarrenal congénita o un tumor virilizante suprarrenal u ovárico, como etiología subyacente que provoca una pubertad precoz gonadotropina-independiente (PPGI) en mujeres.
alteraciones oculares
Estas alteraciones incluyen nódulos de Lisch en la neurofibromatosis tipo 1 y otros déficits visuales debido a lesión cerebral, tumores o infecciones, así como hipoplasia del nervio óptico en displasia septoóptica.
déficits motores
Un examen neurológico detallado debe realizarse. Se pueden presentar déficits motores focales debido a tumores intracraneales, una lesión previa en la cabeza, hidrocefalia, meningitis o encefalitis.
tamaño de cabeza anormal
Debido a hidrocefalia, tumores cerebrales o infecciones en el sistema nervioso central (SNC).
Factores de riesgo
Fuerte
tumores cerebrales
Puede provocar la activación prematura del eje hipotalámico-hipofisario-gonadal. Entre estos se incluyen tumores como gliomas ópticos e hipotalámicos, astrocitomas (estos dos son los más frecuentes), ependimomas, tumores pineales y craneofaringiomas.[27][28] Los hamartomas del tubérculo cinéreo son tumores congénitos compuestos por una masa heterotópica que incluye neuronas neurosecretoras de la hormona liberadora de gonadotrofina (GnRH); se asocian con frecuencia a una pubertad precoz central y suelen aparecer antes de los 3 años de edad, sobre todo en los hombres.
irradiación craneal
Las dosis moderadas de radiación (25-47.5 Gy), usadas en el tratamiento de tumores cerebrales en niños, han sido asociadas con pubertad precoz (PP), con una relación directa entre la edad de inicio de la pubertad y la terapia.[29] Sin embargo, las dosis más altas están generalmente asociadas con una deficiencia de gonadotropina.
Síndrome de McCune-Albright
La enfermedad multisistémica caracterizada por la tríada clásica de pubertad precoz independiente de las gonadotropinas, máculas hiperpigmentadas o manchas café con leche y displasia fibrosa poliostótica. Aunque la afectación gonadal se produce por igual en niñas y niños, la sobreproducción de esteroides sexuales (y, por tanto, la pubertad precoz debida a la pubertad precoz independiente de gonadotrofinas) es mucho más frecuente en las mujeres.
Dos de estas tres características son necesarias para el diagnóstico. La hiperfunción autónoma en su mayor parte implica al ovario, pero otras afectaciones endocrinas involucran la tiroides (tirotoxicosis), las glándulas suprarrenales (síndrome de Cushing), la hipófisis (gigantismo/acromegalia o hiperprolactinemia) y las glándulas paratiroideas (hiperparatiroidismo). Esta afección esporádica es causada por una mutación de sentido erróneo de activación somática en el gen que codifica la subunidad alfa de la proteína-G que estimula la producción de adenosín monofosfato cíclico (AMPc).[Figure caption and citation for the preceding image starts]: Niña con pubertad precoz independiente de gonadotropinas (PPGI) y máculas hiperpigmentadas de color café como parte del síndrome de McCune-Albright (SMA)De la colección del Dr. A. Mehta; usado con autorización [Citation ends].
tumores gonadales
Pueden conducir a la pubertad precoz gonadotropina-independiente (PPGI) con altas concentraciones de esteroides sexuales. Estos tipos incluyen tumores de células de la granulosa, tumores de células de Leydig, gonadoblastomas y tumores suprarrenales virilizantes.
Los tumores de células germinales secretores de gonadotrofina coriónica humana son poco frecuentes y provocan pubertad precoz exclusivamente en los hombres.[38] Estos tumores pueden ocurrir en las gónadas, pero también pueden ocurrir en el cerebro (generalmente en la región pineal), el hígado, el retroperitoneo y el mediastino posterior.
Los tumores de células de Leydig están asociados a la virilización y la conversión de testosterona a estradiol provoca ginecomastia en los varones.
Los tumores de las células de la granulosa y los de las células germinativas pueden secretar tanto andrógenos como estradiol.
hiperplasia suprarrenal congénita (HSC)
Los niños con HSC por déficit de 21-hidroxilasa pueden presentar una pubertad precoz gonadotropina-independiente (PPGI) si no son tratados adecuadamente. Las niñas con HSC por déficit de 21-hidroxilasa presentan signos de virilización (p. ej., vellos púbicos y axilares, clitoromegalia) debido al exceso de andrógenos, aunque no presentan desarrollo mamario.
Débil
antecedentes familiares positivos
Existe una asociación entre la edad de la menarquia en madres e hijas.
En los niños varones, la testotoxicosis hereditaria o la pubertad precoz gonadotropina-independiente (PPGI) limitada a hombres está asociada con madurez prematura de células de Leydig y de células germinativas. Se hereda como una condición autosómica dominante que se manifiesta únicamente en hombres.[43][44]
La neurofibromatosis tipo 1 (NF1) es una afección autosómica dominante con un padre afectado.
exposición a hormonas exógenas
Incluye la píldora anticonceptiva o los geles de testosterona. Los agentes estrogénicos presentes en cosméticos y en productos alimenticios también se han implicado como causantes de pubertad a más temprana edad; las "epidemias" de telarquia prematura (desarrollo mamario aislado) en algunas áreas geográficas pueden estar relacionadas con una exposición ambiental a estrógenos.[22]
lesión en la cabeza
Puede provocar la activación prematura del eje hipotálamo-hipofisario-gonadal y la pubertad precoz central.
neurofibromatosis tipo 1
infecciones previas de sistema nervioso central
Las complicaciones tardías de la meningitis y la encefalitis incluyen la activación precoz del eje hipotálamo-hipofisario-gonadal y la pubertad precoz central.
hidrocefalia
Puede provocar la activación prematura del eje hipotálamo-hipofisario-gonadal y la pubertad precoz central.
anomalías hipofisarias congénitas
Causada por alteraciones estructurales (p. ej., displasia septoóptica y holoprosencefalia). La pubertad precoz o temprana puede estar aislada o combinada con otras deficiencias hormonales hipofisarias.[34]
adopción
abuso sexual
Se ha descrito como causa precipitante de la pubertad precoz central.[37] El desarrollo temprano puede revertirse con un cambio en el entorno.
El uso de este contenido está sujeto a nuestra cláusula de exención de responsabilidad