Etiología
Las causas se pueden dividir entre aquellas que son centrales o dependientes de la gonadotropina, en las que hay activación prematura del eje hipotalámico-hipofisario-gonadal, y aquellas debido a la activación prematura de los ovarios, los testículos o las glándulas suprarrenales, independientemente de la secreción de gonadotropina (pubertad precoz gonadotropina-independiente [PPGI]).
Pubertad precoz central (PPC)
La PPC idiopática es la causa más frecuente en las mujeres (97% en niñas de 6-8 años y 75% en niñas <6 años).[23] En los hombres, la incidencia informada de PPC idiopática es más variable, oscilando entre el 60% y alrededor del 90%.[24][25][26]
Neoplasias cerebrales como gliomas del nervio óptico (p. ej., en asociación con neurofibromatosis), craneofaringiomas o hamartomas.[27][28] Los hamartomas del tuber cinereum son tumores congénitos compuestos por una masa heterotópica que incluye neuronas neurosecretoras de hormona liberadora de gonadotropina (GnRH) frecuentemente asociados con PPC y que a menudo se producen antes de los 3 años de edad, especialmente en hombres. Otros tumores incluyen astrocitomas, ependimomas y tumores pineales.
Radioterapia craneal.[29]
Discapacidad neurológica como la hidrocefalia y la parálisis cerebral, así como las secuelas de infecciones como meningitis o encefalitis.[30]
Trauma craneoencefálico.[30]
Las mutaciones de ganancia de función en KISS1R, un receptor acoplado a proteínas G que es un ligando para la kisspeptina, pueden causar PPC, aunque estas mutaciones se encuentran muy raramente.[31] La interacción entre KISS1R y kisspeptina es necesaria para la función de la GnRH. Más frecuentemente, sobre todo en la PPC familiar, se encuentran mutaciones en el gen MKRN3 como causa. MKRN3 es un gen impreso cuya función es suprimir el eje hipotalámico-hipofisario-gonadal antes de la pubertad.[32] Las mutaciones en DLK1, un segundo gen impreso, son otra causa genética poco frecuente de PPC.[33]
Alteraciones en la línea media del prosencéfalo, como la holoprosencefalia o la displasia septoóptica.[34]
Asociación con la adopción de niños y los abusos sexuales.[35][36][37]
Pubertad precoz gonadotropina-independiente (PPGI)
Causas ováricas: quistes foliculares del ovario, tumores de células de la granulosa, tumores de células de Leydig y gonadoblastoma.
Causas testiculares: tumores de células de Leydig y una anomalía en el funcionamiento del receptor de la hormona luteinizante (LH) (por testotoxicosis o PPGI hereditaria). Esta última es causada por una mutación activadora en el gen del receptor de la LH.
Causas suprarrenales: la hiperplasia suprarrenal congénita (HSC) por déficit de 21-hidroxilasa, y menos frecuentemente de 11-hidroxilasa, en hombres causa PPGI. En niñas, la hiperplasia suprarrenal congénita (HSC) se presenta con signos de virilización (p. ej., vello púbico y axilar, y clitoromegalia) aunque no presentan desarrollo mamario. Otras causas suprarrenales incluyen el síndrome de Cushing y un tumor suprarrenal virilizante. La exposición prolongada a los esteroides sexuales en el PPGI tiene un efecto madurativo directo sobre el hipotálamo y puede acelerar la aparición de la PPC.
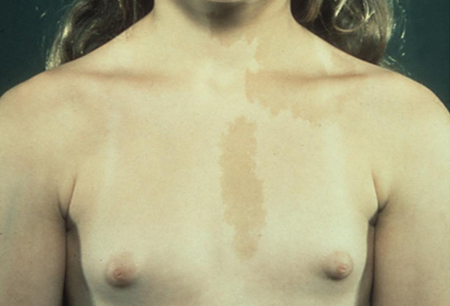
El síndrome de McCune-Albright (SMA), una afección esporádica causada por una mutación de sentido erróneo de activación somática en el gen que codifica la subunidad alfa de la proteína-G que estimula la producción de proteína-G monofosfato cíclico (AMPc). Da como resultado la tríada clásica de la PPGI, manchas color café con leche, y displasias fibrosas del hueso. La pubertad precoz debido al SMA es mucho más frecuente en las niñas que en los niños. La hiperfunción autónoma en su mayor parte implica al ovario, pero otras afectaciones endocrinas involucran la tiroides (tirotoxicosis), las glándulas suprarrenales (síndrome de Cushing), la hipófisis (gigantismo/acromegalia o hiperprolactinemia) y las glándulas paratiroideas (hiperparatiroidismo).[Figure caption and citation for the preceding image starts]: Niña con pubertad precoz independiente de gonadotropinas (PPGI) y máculas hiperpigmentadas de color café como parte del síndrome de McCune-Albright (SMA)De la colección del Dr. A. Mehta; usado con autorización [Citation ends].
La exposición a hormonas exógenas, como las píldoras anticonceptivas o los geles de testosterona, puede ser causa de un desarrollo puberal temprano en casos aislados. Los agentes estrogénicos presentes en cosméticos y en productos alimenticios también se han implicado como causantes de pubertad a más temprana edad; las "epidemias" de telarquia prematura (desarrollo mamario aislado) en algunas áreas geográficas pueden estar relacionadas con una exposición ambiental a estrógenos.[22]
Los tumores de células germinales secretores de gonadotrofina coriónica humana son una causa poco frecuente exclusivamente en hombres.[38] Estos tumores pueden ocurrir en las gónadas, el cerebro (generalmente en la región pineal), el hígado, el retroperitoneo y el mediastino posterior.
Fisiopatología
El aumento nocturno en la amplitud y pulsatilidad de la secreción de la hormona liberadora de gonadotropinas (GnRH) desde el hipotálamo es el primer cambio evidente en la pubertad.[39] La liberación de GnRH es el determinante característico del avance a la pubertad y a través de ella. Este mecanismo permanece latente desde los 2 años de edad hasta los 8 a 9 años de edad. La función normal de la GnRH depende de la interacción entre las entradas gliales neuronales inhibidoras (p. ej., ácido gamma-aminobutírico) y excitadoras (p. ej., kisspeptina, glutamato).[40]
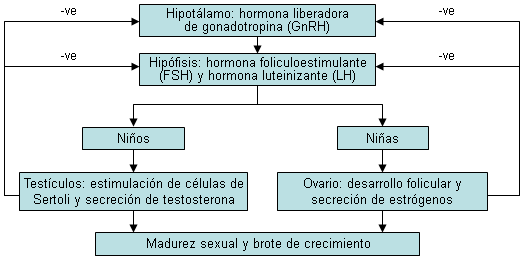
La GnRH hipotalámica, a su vez, estimula la secreción de hormonas pituitarias: la hormona foliculoestimulante (FSH) y la hormona luteinizante (LH). En los varones, la hormona luteinizante (LH) actúa sobre las células de Leydig para producir testosterona, mientras que la FSH actúa sobre las células de Sertoli para promover la espermatogénesis. En las niñas, una interacción compleja entre la LH y la FSH en las células tecales y de la granulosa da origen al desarrollo folicular con la producción de estrógenos y la ovulación.
En la pubertad precoz (PP) central, cuando el eje hipotalámico-hipofisario-gonadal se activa prematuramente, las gonadotropinas séricas se elevan (pubertad precoz gonadotropina-dependiente [PPGD]). El patrón del cambio endocrino es el mismo que en la pubertad normal (es decir, es consonante).
En la pubertad precoz (PP) debido a otras causas (suprarrenales, testiculares, ováricas u hormonas exógenas), la secreción de esteroides sexuales es autónoma e independiente del pulso de la hormona liberadora de gonadotropina (GnRH) hipotalámica. Se produce una pérdida de autorregulación normal y las concentraciones de esteroides sexuales son altas, generalmente, con niveles bajos o suprimidos de gonadotropinas. A esto se le denomina pubertad precoz independiente de gonadotropinas (PPGI). El desarrollo puberal no sigue el patrón de la pubertad normal (es decir, es disonante). La exposición prolongada a esteroides sexuales tiene un efecto madurativo directo sobre el hipotálamo y puede acelerar el inicio de la pubertad central.[Figure caption and citation for the preceding image starts]: Ciclo de retroalimentación hipotalámico-hipofisario-gonadal. GnRH, gonadotropinaseradora de gonadotropinas; FSH, hormona foliculoestimulante; LH, hormona luteinizanteDe la colección del Dr. A. Mehta; usado con autorización [Citation ends].
Por término medio, la pubertad tarda de 2 a 5 años en completarse y proporciona un incremento del crecimiento de 25 cm en las niñas y 30 cm en los niños. Los estrógenos, ya sean ováricos o aromatizados de la testosterona testicular, son el factor que media la respuesta aumentada a la hormona del crecimiento (GH) durante la pubertad.[41][42] La secreción prematura de esteroides gonadales en los niños da lugar a una estatura alta durante la infancia, debido a un ritmo acelerado de crecimiento lineal, con una estatura normal o baja en la edad adulta, debido a la fusión precoz de los cartílagos de crecimiento epifisarios.
Clasificación
Clasificación etiológica
Pubertad precoz central (PPC)
En la PPC (pubertad precoz dependiente de gonadotrofinas), el eje hipotálamo-hipófisis-gonadal se activa prematuramente.
El patrón de cambio endocrino es el mismo que en la pubertad normal (es decir, el desarrollo puberal es consonante).
Pubertad precoz gonadotropina-independiente (PPGI)
La secreción de esteroides sexuales (estrógenos o testosterona) es autónoma e independiente del impulso hipotalámico central de la hormona liberadora de gonadotrofina (GnRH).
Hay una pérdida de autorregulación normal y las concentraciones de esteroides sexuales son típicamente elevadas, con niveles bajos de gonadotropinas.
El desarrollo puberal no sigue el patrón de la pubertad normal (es decir, es disonante).
La exposición prolongada a los esteroides sexuales en el PPGI presenta un efecto madurativo directo sobre el hipotálamo y puede acelerar la aparición de la PPC.
El uso de este contenido está sujeto a nuestra cláusula de exención de responsabilidad