Abordaje
Los objetivos principales del tratamiento incluyen optimización de la estatura, inducción y mantenimiento del desarrollo puberal, tratamiento de la deficiencia de hormonas ováricas en curso y cribado y tratamiento de comorbilidades o complicaciones.[31]
Crecimiento deficiente
Los síntomas primarios son a menudo la estatura baja y el crecimiento deficiente.
Hormona de crecimiento (GH) humana recombinante
A menudo se considera que mejora la estatura en adultos. El objetivo es ayudar a que las niñas obtengan una estatura suficiente para prevenir la discapacidad y que puedan funcionar de forma independiente (p. ej., conducir un auto) así como para promover la integración social.
El tratamiento debe iniciarse desde el momento en que la niña sale de la curva normal de crecimiento hasta que la velocidad de crecimiento sea menor a 2 cm/año.[31]
El tratamiento en niñas muy jóvenes antes del retraso del crecimiento puede prevenir el desarrollo de una estatura baja. La puntuación de la desviación estándar de la estatura cercana a la de adultos fue >-2.0 para el 76% de las niñas que comenzaron a usar la hormona del crecimiento en promedio a los 24 meses y del 60% para las niñas que comenzaron a usar la hormona del crecimiento a los 4 años.[32]
El efecto del tratamiento se monitoriza mediante los niveles de respuesta de crecimiento y del factor de crecimiento similar a la insulina tipo 1 (IGF-1), que deben mantenerse debajo del límite superior de normalidad.
El tratamiento diario con GH durante 5 años iniciado a la edad de 8 años produce una ganancia de 7 cm en la estatura de las niñas con síndrome de Turner, en comparación con aquellas que no reciben GH.[33]
El tratamiento con hormona de crecimiento (GH) diario durante 8.3 años hasta 8.9 años iniciado a la edad de 6.5 a 6.9 años produce una ganancia de 11.9 a 15.7 cm en la estatura de las niñas con síndrome de Turner tratadas con dos dosis distintas de hormona de crecimiento (GH).[34]
La falta de una respuesta de crecimiento buena se debe comúnmente al hipotiroidismo, la enfermedad celíaca o la falta de cumplimiento.
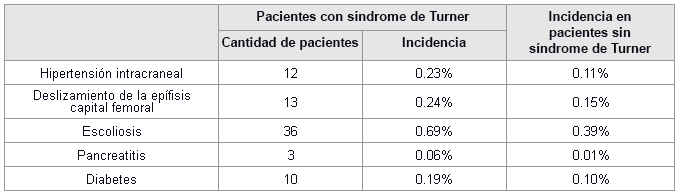
Los efectos adversos de un seguimiento durante 4 a 5 años incluyen aumento de la presión intracraneal, deslizamiento de la epífisis capital femoral, escoliosis, pancreatitis y, posiblemente, un aumento del inicio de diabetes de tipo 1.[5][35][Figure caption and citation for the preceding image starts]: Incidencia de los efectos adversos del tratamiento con hormona del crecimientoDatos del National Cooperative Growth Study (Bolar K, et al. J Clin Endocrinol Metab. 2008;93:344-351) [Citation ends].
Oxandrolona
El principal impedimento de un tratamiento con GH exitoso es el diagnóstico tardío, el cual no es infrecuente.
Para las niñas diagnosticadas de forma tardía que tienen solo un margen de tiempo para realizar el tratamiento o para aquellas que no pueden obtener la GH, algunos pediatras agregan oxandrolona, un andrógeno oral no aromatizable, al tratamiento con GH para promover un crecimiento lineal.[36] Generalmente, el tratamiento con oxandrolona promueve algunos centímetros de estatura adicional.[37][38][39] Sin embargo, puede inhibir el desarrollo mamario y causar virilización, incluso en dosis bajas, debido a sus efectos androgénicos.[37][38]
Retraso puberal
El objetivo es inducir el desarrollo puberal a la par que sus pares y de la forma más fisiológica posible. Esto también asegura que las niñas experimenten los efectos saludables del estrógeno en los huesos y otros tejidos y que logren una adecuación psicosocial óptima para su afección.
El tratamiento incluye dosis en aumento gradual de terapia de estrógenos, y a continuación un tratamiento de estrógenos combinado con progesterona cíclica. No se recomienda el tratamiento con agentes combinados (estrógenos equinos conjugados y medroxiprogesterona) desarrollados para mujeres menopáusicas. No se debe inducir la pubertad utilizando píldoras anticonceptivas porque las dosis de estrógeno son demasiado altas y los progestágenos androgénicos impiden el desarrollo mamario óptimo.
Reemplazo de estrógenos
Si no se ha producido un desarrollo espontáneo de las mamas a la edad de 11-12 años y la hormona foliculoestimulante sérica está elevada, se debe iniciar una terapia de reemplazo de estrógenos.
La preparación de elección consiste en estradiol transdérmico en la dosis más pequeña disponible.[5] La administración transdérmica evita los efectos de primer paso en el hígado. También se puede utilizar estradiol oral como alternativa.
Si continúa el potencial de crecimiento lineal (es posible que la paciente ya haya iniciado un tratamiento con hormona de crecimiento), se debe continuar con una dosis baja con un aumento más lento de la dosis hasta lograr la estatura óptima. Las dosis más altas detienen el crecimiento. Se debe monitorizar la edad ósea y, en caso de que avance rápidamente, se debe reducir la dosificación.
Si no hay potencial de mayor crecimiento o si no existe evidencia de un avance rápido de la edad ósea, la dosis de estradiol se aumenta gradualmente a lo largo de aproximadamente 2 años, hasta una dosis completa para adultos o hasta que se produzca sangrado vaginal.
Progesterona cíclica
Se agrega a la terapia con estrógenos una vez que hay hemorragia de privación o después de 2 años de tratamiento con estrógenos.[5]
Para inducir la menstruación se recomienda el tratamiento con progesterona micronizada oral durante los últimos 10 días de cada mes. Otra opción es el tratamiento durante las últimas 2 semanas de un ciclo de 3 meses.
Anomalías cardíacas congénitas
Las alteraciones más frecuentes son coartación aórtica y válvulas aórticas bicúspides. Otras alteraciones cardíacas incluyen venas pulmonares anómalas parciales, hipoplasia de cavidades izquierdas y dilatación de la aorta. La prevalencia de defectos cardiovasculares es mucho mayor en aquellas pacientes con evidencia clara de linfedema fetal, el cual se puede describir como inflamación de los tejidos, sobre todo de la cabeza y el cuello, debido a un desarrollo linfático disminuido. Las manifestaciones posnatales comunes son cuello alado y nacimiento capilar y orejas de implantación baja.
En el momento del diagnóstico inicial, indistintamente de la edad, se debe realizar una evaluación cardiovascular integral con un especialista en cardiopatía congénita e iniciar el tratamiento adecuado.[27] En el 30% de las pacientes asintomáticas se observa una válvula bicúspide funcional como resultado de la fusión completa o parcial de los velos coronarios derecho e izquierdo, lo que implica un riesgo de infección, deterioro de las válvulas, dilatación y disección aórtica.[18]
Los defectos cardiovasculares congénitos son la causa principal de mortalidad prematura en el síndrome de Turner. Con el tiempo, las niñas con alteraciones cardíacas deben derivarse a una clínica para cardiopatías congénitas en adultos, puesto que existen una morbilidad y mortalidad evidentes en curso asociadas con estos defectos.
Manejo continuo tras el establecimiento de sangrado cíclico
Terapia de reemplazo hormonal (TRH) ovárica
Para estados hipoestrogénicos, se debe usar un tratamiento oral o transdérmico con estrógenos para reducir la osteoporosis, la enfermedad cardiovascular y la atrofia urogenital, y mejorar la calidad de vida.[40]
Las mujeres con síndrome de Turner deben continuar normalmente con el THS tras la inducción y el desarrollo de la pubertad. El THS debe continuarse hasta aproximadamente los 50 años de edad, luego se debe emprender otra terapia de estrógenos según las consideraciones de riesgo/beneficio para la paciente.[41]
El estrógeno se debe combinar con tratamiento con progestágeno (administrado de forma continua o cíclica) para prevenir el cáncer y la hiperplasia endometrial.[40]
Para las mujeres que deseen evitar el embarazo, los anticonceptivos orales combinados son más efectivos que el tratamiento hormonal con estrógenos. Otra opción aceptable es un dispositivo intrauterino con levonorgestrel.[40]
Una baja masa ósea se debe manejar con terapia de sustitución hormonal con estrógeno, una ingesta adecuada de calcio en la dieta, niveles normales de vitamina D y actividades de carga de peso, no con bifosfonatos.[40]
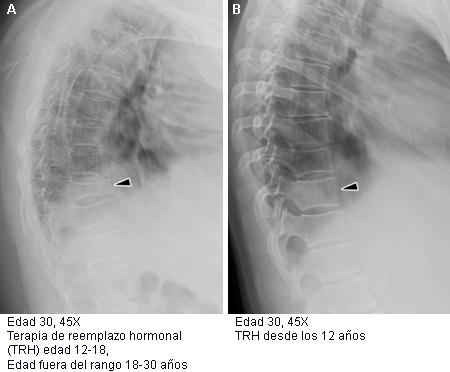
Entre los riesgos de no implementar la TRH ovárica en mujeres jóvenes con insuficiencia ovárica prematura se incluye el riesgo de osteoporosis prematura grave.[Figure caption and citation for the preceding image starts]: Importancia de la terapia con estrógenos en las mujeres adultas jóvenes con síndrome de Turner (ST): La figura A de la radiografía muestra un colapso potencial de T11, osteoporosis difusa y cifosis dorsal en una mujer con ST que suspendió el tratamiento hormonal sustitutivo (THS) a la edad de 18 años. La figura B muestra arquitectura espinal y salud ósea normales en otra mujer con ST, de 30 años de edad, que siguió la TRH consistentemente desde los 12.8 años de edadDe la colección personal de la Dra. Carolyn Bondy, MS (estudio realizado por National Institutes of Health [NIH]) [Citation ends].
Implantes de mamas
Es posible que las niñas que presentan signos notorios de linfedema fetal y pezones hipoplásicos no logren un desarrollo mamario adecuado con el tratamiento con estrógenos y por lo tanto pueden requerir implantes de mamas.
Fertilidad y embarazo
La mayoría de las mujeres con síndrome de Turner son estériles, pero aproximadamente entre el 5% y el 8% pueden producir embarazos espontáneos.[5] Existe una mayor incidencia de un feto con aneuploidía cuando en mujeres con síndrome de Turner se utilizan sus propios ovocitos. El embarazo empeora los problemas metabólicos, hipertensivos y cardiovasculares subyacentes y puede resultar muy peligroso para las mujeres con síndrome de Turner; por lo tanto, se requiere una monitorización estrecha en las niñas mayores de 10 años de edad en relación con la fertilidad potencial y la educación sobre cuestiones reproductivas y conductas sexuales.
Dado que la fertilidad en mujeres con síndrome de Turner disminuye rápidamente con la edad, se debe considerar ofrecer tratamiento para la fertilidad a una edad temprana.[5] Las mujeres jóvenes con síndrome de Turner en mosaico deben recibir asesoramiento sobre la posibilidad de hiperstimulación ovárica controlada y criopreservación de ovocitos, pero no se recomienda la recuperación de ovocitos de rutina en niñas menores de 12 años de edad.[5] Las mujeres con síndrome de Turner pueden estar interesadas en desarrollar un embarazo mediante reproducción asistida con ovocitos de donantes. Dichos embarazos pueden tener un riesgo inusualmente alto de muerte materna debido a la disección o rotura aórtica y debido a la preeclampsia y sus complicaciones.[42][43][44]
La realización de un cribado sumamente estricto previo al embarazo y la educación de la paciente sobre los riesgos antes de intentar una reproducción asistida son imprescindibles para las mujeres con síndrome de Turner.[45] La American Heart Association y el Grupo de Consenso Internacional del Síndrome de Turner han hecho recomendaciones para el manejo de las mujeres embarazadas con síndrome de Turner; esto debe llevarlo a cabo un equipo multidisciplinario, incluido un especialista en medicina materno-fetal y un cardiólogo con la experiencia adecuada.[5][27] La American Society for Reproductive Medicine ha hecho recomendaciones adicionales sobre las contraindicaciones del embarazo para las mujeres con síndrome de Turner, debido a los mayores riesgos cardiovasculares en el embarazo.[42]
El uso de este contenido está sujeto a nuestra cláusula de exención de responsabilidad