Abordagem
O maior conhecimento público sobre o câncer de mama fez com que uma proporção significativa de mulheres se apresentassem ao médico com massas palpáveis. Os cânceres de mama detectados clinicamente ou por autoexame da mama geralmente se encontram em estádios mais avançados.[31] As massas identificadas na mamografia podem ser submetidas a outras avaliações com ultrassonografia para determinar se elas são císticas ou sólidas. O rastreamento mamográfico levou a uma detecção maior de cânceres de mama em estágios não palpáveis.[32][33]
História
A mediana de idade ao diagnóstico do câncer de mama nas mulheres é de 63 anos.[34] A maioria dos cânceres de mama é esporádica (ou seja, em pacientes sem história familiar de câncer de mama).
Aproximadamente 5% a 10% de todos os cânceres de mama são diagnosticados em pacientes com mutação nos genes BRCA-1 ou BRCA-2.[35] As variantes patogênicas em BRCA-1 e BRCA-2 estão associadas a um alto risco de câncer de mama, com razão de chances de 7.62 (IC de 95%: 5.33 a 11.27) e 5.23 (IC de 95%: 4.09 a 6.77), respectivamente.[36] Mutações BRCA-1 e BRCA-2 são mais comuns em mulheres com história familiar de:[37]
câncer de mama aos ou antes dos 50 anos
câncer de mama masculino
câncer de ovário
câncer de pâncreas
câncer de próstata (com metástase ou grupo de alto ou muito alto risco)
≥3 diagnósticos de câncer de mama e/ou próstata no mesmo lado da família
Ascendência judaica asquenaze.
A história familiar deve incluir qualquer membro da família com câncer, local primário de câncer, se o parente afetado apresentava vários cânceres primários, idade quando do diagnóstico, idade quando da morte e sexo. US Preventive Services Task Force. BRCA-related cancer: risk assessment, genetic counselling and genetic testing. 2019 Opens in new window
História de biópsia prévia de hiperplasia atípica traz um risco quatro a cinco vezes maior no desenvolvimento de câncer de mama.[38][39] Para aqueles com uma história de carcinoma lobular in situ (CLIS), há um risco aumentado de sete a 12 vezes.[40] Pacientes diagnosticados com um câncer invasivo têm um risco de câncer de mama contralateral estimado em 0.5% a 1% ao ano, cumulativo ao longo da vida.[40]
Em mulheres menopausadas, terapia de reposição hormonal apenas com estrogênio está associada a pouca ou nenhuma alteração no risco de câncer de mama.[41] Um estrogênio prescrito em combinação com um progestágeno está associado a um aumento na incidência de câncer de mama.[41][42][43][44][45][46]
Há uma associação entre o aumento da densidade das mamas (categorizada pelo Breast Imaging Reporting and Data System [BI-RADS]) e a incidência de câncer de mama em mulheres com mais de 65 anos; no entanto, os mecanismos subjacentes à associação observada ainda não estão claros.[47]
Exame físico
Achados de exame físico isolado não podem estabelecer definitivamente uma massa como benigna ou maligna. Contudo, massas fixas irregulares são suspeitas quanto à malignidade.[48] Lesões malignas também podem estar associadas com o espessamento da pele (por exemplo, "peau d'orange", como a casca de uma laranja) ou alterações nos mamilos.[3] Deve-se realizar um exame das mamas bilateral completo, incluindo avaliação das axilas e linfonodos regionais, para procurar:[49]
Variação no tamanho da mama[Figure caption and citation for the preceding image starts]: Paciente com câncer de mama inflamatório que se apresentou com uma mama retraídaCortesia da Drª Anees Chagpar [Citation ends].
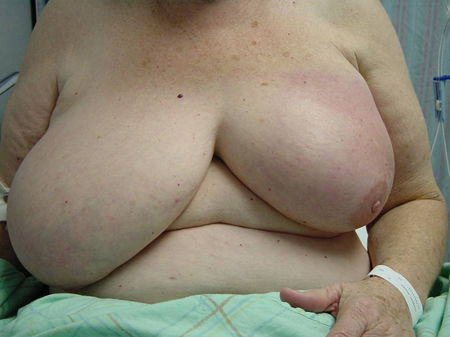
Massas vegetantes[Figure caption and citation for the preceding image starts]: Massa palpável com envolvimento de pele na mama direitaCortesia da Drª Anees Chagpar [Citation ends].
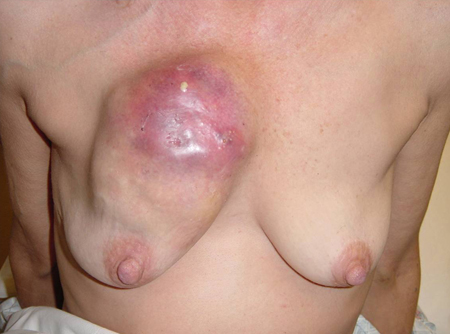 [Figure caption and citation for the preceding image starts]: Massa palpável com envolvimento de pele na mama esquerdaCortesia da Drª Anees Chagpar [Citation ends].
[Figure caption and citation for the preceding image starts]: Massa palpável com envolvimento de pele na mama esquerdaCortesia da Drª Anees Chagpar [Citation ends].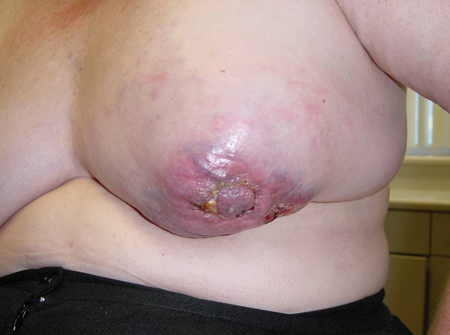
Ondulação ou retração da pele[Figure caption and citation for the preceding image starts]: Paciente com massa mamária grande e retração para baixo da mama esquerda, observada ao elevar os braçosCortesia da Drª Anees Chagpar [Citation ends].
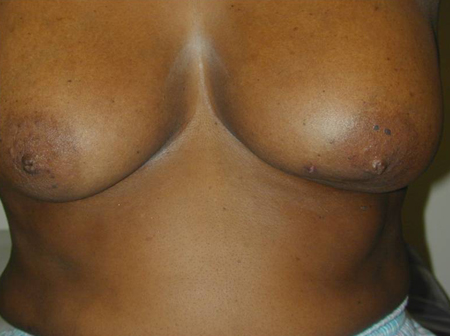
Inversão ou escoriação do mamilo (achado clássico da doença de Paget da mama)[Figure caption and citation for the preceding image starts]: Escoriação do mamilo em paciente com doença de Paget da mamaCortesia da Drª Anees Chagpar [Citation ends].
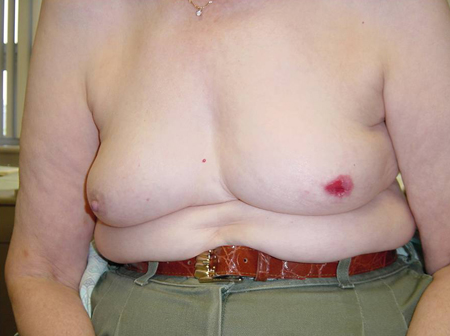
Esses achados podem ser acentuados se for solicitado que o paciente estique os braços acima da cabeça. Da mesma forma, solicitar que os pacientes coloquem as mãos nos quadris e apertem para dentro, ao mesmo tempo em que flexionam os músculos peitorais, pode revelar envolvimento da parede torácica.
Os linfonodos que drenam a fossa cervical, supraclavicular e infraclavicular devem ser avaliados. O exame abrangente requer avaliação do paciente sentado ereto e deitado de costas, uma vez que as massas podem ser observadas melhor em uma posição que em outra.
Um ensaio clínico randomizado e controlado mostrou que estimular a documentação do exame físico com o uso de um formulário específico resultou em maior taxa de avaliações mais aprofundadas de massas mamárias e melhor taxa de detecção de câncer.[50] Esses resultados indicam que o exame clínico focado pode resultar em melhora de desempenho.
Mamografia
As diretrizes dos EUA recomendam que todas as mulheres ≥30 anos que apresentarem massa mamária realizem uma mamografia diagnóstica (com visualizações adicionais, como compressão local, ampliação ou posição tangencial) e tomossíntese digital da mama (ou mamografia com contraste, se disponível) associada a uma ultrassonografia.[19][51] Deve-se notar qualquer doença multifocal ou multicêntrica.
No cenário de uma massa mamária palpável, a mamografia é 82% a 94% sensível e 55% a 84% específica para a detecção de câncer de mama.[52][53][54][55]
Nas mulheres <30 anos com massa mamária palpável e achados da ultrassonografia que representarem suspeita de neoplasia maligna, as diretrizes dos EUA recomendam a mamografia e a tomografia digital da mama como exames de imagem subsequentes.[19][51]
As diretrizes do Reino Unido recomendam que as mulheres ≥30 anos com nódulo mamário inexplicado sejam encaminhadas com urgência a um mastologista, para diagnosticar ou descartar câncer em até 28 dias após o encaminhamento.[56] Para mulheres com <30 anos com nódulo mamário inexplicado, as diretrizes recomendam considerar um encaminhamento não urgente.[56]
Os radiologistas geralmente caracterizam os achados na ultrassonografia ou mamografia de acordo com o BI-RADS.[57][58] Alguns defendem registrar a densidade da mama e o uso de terapia hormonal, uma vez que esses fatores influenciam o desempenho da mamografia de maneira significativa.[59][60][Figure caption and citation for the preceding image starts]: Critérios do BI-RADS (Breast Imaging Reporting and Data System)Cortesia da Drª Anees Chagpar [Citation ends].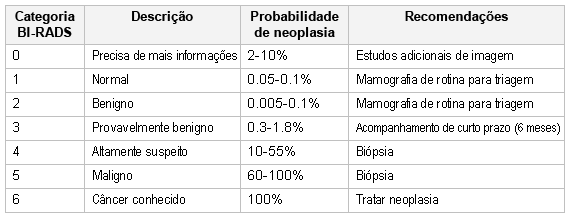 [Figure caption and citation for the preceding image starts]: Mamografia de rastreamento demonstrando massa mamáriaCortesia da Dra. Nancy Pile, Universidade de Louisville; usado com permissão [Citation ends].
[Figure caption and citation for the preceding image starts]: Mamografia de rastreamento demonstrando massa mamáriaCortesia da Dra. Nancy Pile, Universidade de Louisville; usado com permissão [Citation ends].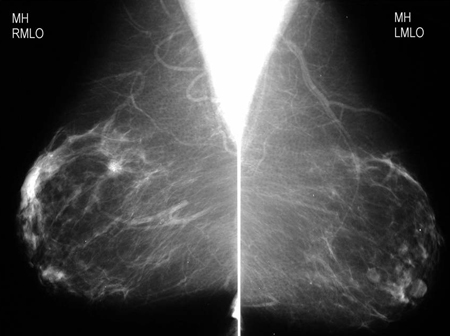 [Figure caption and citation for the preceding image starts]: Visualização de magnificação demonstrando uma massa espiculada irregular com calcificações associadasCortesia da Dra. Nancy Pile, Universidade de Louisville; usado com permissão [Citation ends].
[Figure caption and citation for the preceding image starts]: Visualização de magnificação demonstrando uma massa espiculada irregular com calcificações associadasCortesia da Dra. Nancy Pile, Universidade de Louisville; usado com permissão [Citation ends].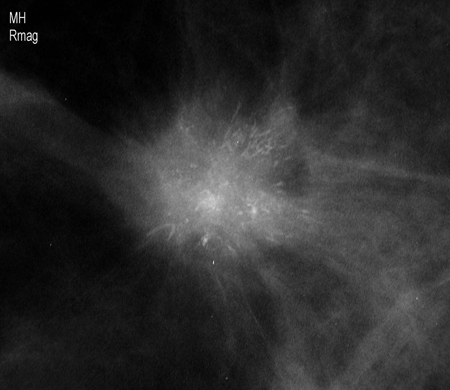
O BI-RADS foi desenvolvido pelo American College of Radiologists como um padrão de comparação para classificar as imagens de mamografia e ultrassonografia.[58] Ele estabelece uma classificação para o nível de suspeita para a possibilidade de câncer de mama. O ACR recomenda que um escore de 1 a 2 permite que a paciente retome o rastreamento de rotina; um escore igual a 3 pode requerer outros exames de imagem com mamografia e/ou ultrassonografia, ou acompanhamento de curto prazo; um escore de 4 a 5 requer uma biópsia tecidual.[58]
Um estudo de imagem negativo de uma massa mamária palpável requer biópsia quando a suspeita clínica permanece alta.[19][51] Um escore de 6 é atribuído apenas depois de a biópsia ser examinada e constatada como cancerosa; neste caso, o tratamento é necessário.[58]
As diretrizes da National Comprehensive Cancer Network (NCCN) recomendam que pacientes com escore BI-RADS de 1 e baixa suspeita clínica de câncer de mama sejam submetidas a exame físico em 3 a 6 meses.[19] Se estiver estável ou houver diminuição de tamanho, o exame de rotina pode ser retomado. Recomenda-se um tratamento clínico adequado adicional (que pode incluir encaminhamento a um especialista em mama, exames de imagem complementares e/ou amostragem tecidual) se houver aumento significativo no tamanho da massa palpável ou se houver suspeita clínica.[19]
O NCCN recomenda que pacientes com escore BI-RAD de 2 com baixa suspeita clínica (por exemplo, um cisto simples) retomem o rastreamento de rotina. Palpação ou amostragem tecidual guiada por imagem é recomendada para pacientes com escore BI-RAD de 2 com sintomas palpáveis clinicamente suspeitos.[19]
Ultrassonografia da mama
Normalmente a ultrassonografia é considerada o exame diagnóstico inicial de primeira escolha em pacientes <30 anos de idade, pois a densidade do tecido mamário nas mulheres mais jovens limita a sensibilidade da mamografia.[3][51][61][62] Há relatos de que a taxa de falsos-negativos nas mamografias chega a até 52% em pacientes com <35 anos de idade com uma massa mamária maligna palpável.[63]
Geralmente, a ultrassonografia é realizada além da mamografia na avaliação de mulheres idosas com suspeita de câncer de mama.[19][64]
A ultrassonografia está disponível rotineiramente no contexto ambulatorial e é uma extensão imediata para o exame físico. O American College of Radiology publicou diretrizes que podem auxiliar os médicos na realização da ultrassonografia da mama.[61][65]
A ultrassonografia pode identificar estruturas císticas simples ou complexas.[51] Cistos simples são lesões preenchidas por fluidos que têm apresentação lisa, arredondada, bem-demarcada e anecoica. Se eles não tiverem septações ou detritos celulares internos, eles podem ser simplesmente acompanhados. A ultrassonografia não é capaz de detectar microcalcificações na mama.[Figure caption and citation for the preceding image starts]: Imagem ultrassonográfica de um cisto simplesCortesia do Dr. Lane Roland, Universidade de Louisville; usado com permissão [Citation ends].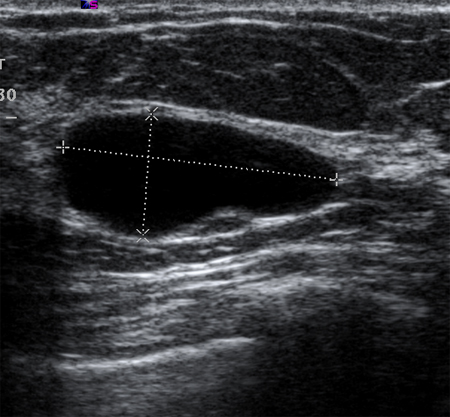
O manejo sugerido para pacientes com massas "provavelmente benignas" na ultrassonografia de mama inclui:[19]
Observação, se a suspeita clínica for baixa, com exame clínico e exame de imagem com ultrassonografia ou mamografia em 6, 12 e 24 meses, para documentar a estabilidade.
Biópsia percutânea com agulha grossa para fazer um diagnóstico definitivo, mas deixando a lesão in situ. Se o resultado for benigno e concordante, recomenda-se a realização de um exame clínico da mama a cada 6 a 12 meses, com ou sem ultrassonografia ou mamografia, por 1 ano, para avaliar a estabilidade.
Também se pode realizar ultrassonografia da axila para avaliação de linfadenopatia e biópsia de linfonodos anormais.[Figure caption and citation for the preceding image starts]: Algoritmo de diagnóstico para ultrassonografia de mamaCortesia da Drª Anees Chagpar [Citation ends].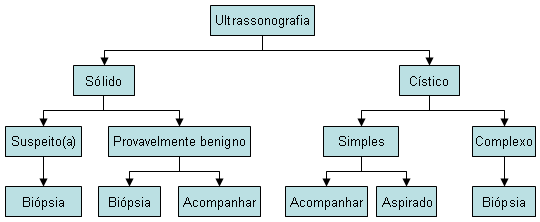
Ressonância nuclear magnética (RNM) da mama
As diretrizes da National Comprehensive Cancer Network (NCCN) recomendam considerar a RNM com e sem contraste para investigar a presença de câncer de mama inflamatório se a paciente apresentar alterações cutâneas consistentes com doença mamária grave, estiver na categoria BI-RADS 1-3 ou na categoria BI-RADS 4-5 e tiver tido uma biópsia percutânea com agulha grossa benigna.[19] A RNM pode também ser usada para avaliar a suspeita de descarga mamilar sem massa palpável quando os achados da mamografia e da ultrassonografia forem BIRADS 1-3.[19]
A European Society of Medical Oncology recomenda a RNM da mama para investigar suspeitas de câncer de mama se houver incertezas diagnósticas após a ultrassonografia da mama e a mamografia.[64]
A US Preventive Services Task Force conclui que não há evidências suficientes para determinar o equilíbrio entre os benefícios e os danos do rastreamento suplementar para câncer de mama com RNM (ou ultrassonografia mamária) nas mulheres identificadas como tendo mamas densas com uma mamografia de rastreamento negativa.[66]
O American College of Radiology não recomenda a RNM na avaliação inicial de pacientes com massa mamária.[51]
Para pacientes que se submetem a RNM, a imagem ponderada por difusão pode ser superior à da RNM com contraste para diferenciar entre lesões benignas e malignas.[67] A biópsia é indicada para qualquer lesão suspeita na RNM.
Aspiração e biópsia de mama
Um diagnóstico definitivo de carcinoma mamário requer uma biópsia da mama. Três tipos principais de biópsia são comumente realizados.
Aspiração com agulha fina (AAF): envolve a inserção de uma agulha de calibre 22 a 25 na massa mamária e a extração de células. Aumentar o número de passes aumenta a razão de chances do diagnóstico por AAF.[68] Em seguida, as células podem ser colocadas em uma lâmina ou bloco celular. As vantagens da AAF consistem na rapidez e na facilidade de execução e no fato dela poder ser realizada no ambiente clínico. As desvantagens são que ela não mostra a estrutura histológica e não pode auxiliar na diferenciação entre carcinoma ductal in situ e neoplasia maligna invasiva. Entretanto, nas mãos de um citopatologista experiente, essa técnica pode ajudar a distinguir as lesões benignas das malignas e é valiosa para avaliar os linfonodos axilares.[68][69]
Biópsia percutânea com agulha grossa: utilizando uma agulha de calibre de 8 a 14, fornece uma amostra de tecido maior que a AAF. Pode ser realizada por palpação, sob controle estereotático, ou guiada por ultrassonografia. Esta técnica pode ser feita no ambiente clínico; é relativamente rápida e fácil e permite o diagnóstico histológico. Caso o diagnóstico seja de neoplasia maligna, estudos do receptor de hormônio podem ser conduzidos nas amostras da biópsia com agulha. Vários instrumentos podem ser utilizados para obter esses espécimes; alguns deles utilizam auxílio de vácuo, outros energia de radiofrequência.[70][71] Em geral, a biópsia percutânea com agulha grossa é o método de escolha para o diagnóstico histológico das massas mamárias.[72]
Biópsia por excisão: envolve retirar toda a massa mamária para um diagnóstico histológico preciso. Essa técnica invasiva, no caso de uma massa assintomática benigna, pode não ser necessária; e no caso de uma massa maligna, pode não evitar a necessidade de um segundo procedimento para tratar o câncer uma vez que o diagnóstico tiver sido firmado. Os achados, por biópsia com agulha, de hiperplasia atípica ou cicatrizes radiais requerem uma biópsia por excisão para descartar uma neoplasia maligna concomitante.[Figure caption and citation for the preceding image starts]: Técnicas de biópsia da mama (AAF; aspiração com agulha fina)Cortesia da Drª Anees Chagpar [Citation ends].

Cistos dolorosos
A aspiração guiada por ultrassonografia pode ser realizada. O líquido do cisto aspirado não deve ser enviado para citologia porque, com a exceção de líquido cístico hemorrágico, não se costumam identificar células malignas.[73]
Os cistos que persistem ou não se resolvem completamente com a aspiração devem ser submetidos a biópsia para descartar a malignidade. Da mesma forma, a biópsia deve ser considerada em cistos complexos ou naqueles com elementos sólidos. As características sonográficas podem classificar uma massa sólida tanto como "provavelmente benigna" quanto como "suspeita". Massas lisas, ovais, lobuladas, com margens claramente definidas e mais largas que compridas geralmente são benignas (por exemplo, fibroadenoma). Se a massa é irregular, heterogênea, tem margens espiculadas ou pouco definidas, é mais comprida que larga, ela é considerada "suspeita" para malignidade, e deve ser realizada uma biópsia.[Figure caption and citation for the preceding image starts]: Imagem ultrassonográfica de um carcinoma complexoCortesia do Dr. Lane Roland, Universidade de Louisville; usado com permissão [Citation ends].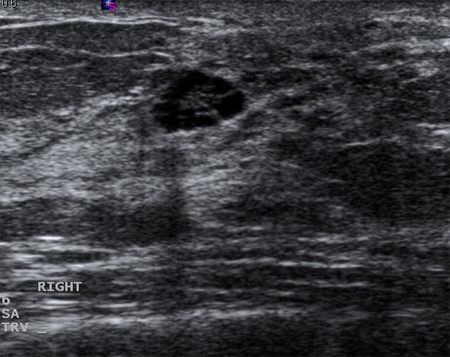 [Figure caption and citation for the preceding image starts]: Imagem ultrassonográfica de fibroadenomaCortesia do Dr. Lane Roland, Universidade de Louisville; usado com permissão [Citation ends].
[Figure caption and citation for the preceding image starts]: Imagem ultrassonográfica de fibroadenomaCortesia do Dr. Lane Roland, Universidade de Louisville; usado com permissão [Citation ends].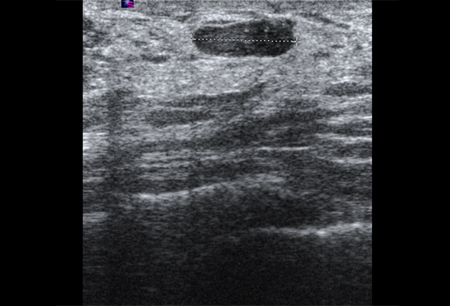 [Figure caption and citation for the preceding image starts]: Imagem ultrassonográfica de um carcinoma invasivoCortesia do Dr. Lane Roland, Universidade de Louisville; usado com permissão [Citation ends].
[Figure caption and citation for the preceding image starts]: Imagem ultrassonográfica de um carcinoma invasivoCortesia do Dr. Lane Roland, Universidade de Louisville; usado com permissão [Citation ends].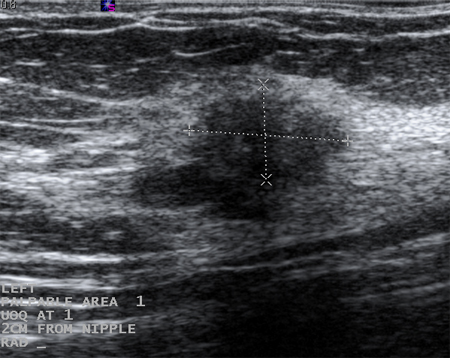
O uso deste conteúdo está sujeito ao nosso aviso legal