ლეიშმანიოზის მკურნალობა კომპლექსურია. პირველადი სამკურნალო ვარიანტების ზოგადი განხილვის შემდეგ, დისკუსია ეფუძნება კლინიკურ სინდრომებს. მნიშვნელოვანია გვახსოვდეს, რომ მკურნალობის შესახებ არსებული ლიტერატურა მოიცავს რამდენიმე კონტროლირებულ კლინიკურ კვლევას, განსხვავდება მეთოდოლოგიით და მკურნალობის გამოსავლებით.
ლეიშმანიოზის ყველა ტიპის შემთხვევაში, პარაზიტის და მასპინძლის გარკვეული მახასიათებლები გავლენას იქონიებს მკურნალობის შედეგებზე. მკურნალობის გამოსავლები განსხვავდება არა მხოლოდ სახეობის მიხედვით, არამედ სხვადასხვა გეოგრაფიულ რეგიონებში ერთი და იგივე სახეობით გამოწვეული ინფექციის შემთხვევებშიც. მაგალითად, Leishmania donovani-ით გამოწვეული ვისცერული ლეიშმანიოზის მკურნალობაზე პასუხი მნიშვნელოვნად განსხვავებულია სამხრეთ აზიასა და აღმოსავლეთ აფრიკაში. ლიპოსომური ამფოტერიცინი-B უპირატესია პირველ შემთხვევაში, ხოლო ხუთვალენტიანი ანტიმონიური პრეპარატები იძლევა უფრო მაღალ ეფექტურობას მეორე რეგიონში.[107]Burza S, Croft SL, Boelaert M. Leishmaniasis. Lancet. 2018 Sep 15;392(10151):951-70.
http://www.ncbi.nlm.nih.gov/pubmed/30126638?tool=bestpractice.com
მასპინძლის ფაქტორები, რომლებიც გავლენას ახდენენ, მკურნალობის ეფექტურობაზე, მოიცავს კვების სტატუსს და იმუნოკომპრომისული მდგომარეობის (მაგალითად, აივ/შიდსის) არსებობას.
პარაზიტის საწინააღმდეგო პრეპარატების გარდა, განსახილველია კოინფექციების მართვა და/ან დამხმარე მოვლა, განსაკუთრებით ვისცერული ლეიშმანიოზის დროს. თერაპიის მიზანი ლეიშმანიოზის ყველა ფორმის დროს არის კლინიკური განკურნება, რადგან ლეიშმანიის პარაზიტები რჩება მკურნალობის შემდეგაც.[108]Martínez-Valencia AJ, Daza-Rivera CF, Rosales-Chilama M, et al. Clinical and parasitological factors in parasite persistence after treatment and clinical cure of cutaneous leishmaniasis. PLoS Negl Trop Dis. 2017 Jul 13;11(7):e0005713.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5526576
http://www.ncbi.nlm.nih.gov/pubmed/28704369?tool=bestpractice.com
[109]Dereure J, Duong Thanh H, Lavabre-Bertrand T, et al. Visceral leishmaniasis: persistence of parasites in lymph nodes after clinical cure. J Infect. 2003 Jul;47(1):77-81.
http://www.ncbi.nlm.nih.gov/pubmed/12850167?tool=bestpractice.com
თერაპიის შერჩევისას გასათვალისწინებელია რეგიონული ეფექტურობა, უსაფრთხოება, ხელმისაწვდომობა და ხარჯი. უკანასკნელი ორი კი ხშირად გადამწყვეტია მწირი რესურსების მქონე პირობებში გადაწყვეტილების მიღებისას.
ლეიშმანიოზის საწინააღმდეგო მედიკამენტები
ამფოტერიცინი B
ლიპოსომური ამფოტერიცინი-B უპირატესი ვარიანტია ლეიშმანიოზის სამკურნალოდ, როცა ხელმისაწვდომია. მისი გამოყენება ლიმიტირებულია ფასის, ხელმისაწვდომობის და ცივი ჯაჭვის საჭიროების გამო. დამტკიცებულია ევროპასა და აშშ-ში ვისცერული ლეიშმანიოზის სამკურნალოდ; სხვა ტიპის ლეიშმანიოზის დროს მისი გამოყენება დამტკიცებული არ არის. ლიპოსომური ამფოტერიცინი-B, როგორც წესი, კარგი ამტანობით ხასიათდება; გვერდითი ეფექტებია: ინფუზიასთან დაკავშირებული რეაქციები (ჟრჟოლა, ცხელება), გულისრევა, ღებინება, ჰიპოკალიემია და თირკმლის უკმარისობა.[110]Berman JD. U.S Food and Drug Administration approval of AmBisome (liposomal amphotericin B) for treatment of visceral leishmaniasis. Clin Infect Dis. 1999 Jan;28(1):49-51.
https://academic.oup.com/cid/article/28/1/49/302484?login=false
http://www.ncbi.nlm.nih.gov/pubmed/10391695?tool=bestpractice.com
[111]Berman JD, Badaro R, Thakur CP, et al. Efficacy and safety of liposomal amphotericin B (AmBisome) for visceral leishmaniasis in endemic developing countries. Bull World Health Organ. 998;76(1):25-32.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2305623
http://www.ncbi.nlm.nih.gov/pubmed/9615494?tool=bestpractice.com
[112]Bern C, Adler-Moore J, Berenguer J, et al. Liposomal amphotericin B for the treatment of visceral leishmaniasis. Clin Infect Dis. 2006 Oct 1;43(7):917-24.
http://cid.oxfordjournals.org/content/43/7/917.full
http://www.ncbi.nlm.nih.gov/pubmed/16941377?tool=bestpractice.com
ამფოტერიცინის დეზოქსიქოლატი მისაღები არჩევანია, თუ ლიპოსომური ფორმა ხელმისაწვდომი არ არის; გვერდითი ეფექტები მსგავსია, მაგრამ უფრო ხშირი და მძიმეა. ასევე შედარებით რთულია მიღება.[113]Olliaro PL, Guerin PJ, Gerstl S, et al. Treatment options for visceral leishmaniasis: a systematic review of clinical studies done in India, 1980-2004. Lancet Infect Dis. 2005 Dec;5(12):763-74.
http://www.ncbi.nlm.nih.gov/pubmed/16310148?tool=bestpractice.com
[114]Sundar S, Mehta H, Suresh AV, et al. Amphotericin B treatment for Indian visceral leishmaniasis: conventional versus lipid formulations. Clin Infect Dis. 2004 Feb 1;38(3):377-83.
http://cid.oxfordjournals.org/content/38/3/377.full
http://www.ncbi.nlm.nih.gov/pubmed/14727208?tool=bestpractice.com
ამფოტერიცინ B-ს სხვა ლიპიდური ფორმები (თუ ხელმისაწვდომია) ნაკლებადაა შესწავლილი და ჩამორჩება ლიპოსომურ ამფოტერიცინ-B ფორმას.[115]Yardley V, Croft SL. A comparison of the activities of three amphotericin B lipid formulations against experimental visceral and cutaneous leishmaniasis. Int J Antimicrob Agents. 2000 Feb;13(4):243-8.
http://www.ncbi.nlm.nih.gov/pubmed/10755238?tool=bestpractice.com
ამფოტერიცინი B არის ლეიშმანიოზის ერთადერთი სამკურნალო საშუალება, რომლის უსაფრთხოება დამტკიცებულია ორსულობის დროს.
მილტეფოზინი
მილტეფოზინი ლეიშმანიოზის საწინააღმდეგო ერთადერთი პერორალური მედიკამენტია.
მილტეფოზინის გამოყენების შეზღუდვებია:
ტერატოგენურობის მაღალი რისკი ორსულებში. ქალებს მოეთხოვებათ უარყოფითი ორსულობის ტესტი და ეფექტური კონტრაცეფცია მკურნალობის პერიოდში და მკურნალობის შემდეგ მინიმუმ 5 თვის განმავლობაში.
მნიშვნელოვანი გასტროინტესტინური არასასურველი ეფექტები მოიცავს გულისრევას, ღებინებასა და მუცლის ტკივილს
ბუნებრივი ან ახალი რეზისტენტობა ზოგიერთ რეგიონში.[116]Carnielli JBT, Crouch K, Forrester S, et al. A Leishmania infantum genetic marker associated with miltefosine treatment failure for visceral leishmaniasis. EBioMedicine. 2018 Oct;36:83-91.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6197651
http://www.ncbi.nlm.nih.gov/pubmed/30268832?tool=bestpractice.com
[117]Tiwary P, Kumar D, Sundar S. Identification and functional validation of a biomarker for the diagnosis of miltefosine relapse during visceral leishmaniasis. Am J Trop Med Hyg. 2018 Feb;98(2):492-6.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6197651
http://www.ncbi.nlm.nih.gov/pubmed/29280431?tool=bestpractice.com
მილტეფოზინი დამტკიცებულია აშშ-ში (მაგრამ არა ევროპაში) ჩამოთვლილი ჩვენებებით:
Leishmania donovani-ის მიერ გამოწვეული ვისცერული ლეიშმანიოზი
Leishmania braziliensis, Leishmania guyanensis და Leishmania panamensis-ის მიერ გამოწვეული კანის ლეიშმანიოზი.
Leishmania braziliensis-ის მიერ გამოწვეული ლორწოვანის ლეიშმანიოზი.
ხუთვალენტიანი ანტიმონიური პრეპარატები
სპეციფიკური მედიკამენტებია: ნატრიუმის სტიბოგლუკონატი და მეგლუმინის ანტიმონატი. ბრენდირებული პროდუქტები, როგორც წესი, უპირატესია, რადგან შემცველობა უფრო სანდოა და ნაკლებია ტოქსიკურობა.[121]Sundar S, Chakravarty J. Antimony toxicity. Int J Environ Res Public Health. 2010 Dec;7(12):4267-77.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3037053
http://www.ncbi.nlm.nih.gov/pubmed/21318007?tool=bestpractice.com
მიზნობრივი ეფექტურობა მნიშვნელოვნად განსხვავდება სხვადასხვა რეგიონებში, სამხრეთ აზიაში რეზისტენტობა ძალიან მაღალია.[122]Sundar S. Drug resistance in Indian visceral leishmaniasis. Trop Med Int Health. 2001 Nov;6(11):849-54.
https://onlinelibrary.wiley.com/doi/full/10.1046/j.1365-3156.2001.00778.x
http://www.ncbi.nlm.nih.gov/pubmed/11703838?tool=bestpractice.com
პარომომიცინი
პარომომიცინი ამინოგლიკოზიდია, რომელიც ტოპიკალურად გამოიყენება ლეიშმანიოზის კანის ფორმის დროს ან ინტრამუსკულარულად ვისცერული ფორმის დროს, ხშირად სხვა პრეპარატთან კომბინაციაში.
პარომიმიცინის კუნთშიდა და ტოპიკალური ფორმები დამტკიცებულია აშშ-სა და ევროპაში. აშშ-ში პერორალური ფორმა დამტკიცებულია სხვა ჩვენებებით და შეიძლება გამოყენებული იქნას ტოპიკალური მალამოების შემადგენლობაში, რაც არ არის დამტკიცებული.
ტოპიკალურად გამოყენების დროს პარომომიცინი იწვევს მსუბუქ-საშუალო სიმძიმის ადგილობრივ რეაქციებს, როგორიცაა სიწითლე, ტკივილი, შეშუპება, წვა, ქავილი. პარომომიცინის სისტემური არასასურველი ეფექტებია: ტკივილი ინექციის ადგილზე, მომატებული ამინოტრანსფერაზები, თირკმლის უკმარისობა, შექცევადი ოტოტოქსიკურობა.
ორსულებში პარომომიცინის უსაფრთხოების შესახებ მონაცემები არ არსებობს.
პენტამიდინი
როგორც წესი, გამოიყენება კანის ლეიშმანიოზის განსაკუთრებულ შემთხვევებში და მეორეული პროფილაქტიკის მიზნით იმუნოკომპრომისულ პაციენტებში.
პენდამიდინი ხელმისაწვდომია აშშ-ში, მაგრამ ლეიშმანიოზის დროს მისი გამოყენება დამტკიცებული არ არის. დამტკიცებულია ევროპაში კანის ლეიშმანიოზის სამკურნალოდ.
არასასურველი ეფექტები საყურადღებოა და მოიცავს შაქრიან დიაბეტს, პანკრეატიტს, გასტროინტესტინურ სიმპტომებს, ჰიპოტენზიას, QT ინტერვალის გახანგრძლივებას, ელექტროლიტების დარღვევებს, ნეფროტოქსიკურობას, ჰეპატოტოქსიკურობას, ციტოპენიებს და რაბდომიოლიზს. კანის ლეიშმანიოზის შემთხვევაში ეს ეფექტები მცირდება პრეპარატის შეყვანისას დაზიანების შიგნით.
არ არსებობს მონაცემები პენტამიდინის უსაფრთხოების თაობაზე ორსულებში.
სხვა მედიკამენტები, როგორიცაა აზოლური ფუნგიციდი, გამოიყენება კონკრეტულ შემთხვევებში.
კანის ლეიშმანიოზი: ზოგადი პრინციპები
კანის ლეიშმანიოზის დროს საჭიროა ინდივიდზე მორგებული მკურნალობის ტაქტიკა. ამერიკის ინფექციური დაავადებების საზოგადოების (IDSA)/ტროპიკული მედიცინის და ჰიგიენის ამერიკული საზოგადოების (ASTMH) გაიდლაინებით გამოიყოფა კანის ლეიშმანიოზის მარტივი და რთული (კომპლექსური) ფორმები.[8]Aronson N, Herwaldt BL, Libman M, et al. Diagnosis and treatment of leishmaniasis: clinical practice guidelines by the Infectious Diseases Society of America (IDSA) and the American Society of Tropical Medicine and Hygiene (ASTMH). Clin Infect Dis. 2016 Dec 15;63(12):1539-57.
https://academic.oup.com/cid/article/63/12/1539/2645617
http://www.ncbi.nlm.nih.gov/pubmed/27941143?tool=bestpractice.com
რესურსებით მდიდარ პირობებში, მართვის თაობაზე გადაწყვეტილების მისაღებად, ოპტიმალურია პარაზიტოლოგიური დიაგნოსტიკა პათოგენის იდენტიფიცირებით. მწირი რესურსების პირობებში შეძლებისდაგვარად უნდა ეცადოთ დიაგნოზის დადასტურებას, ვინაიდან მკურნალობას თან ახლავს მნიშვნელოვანი არასასურველი ეფექტები.[123]Croft SL, Yardley V. Chemotherapy of leishmaniasis. Curr Pharm Des. 2002;8(4):319-42.
http://www.ncbi.nlm.nih.gov/pubmed/11860369?tool=bestpractice.com
[124]Amato VS, Tuon FF, Siqueira AM, et al. Treatment of mucosal leishmaniasis in Latin America: systematic review. Am J Trop Med Hyg. 2007 Aug;77(2):266-74.
http://www.ncbi.nlm.nih.gov/pubmed/17690398?tool=bestpractice.com
[125]Oliveira LF, Schubach AO, Martins MM, et al. Systematic review of the adverse effects of cutaneous leishmaniasis treatment in the New World. Acta Tropica. 2011 May;118(2):87-96.
http://www.ncbi.nlm.nih.gov/pubmed/21420925?tool=bestpractice.com
თუ სახეობის განსაზღვრა ვერ ხერხდება, რეგიონული გავრცელების ("ძველი მსოფლიო" თუ "ახალი მსოფლიო") ცოდნა და ადგილობრივი გავრცელების სურათი შეიძლება დაგეხმაროთ მკურნალობის წარმართვაში. მაგალითად, კანის ლეიშმანიოზის მქონე პაციენტი, რომელიც ბოლივიის, ბრაზილიის და პერუს "ლორწოვანი სარტყელიდან" არის, შეიძლება იყოს ლორწოვანი გავრცელების უფრო მაღალი რისკის ქვეშ, ამიტომ კანის დაზიანებ(ებ)ის მართვის შემდეგ საჭიროა პაციენტის მონიტორინგი ლორწოვანი დაავადების განვითარებაზე, სახეობა-სპეციფიკური დიაგნოზის გარეშე.
კანის მარტივი ლეიშმანიოზი შეიძლება საჭიროებდეს მხოლოდ ფრთხილ დაკვირვებას, ან, განკურნების დასაჩქარებლად, შესაძლებელია მართვა ადგილობრივი თერაპიით ან აზოლური ფუნგიციდით. კანის რთული ლეიშმანიოზი, როგორც წესი, საჭიროებს სისტემურ თერაპიას ინვალიდობისა და სოციალური სტიგმის პრევენციისთვის და/ან პარაზიტის დისემინაციისა (მაგ., ლორწოვანის ლეიშმანიოზი) და რეციდივის თავიდან აცილების მიზნით.
კანის წყლულოვანი ლეიშმანიოზის ყველა შემთხვევაში საჭიროა ჭრილობის სათანადო დამუშავება - წყლულის მობანა და ბარიერული მალამოს გამოყენება. სითბოს, სიწითლის, ტკივილის და/ან ჩირქოვანი გამონადენის არსებობა საჭიროებს მეორეული ბაქტერიული ინფექციის სწრაფ შეფასებასა და მართვას. შეხორცება ხშირად იწყება წყლულების დაბრტყელებით. დიდი ზომის წყლულები მკურნალობის დასრულებისთვის შეიძლება არც შეხორცდეს.
CDC: parasites – leishmaniasis
Opens in new window
ქვემოთ ჩამოთვლილია სამკურნალო რეკომენდაციები კონკრეტული სიტუაციებისთვის; თუმცა, კანის ლეიშმანიოზის მკურნალობის შესახებ ჩატარებული კლინიკური კვლევების უმეტესობაში, არასათანადო დიზაინისა და გადმოცემის გამო, მკურნალობის პოტენციური სარგებლის შესახებ მტკიცებულება არასაკმარისია. საჭიროა დიდი, სწორად ჩატარებული კვლევები, რომლებიც შეაფასებენ არსებული თერაპიების გრძელვადიან ეფექტებს, კანის ლეიშმანიოზის რეციდივისა და მისი ლორწოვან დაავადებამდე პროგრესირების სიხშირეს.[126]Heras-Mosteiro J, Monge-Maillo B, Pinart M, et al. Interventions for Old World cutaneous leishmaniasis. Cochrane Database Syst Rev. 2017 Nov 17;11(11):CD005067.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD005067.pub4/full
http://www.ncbi.nlm.nih.gov/pubmed/29149474?tool=bestpractice.com
[127]Pinart M, Rueda JR, Romero GA, et al. Interventions for American cutaneous and mucocutaneous leishmaniasis. Cochrane Database Syst Rev. 2020 Aug 27;8(8):CD004834.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD004834.pub3/full
http://www.ncbi.nlm.nih.gov/pubmed/32853410?tool=bestpractice.com
კანის ლეიშმანიოზი: სპეციფიკური მკურნალობა
კანის მარტივი ლეიშმანიოზი
კანის მარტივი ლეიშმანიოზის დროს მისაღები ვარიანტებია: ფრთხილი დაკვირვება, ადგილობრივი თერაპიები, ნაკლებად ტოქსიკური სისტემური მედიკამენტები.
კანის ლეიშმანიოზის შემთხვევების უმეტესობა, განსაკუთრებით ძველი მსოფლიოს შტამების შემთხვევაში, სპონტანურად ალაგდება 18 თვის განმავლობაში; შესაბამისად, მნიშვნელოვანია გადაწყვეტა, არსებობს თუ არა მკურნალობის ჩვენება.[107]Burza S, Croft SL, Boelaert M. Leishmaniasis. Lancet. 2018 Sep 15;392(10151):951-70.
http://www.ncbi.nlm.nih.gov/pubmed/30126638?tool=bestpractice.com
[128]Morizot G, Kendjo E, Mouri O, et al. Travelers with cutaneous leishmaniasis cured without systemic therapy. Clin Infect Dis. 2013 Aug;57(3):370-80.
https://academic.oup.com/cid/article/57/3/370/461927
http://www.ncbi.nlm.nih.gov/pubmed/23633111?tool=bestpractice.com
გადაწყვეტილება ინდივიდუალურია, იმის გათვალისწინებით, დაწყებულია თუ არა შეხორცების პროცესი და ხომ არ არსებობს შეხორცების გაძნელება, მეორეული ინფექციების რისკი, ან დაქვეითებული უჯრედული იმუნიტეტი. ასევე მხედველობაში მისაღებია პაციენტის არჩევანი, მკურნალობის ხელმისაწვდომობა და შესაბამისი გამოცდილების ქონა.
ადგილობრივი თერაპიის ვარიანტებია: კრიოთერაპია, თერმოთერაპია და ტოპიკურად ან დაზიანების შიგნით მედიკამენტების გამოყენება. ადგილობრივი თერაპიის დაწყებამდე საჭიროა ფუფხის მოშორება (თუ ვლინდება).[8]Aronson N, Herwaldt BL, Libman M, et al. Diagnosis and treatment of leishmaniasis: clinical practice guidelines by the Infectious Diseases Society of America (IDSA) and the American Society of Tropical Medicine and Hygiene (ASTMH). Clin Infect Dis. 2016 Dec 15;63(12):1539-57.
https://academic.oup.com/cid/article/63/12/1539/2645617
http://www.ncbi.nlm.nih.gov/pubmed/27941143?tool=bestpractice.com
კრიოთერაპია: მოიცავს დაზიანების და მის გარშემო 1-2 მმ ჯანსაღი კანის მოყინვას თხევადი აზოტის გამოყენებით, სანამ დაზიანება არ გახდება თეთრი. დაზიანება ხელახლა უნდა მოიყინოს გალღობის შემდეგ. IDSA/ASTMH გაიდლაინებით რეკომენდებულია კრიოთერაპიის სესია ყოველ 3 კვირაში ერთხელ, ჯამში სამჯერ.[8]Aronson N, Herwaldt BL, Libman M, et al. Diagnosis and treatment of leishmaniasis: clinical practice guidelines by the Infectious Diseases Society of America (IDSA) and the American Society of Tropical Medicine and Hygiene (ASTMH). Clin Infect Dis. 2016 Dec 15;63(12):1539-57.
https://academic.oup.com/cid/article/63/12/1539/2645617
http://www.ncbi.nlm.nih.gov/pubmed/27941143?tool=bestpractice.com
კრიოთერაპიის მიზნობრივი ეფექტურობა თითოეულ დაზიანებაზე 67%-ია ყველა ზონაში და სტატისტიკურად ისეთივე ეფექტურია, როგორც დაზიანების-შიდა ანტიმონიური პრეპარატები.[129]López-Carvajal L, Cardona-Arias JA, Zapata-Cardona MI, et al. Efficacy of cryotherapy for the treatment of cutaneous leishmaniasis: meta-analyses of clinical trials. BMC Infect Dis. 2016 Jul 26;16:360.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4960741
http://www.ncbi.nlm.nih.gov/pubmed/27456008?tool=bestpractice.com
არასასურველი ეფექტებია: გარდამავალი ტკივილი და სიწითლე, ასევე ჰიპოპიგმენტაცია.
თერმოთერაპია: დაზიანებები სითბურად მუშავდება, ხშირად ერთჯერადად. იწვევს მეორე ხარისხის დამწვრობას და საჭიროებს ადგილობრივ ანესთეზიას. მეტა-ანალიზის თანახმად, მიზნობრივი ეფექტურობა 73%-ია ყველა ზონაში, ექვივალენტურია სისტემური ანტიმონიური თერაპიის, მაგრამ ნაკლები არასასურველი ეფექტებით.[130]Cardona-Arias JA, Vélez ID, López-Carvajal L. Efficacy of thermotherapy to treat cutaneous leishmaniasis: a meta-analysis of controlled clinical trials. 2015 May 26;10(5):e0122569.
https://journals.plos.org/plosone/article?id=10.1371/journal.pone.0122569
http://www.ncbi.nlm.nih.gov/pubmed/26009885?tool=bestpractice.com
მიზნობრივი ეფექტურობა უფრო მაღალი შეიძლება იყოს "ძველ მსოფლიოში", განკურნების სიხშირე Leishmania tropica-ს შემთხვევაში 94%-მდეა.[107]Burza S, Croft SL, Boelaert M. Leishmaniasis. Lancet. 2018 Sep 15;392(10151):951-70.
http://www.ncbi.nlm.nih.gov/pubmed/30126638?tool=bestpractice.com
არასასურველი ეფექტებია: ცელულიტი, სიწითლე, ტკივილი მკურნალობის ადგილას; აშშ გაიდლაინებით რეკომენდებულია ტოპიკური ანტიბიოტიკები პროცედურის შემდეგ, რამდენიმე დღის განმავლობაში.[8]Aronson N, Herwaldt BL, Libman M, et al. Diagnosis and treatment of leishmaniasis: clinical practice guidelines by the Infectious Diseases Society of America (IDSA) and the American Society of Tropical Medicine and Hygiene (ASTMH). Clin Infect Dis. 2016 Dec 15;63(12):1539-57.
https://academic.oup.com/cid/article/63/12/1539/2645617
http://www.ncbi.nlm.nih.gov/pubmed/27941143?tool=bestpractice.com
მკურნალობის ეს მეთოდი საჭიროებს სპეციალური მოწყობილობების მოხმარებას და ოპერატორების გადამზადებას, რის გამოც ფართოდ არ გამოიყენება.
ტოპიკური პარომომიცინი: ყველაზე მეტად შესწავლილი ტოპიკური მედიკამენტია კანის ლეიშმანიოზის სამკურნალოდ. მიზნობრივი ეფექტურობა ლიტერატურაში განსხვავდება ზუსტი ფორმის მიხედვით; ამიტომ კომერციული ვარიანტები და ნარევები შეიძლება არ იყოს მოცემულობასთან ექვივალენტური. პარომომიცინი შეიძლება გამოიყენოთ ცალკე ან კომბინაციაში მეთილბენზეთონიუმ ქლორიდთან, შარდოვანასთან ან გენტამიცინთან.[126]Heras-Mosteiro J, Monge-Maillo B, Pinart M, et al. Interventions for Old World cutaneous leishmaniasis. Cochrane Database Syst Rev. 2017 Nov 17;11(11):CD005067.
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD005067.pub4/full
http://www.ncbi.nlm.nih.gov/pubmed/29149474?tool=bestpractice.com
"ძველი მსოფლიოს" დაავადებების შემთხვევაში, წყლულოვანი Leishmania major-ის განკურნების სიხშირე დაახლოებით 80%-მდეა (გენტამიცინის დამატებით ან მის გარეშე), შედარებით 57%-თან პლაცებოს ჯგუფში.[131]Ben Salah A, Ben Messaoud N, Guedri E, et al. Topical paromomycin with or without gentamicin for cutaneous leishmaniasis. N Engl J Med. 2013 Feb 7;368(6):524-32.
http://www.ncbi.nlm.nih.gov/pubmed/23388004?tool=bestpractice.com
"ახალი მსოფლიოს" დაავადებების ორ კვლევაში, L panamensis, L guyanensis, ან L braziliensis პათოგენებით გამოწვეული დაზიანებების დროს პარომომიცინის მსგავს პროდუქტებს განკურნების სიხშირე 77%-79% ჰქონდა.[132]Sosa N, Pascale JM, Jiménez AI, et al. Topical paromomycin for New World cutaneous leishmaniasis. PLoS Negl Trop Dis. 2019 May 2;13(5):e0007253.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6497224
http://www.ncbi.nlm.nih.gov/pubmed/31048871?tool=bestpractice.com
[133]Soto J, Soto P, Ajata A, et al. Topical 15% paromomycin-aquaphilic for Bolivian Leishmania braziliensis cutaneous leishmaniasis: a randomized, placebo-controlled trial. Clin Infect Dis. 2019 Feb 15;68(5):844-9.
https://academic.oup.com/cid/article/68/5/844/5107841
http://www.ncbi.nlm.nih.gov/pubmed/30260376?tool=bestpractice.com
"ახალი მსოფლიოს" ძველმა კვლევებმა შედარებით დაბალი მიზნობრივი ეფექტურობა აჩვენა პარომომიცინის სხვადასხვა ფორმებისთვის (დაახლოებით 50%); ხოლო სისტემური ხუთვალენტიანი ანტიმონიური პრეპარატებით განკურნების სიხშირე (74%) ამ კვლევებში მსგავსი იყო უფრო ახალ კვლევებში აღწერილი ტოპიკური პარომომიცინის ეფექტურობისა.[134]Kim DH, Chung HJ, Bleys J, et al. Is paromomycin an effective and safe treatment against cutaneous leishmaniasis? A meta-analysis of 14 randomized controlled trials. PLoS Negl Trop Dis. 2009;3(2):e381.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2637543
http://www.ncbi.nlm.nih.gov/pubmed/19221595?tool=bestpractice.com
პანამაში ტოპიკური პარომომიცინით ნამკურნალებ პაციენტთა 3%-ს განუვითარდა ლორწოვანი დაავადება, რომელიც სისტემურ მკურნალობას საჭიროებდა.[132]Sosa N, Pascale JM, Jiménez AI, et al. Topical paromomycin for New World cutaneous leishmaniasis. PLoS Negl Trop Dis. 2019 May 2;13(5):e0007253.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6497224
http://www.ncbi.nlm.nih.gov/pubmed/31048871?tool=bestpractice.com
ლორწოვანი დაავადების რისკი Viannia-ს ქვესახეობის პარაზიტების ფონზე მაღალია და საჭიროა ინტენსიური მეთვალყურეობა, თუ არჩეულია ტოპიკური მკურნალობა და არა სისტემური თერაპია.
დაზიანების-შიდა თერაპია: გულისხმობს დაზიანების ინექციას ანტი-ლეიშმანიური მედიკამენტით, ყველაზე ხშირად ხუთვალენტიანი ანტიმონიური პრეპარატებით. ტკივილი ინექციის ადგილას შეიძლება იყოს ძლიერი. "ძველ მსოფლიოში" საუკეთესო შედეგები აღწერილია დაზიანების-შიდა ნატრიუმის სტიბოგლუკონატის და კრიოთერაპიის კომბინაციის შემთხვევაში, რომლის დროსაც განკურნების სიხშირე 89-91%-ია.[107]Burza S, Croft SL, Boelaert M. Leishmaniasis. Lancet. 2018 Sep 15;392(10151):951-70.
http://www.ncbi.nlm.nih.gov/pubmed/30126638?tool=bestpractice.com
მიუხედავად იმისა, რომ "ახალ მსოფლიოში" ნაკლებად მყარი მტკიცებულებები არსებობს და ლორწოვანი ლეიშმანიოზი რჩება საფრთხედ, მეტა-ანალიზის თანახმად ჯამური მიზნობრივი ეფექტურობა არის 75%, მაგრამ მეგლუმინ ანტიმონატი უფრო ეფექტურია (82%), ვიდრე ნატრიუმის სტიბოგლუკონატი, რომელიც "ძველ მსოფლიოში" გამოიყენება.[135]Brito NC, Rabello A, Cota GF. Efficacy of pentavalent antimoniate intralesional infiltration therapy for cutaneous leishmaniasis: a systematic review. PLoS One. 2017 Sep 19;12(9):e0184777.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5604971
http://www.ncbi.nlm.nih.gov/pubmed/28926630?tool=bestpractice.com
ნატრიუმის სტიბოგლუკონატი ხელმისაწვდომია ევროპაში დაზიანების-შიდა გამოყენებისთვის, მაგრამ არ არის ხელმისაწვდომი აშშ-ში. დაზიანების შიგნით ასევე შეიძლება გამოვიყენოთ პენტამიდინი.[136]Soto J, Paz D, Rivero D, et al. Intralesional pentamidine: a novel therapy for single lesions of Bolivian cutaneous leishmaniasis. Am J Trop Med Hyg. 2016 Apr;94(4):852-6.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4824229
http://www.ncbi.nlm.nih.gov/pubmed/26903605?tool=bestpractice.com
ადგილობრივი მკურნალობის ალტერნატივაა ისეთი მეთოდები, როგორიცაა ფოტოდინამიური ან CO₂ ლაზერით თერაპია, მაგრამ მტკიცებულება მწირია რეკომენდაციების გასაცემად.[Figure caption and citation for the preceding image starts]: კანის ლეიშმანიოზის მკურნალობა, დაზიანების-შიდა ინექციასურათი ეკუთვნის ჯანმრთელობის მსოფლიო ორგანიზაციას [Citation ends].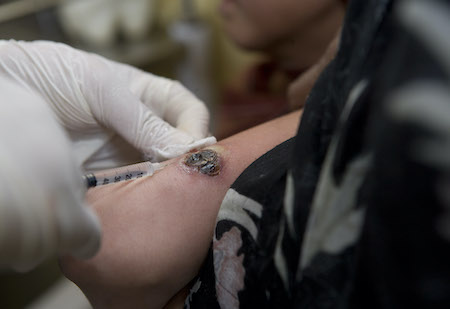
ზოგადად, სისტემური თერაპია გამოიყენება მხოლოდ კომპლექსურ შემთხვევებში, მაგრამ აზოლური ფუნგიციდი ასევე განიხილება კანის მარტივი ლეიშმანიოზის დროს.
ფლუკონაზოლი, იტრაკონაზოლი და კეტოკონაზოლი შეფასებულია და ხელმისაწვდომია გლობალურად, თუმცა კანის ლეიშმანიოზის დროს მისი გამოიყენება აშშ-სა და ევროპაში დამტკიცებული არ არის.
ყველა მათგანს ახასიათებს არასასურველი ეფექტები კუჭ-ნაწლავის მხრივ და ჰეპატოტოქსიკურობის რისკი, მაგრამ კეტოკონაზოლის შემთხვევაში განსაკუთრებული სიფრთხილეა საჭიროა სიცოცხლისათვის საშიში ჰეპატოტოქსიკურობისა და QT ინტერვალის გახანგრძლივების (ფატალური არითმიებით) რისკის გამო.
სისტემური მიმოხილვით არ გამოვლინდა საკმარისი მტკიცებულება აზოლის ფუნგიციდის რუტინულ მომხარებაზე რეკომენდაციის გასაცემად, მაგრამ "ახალ მსოფლიოში" კეტოკონაზოლის ჯამურმა მიზნობრივმა ეფექტურობამ Leishmania mexicana-ს შემთხვევაში მიაღწია 89%-ს, ამიტომ ეს მისაღები ვარიანტია მექსიკაში და ცენტრალური ამერიკის გარკვეულ ნაწილებში, არასასურველი ეფექტების შესაბამისი მონიტორინგით.[137]Galvão EL, Rabello A, Cota GF. Efficacy of azole therapy for tegumentary leishmaniasis: a systematic review and meta-analysis. PLoS One. 2017 Oct 9;12(10):e0186117.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5633178
http://www.ncbi.nlm.nih.gov/pubmed/29016694?tool=bestpractice.com
კანის რთული (კომპლექსური) ლეიშმანიოზი
კანის რთული ლეიშმანიოზის დროს სისტემური თერაპია უპირატესია დაზიანებ(ებ)ის სიდიდისა და მდებარეობის, ადგილობრივი თერაპიის წარუმატებლობის და/ან გავრცელების რისკის გათვალისწინებით.
მილტეფოზინი: შედარებით ახალი ვარიანტი კანის ლეიშმანიოზის დროს. დამტკიცებულია Viannia-ს ქვესახეობის პარაზიტებისთვის "ახალ მსოფლიოში", მაგრამ ამ კონტექსტშიც კი განსხვავება თვალსაჩინოა რეგიონების მიხედვით. განკურნების სიხშირე ბრაზილიაში, ბოლივიასა და კოლუმბიაში მერყეობს 71%-დან 91%-მდე Viannia-ს შემთხვევაში; გვატემალაში განკურნების სიხშირე მხოლოდ 33% იყო L brazilensis-ის დროს.[138]Chakravarty J, Sundar S. Current and emerging medications for the treatment of leishmaniasis. Expert Opin Pharmacother. 2019 Jul;20(10):1251-65.
http://www.ncbi.nlm.nih.gov/pubmed/31063412?tool=bestpractice.com
ხუთვალენტიანი ანტიმონიური ნაერთები (ნატრიუმის სტიბოგლუკონატი, მეგლუმინის ანტიმონატი): ზოგადად ეფექტურია, მაგრამ ნაკლებად მისაღებია ტოქსიკურობისა და მკურნალობის ხანგრძლივობის გამო. "ძველ მსოფლიოში" განკურნების სიხშირე 98%-მდეა L major-ის დროს და 41%-მდეა L tropica-ს შემთხვევაში. "ახალ მსოფლიოში" ეფექტურობა მერყეობს 77%-დან 90%-მდე, მაგრამ წარუმატებელი მკურნალობა საკმაოდ ხშირია Viannia-ს ქვესახეობის პარაზიტებში, განსაკუთრებით L brazilensis-ის შემთხვევაში, ასევე გარკვეულ გეოგრაფიულ რეგიონებში, როგორიცაა L mexicana გვატემალაში და პერუ/ბოლივიას საზღვარზე, სამხრეთ რეგიონებში.[138]Chakravarty J, Sundar S. Current and emerging medications for the treatment of leishmaniasis. Expert Opin Pharmacother. 2019 Jul;20(10):1251-65.
http://www.ncbi.nlm.nih.gov/pubmed/31063412?tool=bestpractice.com
ლიპოსომური ამფოტერიცინი-B: კანის რთული ლეიშმანიოზის დროს მოსალოდნელია მისი ეფექტურობა, მაგრამ მონაცემები მწირია და ეფუძნება ობსერვაციულ კვლევებს და რამდენიმე მცირე კლინიკურ კვლევას. რეტროსპექტული მონაცემების მიხედვით, სხვადასხვა მდებარეობის მიხედვით განკურნების სიხშირე 46-დან 84%-მდე მერყეობს, მაგრამ ბოლივიაში ჩატარებული მცირე კლინიკური კვლევების თანახმად, მაჩვენებლები 85-100%-ია.[138]Chakravarty J, Sundar S. Current and emerging medications for the treatment of leishmaniasis. Expert Opin Pharmacother. 2019 Jul;20(10):1251-65.
http://www.ncbi.nlm.nih.gov/pubmed/31063412?tool=bestpractice.com
პენტამიდინი: საფრანგეთის გვიანასა და სურინამში, L guyanensis-ით გამოწვეული "ახალი მსოფლიოს" კანის ლეიშმანიოზის მკურნალობაში მისი როლი შეზღუდულია. განკურნების სიხშირე 84-90%-ია.[139]Roussel M, Nacher M, Frémont G, et al. Comparison between one and two injections of pentamidine isethionate, at 7 mg/kg in each injection, in the treatment of cutaneous leishmaniasis in French Guiana. Ann Trop Med Parasitol. 2006 Jun;100(4):307-14.
http://www.ncbi.nlm.nih.gov/pubmed/16762111?tool=bestpractice.com
[140]Lai A Fat EJ, Vrede MA, Soetosenojo RM, et al. Pentamidine, the drug of choice for the treatment of cutaneous leishmaniasis in Surinam. Int J Dermatol. 2002 Nov;41(11):796-800.
http://www.ncbi.nlm.nih.gov/pubmed/12453009?tool=bestpractice.com
ინტრავენური გზა უპირატესია კუნთში ინექციასთან შედარებით, რადგან მიზნობრივი ეფექტურობა უფრო მაღალია (85% ინტრავენური გზის შემთხვევაში და 51% კუნთში შეყვანისას).[141]Christen JR, Bourreau E, Demar M, et al. Use of the intramuscular route to administer pentamidine isethionate in Leishmania guyanensis cutaneous leishmaniasis increases the risk of treatment failure. Travel Med Infect Dis. 2018 Jul - Aug;24:31-6.
http://www.ncbi.nlm.nih.gov/pubmed/29482012?tool=bestpractice.com
პენტამიდინის გამოყენების კიდევ ერთი პოტენციური გზა არის დაზიანების შიგნით შეყვანა, რომლის მიზნობრივი ეფექტურობა ბოლივიაში 73% იყო, მაგრამ ამ მეთოდმა შესაძლოა გავლენა ვერ იქონიოს ლორწოვანზე გავრცელების რისკზე.[136]Soto J, Paz D, Rivero D, et al. Intralesional pentamidine: a novel therapy for single lesions of Bolivian cutaneous leishmaniasis. Am J Trop Med Hyg. 2016 Apr;94(4):852-6.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4824229
http://www.ncbi.nlm.nih.gov/pubmed/26903605?tool=bestpractice.com
თუმცა, იმავე რეჟიმის კომბინაცია მილტეფოზინის 28 დღიან კურსთან იძლევა 92%-იან განკურნების მაჩვენებელს და გააჩნია სისტემური მკურნალობის უპირატესობა, მიუხედავად დიდი ხანგრძლივობისა და მაღალი ღირებულების.[142]Soto J, Soto P, Ajata A, et al. Miltefosine combined with intralesional pentamidine for Leishmania braziliensis cutaneous leishmaniasis in Bolivia. Am J Trop Med Hyg. 2018 Nov;99(5):1153-5.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6221230
http://www.ncbi.nlm.nih.gov/pubmed/30255833?tool=bestpractice.com
სხვა პირობებში, პენტამიდინის არასასურველი ეფექტები და შედარებით დაბალი მიზნობრივი ეფექტურობა, როგორც წესი, გამორიცხავს მის გამოყენებას. ეს შეიძლება ნაწილობრივ გამოწვეული იყოს მარილზე (ისეთიონატზე) დაფუძნებული დოზის ნაკლებობით, ბაზასთან შედარებით.[143]Dorlo TP, Kager PA. Pentamidine dosage: a base/salt confusion. PLoS Negl Trop Dis. 2008 May 28;2(5):e225.
https://www.doi.org/10.1371/journal.pntd.0000225
http://www.ncbi.nlm.nih.gov/pubmed/18509543?tool=bestpractice.com
კანის ლეიშმანიოზის სხვა კომპლექსური ფორმების მკურნალობა, როგორიცაა დისემინირებული ლეიშმანიოზი, კანის დიფუზური ლეიშმანიოზი და leishmaniasis recidivans, უნდა იმართოს ექსპერტების ხელმძღვანელობით, რადგან მკურნალობა რთულია და მონაცემები მწირია.
ლიპოსომური ამფოტერიცინი-B წარმატებით გამოიყენება დისემინირებული ლეიშმანიოზის დროს (განკურნების სიხშირე 75%).[144]Machado PR, Rosa ME, Guimarães LH, et al. Treatment of disseminated leishmaniasis with liposomal amphotericin B. Clin Infect Dis. 2015 Sep 15;61(6):945-9.
https://academic.oup.com/cid/article/61/6/945/450907
http://www.ncbi.nlm.nih.gov/pubmed/26048961?tool=bestpractice.com
კანის დიფუზური ლეიშმანიოზის შემთხვევაში ჯანმრთელობის პანამერიკული ორგანიზაცია რეკომენდაციას უწევს რეფერალურ ცენტრში მკურნალობას და შემდეგი პრეპარატების გამოყენებას: ხუთვალენტიანი ანიმონიური ნაერთები, პენტამიდინი, ან მილტეფოზინი.[145]Pan American Health Organization. Guideline for the treatment of Leishmaniasis in the Americas. Second edition. Sep 2022 [internet publication].
https://iris.paho.org/handle/10665.2/56120
თუმცა, ასეთ პაციენტებში განკურნების მიღწევა შესაძლოა რთული იყოს.
Leishmaniasis recidivan-ის მკურნალობა განსაკუთრებით რთულია.[8]Aronson N, Herwaldt BL, Libman M, et al. Diagnosis and treatment of leishmaniasis: clinical practice guidelines by the Infectious Diseases Society of America (IDSA) and the American Society of Tropical Medicine and Hygiene (ASTMH). Clin Infect Dis. 2016 Dec 15;63(12):1539-57.
https://academic.oup.com/cid/article/63/12/1539/2645617
http://www.ncbi.nlm.nih.gov/pubmed/27941143?tool=bestpractice.com
შესაძლო რეჟიმი მოიცავს ხუთვალენტიანი ანტიმონიური პრეპარატის და ალოპურინოლის კომბინაციას 30 დღის განმავლობაში.[146]Esfandiarpour I, Dabiri SH. Treatment of cutaneous leishmaniasis recidivans with a combination of allopurinol and meglumine antimoniate: a clinical and histologic study. Int J Dermatol. 2007 Aug;46(8):848-52.
http://www.ncbi.nlm.nih.gov/pubmed/17651170?tool=bestpractice.com
ხშირად გამოიყენება ლიპოსომური ამფოტერიცინი და მილტეფოზინი.
ორსული პაციენტები
კანის მარტივი და რთული ლეიშმანიოზის მკურნალობა ორსულ პაციენტებში ძალიან ინდივიდუალურია. თუ შესაძლებელია, მკურნალობა უნდა გადაიდოს ორსულობის დასრულებამდე, ეგზოფიტური დაზიანებების შემთხვევაშიც კი; თუმცა, მკურნალობის გარეშე შესაძლებელია მომატებული იყოს ნაადრევი მშობიარობის ან მკვდრადშობადობის რისკი.[147]Morgan DJ, Guimaraes LH, Machado PR, et al. Cutaneous leishmaniasis during pregnancy: exuberant lesions and potential fetal complications. Clin Infect Dis. 2007 Aug 15;45(4):478-82.
https://academic.oup.com/cid/article/45/4/478/426772
http://www.ncbi.nlm.nih.gov/pubmed/17638198?tool=bestpractice.com
თაგვებში ჩატარებული კვლევების საფუძველზე არსებობს კანის ლეიშმანიოზის ტრანსპლაცენტური გადაცემის თეორიული რისკი, მაგრამ ადამიანებში აღწერილი არ არის.[148]Avila-García M, Mancilla-Ramírez J, Segura-Cervantes E, et al. Transplacental transmission of cutaneous Leishmania mexicana strain in BALB/c mice. Am J Trop Med Hyg. 2013 Aug;89(2):354-8.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3741259
http://www.ncbi.nlm.nih.gov/pubmed/23798582?tool=bestpractice.com
ადგილობრივი თერაპია, როგორც წესი, უპირატესია სისტემურ მკურნალობასთან შედარებით. გასათვალისწინებელია, რომ დაზიანების-შიდა მედიკამენტის გამოყენებისას პრეპარატი შეიძლება სისტემურადაც გავრცელდეს.
ამფოტერიცინი-B უპირატესი აგენტია სისტემური თერაპიის საჭიროების შემთხვევაში, რადგან სხვა შესაძლო ვარიანტებთან შედარებით უსაფრთხოა.
ხუთვალენტიანი ანტიმონიური პრეპარატები ატარებს სპონტანური აბორტის და ნაადრევი მშობიარობის რისკს, რის გამოც ორსულობის დროს არ გამოიყენება.
ლორწოვანის ლეიშმანიოზი
ლორწოვანი ლეიშმანიოზის მქონე პაციენტებში ყოველთვის მოწოდებულია სისტემური მკურნალობა. მონაცემები მწირია და მკურნალობის მიზნობრივი ეფექტურობა განსხვავდება, რის გამოც საჭიროა ინდივიდუალური მიდგომა. თერაპიის შესაძლო ვარიანტებია: ხუთვალენტიანი ანტიმონიური პრეპარატები, ამფოტერიცინი-B, მილტეფოზინი და პენტამიდინი. ჯანმრთელობის პანამერიკული ორგანიზაციის კლასიფიკაციით, ყველა ამ მედიკამენტის შესახებ არსებული მტკიცებულება არის სუსტი ან ძალიან სუსტი, ხოლო ყველაზე ძლიერ რეკომენდაციას გასცემს ხუთვალენტიან ანტიმონიურ პრეპარატებზე.[145]Pan American Health Organization. Guideline for the treatment of Leishmaniasis in the Americas. Second edition. Sep 2022 [internet publication].
https://iris.paho.org/handle/10665.2/56120
[149]Pan American Health Organization. Manual of procedures for leishmaniases surveillance and control in the Americas. Dec 2019 [internet publication].
https://iris.paho.org/handle/10665.2/51838
აშშ-ის გაიდლაინები არ არის სტრატიფიცირებული ალტერნატივებს შორის, გარდა პენტამიდინის კლასიფიკაციისა, როგორც ნაკლებად ალტერნატიული.[8]Aronson N, Herwaldt BL, Libman M, et al. Diagnosis and treatment of leishmaniasis: clinical practice guidelines by the Infectious Diseases Society of America (IDSA) and the American Society of Tropical Medicine and Hygiene (ASTMH). Clin Infect Dis. 2016 Dec 15;63(12):1539-57.
https://academic.oup.com/cid/article/63/12/1539/2645617
http://www.ncbi.nlm.nih.gov/pubmed/27941143?tool=bestpractice.com
ხუთვალენტიანი ანტიმონიური პრეპარატები არჩევის პრეპარატია პაციენტებში, რომელთაც ამ კურსის კარგი ამტანობა აქვთ. მიზნობრივი ეფექტურობა ვარირებს 58%-დან (ნატრიუმის სტიბოგლუკონატთან კომბინაციაში) 88%-მდე (მეგლუმინის ანტიმონატთან კომბინაციაში). ზოგიერთი კვლევით დამატებულია დამხმარე საშუალებები, როგორებიცაა პენტოქსიფილინი ან ინტერფერონ-გამა, მაგრამ ამასთან დაკავშირებით მტკიცებულება სუსტია.[124]Amato VS, Tuon FF, Siqueira AM, et al. Treatment of mucosal leishmaniasis in Latin America: systematic review. Am J Trop Med Hyg. 2007 Aug;77(2):266-74.
http://www.ncbi.nlm.nih.gov/pubmed/17690398?tool=bestpractice.com
ამფოტერიცინ-B-ს სხვადასხვა ფორმა მისაღები ალტერნატივაა, განსაკუთრებით თუ მკურნალობა წარუმატებელია, ვითარდება რეციდივი, ან ანტიმონიური პრეპარატების აუტანლობა. ლიპოსომურ ამფოტერიცინ-B-ზე მონაცემები ნაკლებია, მაგრამ თუკი ხელმისაწვდომია, მისი გამოყენება მოწოდებულია უსაფრთხოებისა და ადვილად ამტანობის გამო.[8]Aronson N, Herwaldt BL, Libman M, et al. Diagnosis and treatment of leishmaniasis: clinical practice guidelines by the Infectious Diseases Society of America (IDSA) and the American Society of Tropical Medicine and Hygiene (ASTMH). Clin Infect Dis. 2016 Dec 15;63(12):1539-57.
https://academic.oup.com/cid/article/63/12/1539/2645617
http://www.ncbi.nlm.nih.gov/pubmed/27941143?tool=bestpractice.com
ბრაზილიაში რეტროსპექტულად აღწერილი შემთხვევათა სერიის თანახმად, ლიპოსომური ამფოტერიცინი-B-ს გამოყენებისას განკურნების სიხშირე 93% იყო.[150]Cunha MA, Leão AC, de Cassia Soler R, et al. Efficacy and safety of liposomal amphotericin B for the treatment of mucosal leishmaniasis from the New World: a retrospective study. Am J Trop Med Hyg. 2015 Dec;93(6):1214-8.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4674237
http://www.ncbi.nlm.nih.gov/pubmed/26483120?tool=bestpractice.com
თუ აღნიშნული მკურნალობა წარუმატებელია, დასაშვებია მილტეფოზინის გამოყენება, მაგრამ განკურნების სიხშირე დაბალია, გარდა კლინიკურად მსუბუქი ფორმებისა.[151]Soto J, Toledo J, Valda L, et al. Treatment of Bolivian mucosal leishmaniasis with miltefosine. Clin Infect Dis. 2007 Feb 1;44(3):350-6.
https://academic.oup.com/cid/article/44/3/350/312370
http://www.ncbi.nlm.nih.gov/pubmed/17205440?tool=bestpractice.com
ორსული პაციენტები
ვისცერული ლეიშმანიოზი: ზოგადი პრინციპები
მკურნალობის მთავარი ამოცანაა სიკვდილის თავიდან აცილება და ხანგრძლივი კლინიკური განკურნების მიღწევა. უმეტეს შემთხვევაში, პარაზიტის ერადიკაცია ნაკლებად მოსალოდნელია, რასაც ადასტურებს პაციენტთა მნიშვნელოვან ნაწილში, საწყისი კლინიკური განკურნებიდან წლების შემდეგ, მაღალმგრძნობიარე მეთოდებით (მაგ., PCR-ით) დადგენილი დაავადების რეაქტივაცია და პარაზიტის მკურნალობის შემდგომი პერსისტირება.[82]Cruz I, Chicharro C, Nieto J, et al. Comparison of new diagnostic tools for management of pediatric Mediterranean visceral leishmaniasis. J Clin Microbiol. 2006 Jul;44(7):2343-7.
https://journals.asm.org/doi/10.1128/JCM.02297-05?url_ver=Z39.88-2003
http://www.ncbi.nlm.nih.gov/pubmed/16825347?tool=bestpractice.com
[152]Osman OF, Oskam L, Zijlstra EE, et al. Use of the polymerase chain reaction to assess the success of visceral leishmaniasis treatment. Trans R Soc Trop Med Hyg. 1998 Jul-Aug;92(4):397-400.
http://www.ncbi.nlm.nih.gov/pubmed/9850390?tool=bestpractice.com
კანის ლეიშმანიოზის დროს, მკურნალობის კურსის შერჩევისას, გასათვალისწინებელია პარაზიტული (რომლებიც ხშირად უკავშირდება სახეობას და/ან გეოგრაფიულ რეგიონს), ისევე როგორც, მასპინძლის ფაქტორები . სიმპტომური დაავადების მქონე ყველა პაციენტს უნდა ჩაუტარდეს მკურნალობა. უცნობია, ლატენტური ვისცერული ლეიშმანიოზის მკურნალობა ახდენს თუ არა სიმპტომური დაავადების პრევენციას, ამიტომ, არსებული მეთოდების ტოქსიკურობის გათვალისწინებით, მკურნალობა არ არის რეკომენდებული.
ლეიშმანიოზის მკურნალობის გარდა, მართვა უნდა ითვალისწინებდეს ისეთ ხშირ გართულებებს, როგორებიცაა სითხის მოცულობის შემცირება, მალნუტრიცია, ანემია და თანდართული ბაქტერიული ინფექცია (მაგ., პნევმონია) ან პარაზიტული ინფექციები (მაგ., მალარია).
ვისცერული ლეიშმანიოზი: მკურნალობა იმუნოკომპეტენტურ პაციენტებში
ამფოტერიცინ-B-ს ფორმები
აღმოსავლეთ აფრიკის გარეთ, ლიპოსომური ამფოტერიცინი-B არჩევის პრეპარატია, კლინიკური განკურნება >90%-ში აღინიშნება სხვადასხვა რეჟიმის გამოყენებისას.[8]Aronson N, Herwaldt BL, Libman M, et al. Diagnosis and treatment of leishmaniasis: clinical practice guidelines by the Infectious Diseases Society of America (IDSA) and the American Society of Tropical Medicine and Hygiene (ASTMH). Clin Infect Dis. 2016 Dec 15;63(12):1539-57.
https://academic.oup.com/cid/article/63/12/1539/2645617
http://www.ncbi.nlm.nih.gov/pubmed/27941143?tool=bestpractice.com
[107]Burza S, Croft SL, Boelaert M. Leishmaniasis. Lancet. 2018 Sep 15;392(10151):951-70.
http://www.ncbi.nlm.nih.gov/pubmed/30126638?tool=bestpractice.com
[138]Chakravarty J, Sundar S. Current and emerging medications for the treatment of leishmaniasis. Expert Opin Pharmacother. 2019 Jul;20(10):1251-65.
http://www.ncbi.nlm.nih.gov/pubmed/31063412?tool=bestpractice.com
ინდოეთში, L donovani-ს შემთხვევაში, ლიპოსომური ამფოტერიცინი-B აჩვენებს უსაფრთხოების კარგ პროფილს და ხასიათდება 96%-იანი განკურნებით კლინიკურ კვლევებში.[153]Sundar S, Chakravarty J, Agarwal D, et al. Single-dose liposomal amphotericin B for visceral leishmaniasis in India. N Engl J Med. 2010 Feb 11;362(6):504-12.
https://www.doi.org/10.1056/NEJMoa0903627
http://www.ncbi.nlm.nih.gov/pubmed/20147716?tool=bestpractice.com
შემდგომი კვლევების თანახმად, რომლებშიც მონაწილეობდა სამხრეთ აზიაში ლიპოსომური ამფოტერიცინი B-თი ნამკურნალები 2500-ზე მეტი პაციენტი, მიზნობრივი ეფექტურობა მსგავსია ან უფრო მაღალი.[154]Lucero E, Collin SM, Gomes S, et al. Effectiveness and safety of short course liposomal amphotericin B (AmBisome) as first line treatment for visceral leishmaniasis in Bangladesh. PLoS Negl Trop Dis. 2015 Apr 2;9(4):e0003699.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4383421
http://www.ncbi.nlm.nih.gov/pubmed/25837313?tool=bestpractice.com
[155]Goswami RP, Goswami RP, Das S, et al. Short-course treatment regimen of Indian visceral leishmaniasis with an Indian liposomal amphotericin B preparation (Fungisome™). Am J Trop Med Hyg. 2016 Jan;94(1):93-8.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4710453
http://www.ncbi.nlm.nih.gov/pubmed/26526926?tool=bestpractice.com
[156]Pandey K, Pal B, Siddiqui NA, et al. Efficacy and safety of liposomal amphotericin B for visceral leishmaniasis in children and adolescents at a tertiary care center in Bihar, India. Am J Trop Med Hyg. 2017 Nov;97(5):1498-502.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5817748
http://www.ncbi.nlm.nih.gov/pubmed/29016288?tool=bestpractice.com
[157]Rahman R, Goyal V, Haque R, et al. Safety and efficacy of short course combination regimens with AmBisome, miltefosine and paromomycin for the treatment of visceral leishmaniasis (VL) in Bangladesh. PLoS Negl Trop Dis. 2017 May 30;11(5):e0005635.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5466346
http://www.ncbi.nlm.nih.gov/pubmed/28558062?tool=bestpractice.com
[158]Goyal V, Mahajan R, Pandey K, et al. Field safety and effectiveness of new visceral leishmaniasis treatment regimens within public health facilities in Bihar, India. PLoS Negl Trop Dis. 2018 Oct 22;12(10):e0006830.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6197645
http://www.ncbi.nlm.nih.gov/pubmed/30346949?tool=bestpractice.com
აღმოსავლეთ აფრიკაში, ლიპოსომური ამფოტერიცინ-B-ის მაღალი დოზები საჭიროა L donovani-ს სამკურნალოდ. განკურნების სიხშირე >90%-ია, თუმცა პაციენტების უმეტესობა კომპლექსურია (მაგ., ორსულობა, რეციდივი, შორსწასული დაავადება, მცირეწლოვანი/ხანდაზმული ასაკობრივი ჯგუფები).[159]Copeland NK, Aronson NE. Leishmaniasis: treatment updates and clinical practice guidelines review. Curr Opin Infect Dis. 2015 Oct;28(5):426-37.
http://www.ncbi.nlm.nih.gov/pubmed/26312442?tool=bestpractice.com
[160]Gebreyohannes EA, Bhagvathula AS, Abegaz TM, et al. Treatment outcomes of visceral leishmaniasis in Ethiopia from 2001 to 2017: a systematic review and meta-analysis. Infect Dis Poverty. 2018 Oct 19;7(1):108.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6194743
http://www.ncbi.nlm.nih.gov/pubmed/30340519?tool=bestpractice.com
Leishmania infantum (იგივე Leishmania chagasi) ასევე ექვემდებარება მკურნალობას ლიპოსომური ამფოტერიცინი-B-ით.[138]Chakravarty J, Sundar S. Current and emerging medications for the treatment of leishmaniasis. Expert Opin Pharmacother. 2019 Jul;20(10):1251-65.
http://www.ncbi.nlm.nih.gov/pubmed/31063412?tool=bestpractice.com
მიზნობრივი ეფექტურობის შესახებ მონაცემების უმეტესობა ეფუძნება ხმელთაშუა ზღვის რეგიონში ჩატარებულ კვლევებს, მაგრამ ერთ-ერთი ბრაზილიური კვლევა მხარს უჭერს ლიპოსომური ამფოტერიცინის გამოყენებას ხუთვალენტიანი ანტიმონიური პრეპარატების ნაცვლად. მოდელირების თანახმად, ეს მიდგომა უფრო ხარჯთეფექტურია.[161]Romero GAS, Costa DL, Costa CHN, et al. Efficacy and safety of available treatments for visceral leishmaniasis in Brazil: a multicenter, randomized, open label trial. PLoS Negl Trop Dis. 2017 Jun 29;11(6):e0005706.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5507560
http://www.ncbi.nlm.nih.gov/pubmed/28662034?tool=bestpractice.com
[162]Assis TSM, Rabello A, Cota G, et al. Cost-effectiveness analysis of diagnostic-therapeutic strategies for visceral leishmaniasis in Brazil. Rev Soc Bras Med Trop. 2019 Apr 11;52:e20180272.
http://www.scielo.br/scielo.php?script=sci_arttext&pid=S0037-86822019000100638&lng=en&nrm=iso&tlng=en
http://www.ncbi.nlm.nih.gov/pubmed/30994802?tool=bestpractice.com
კომბინირებული თერაპია
ხუთვალენტიანი ანტიმონიური ნაერთების და პარომომიცინის კომბინაცია მაღალეფექტურია L donovani-ით გამოწვეული ვისცერული ლეიშმანიოზის დროს აღმოსავლეთ აფრიკაში; განკურნების სიხშირე არის 90-95%.[160]Gebreyohannes EA, Bhagvathula AS, Abegaz TM, et al. Treatment outcomes of visceral leishmaniasis in Ethiopia from 2001 to 2017: a systematic review and meta-analysis. Infect Dis Poverty. 2018 Oct 19;7(1):108.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6194743
http://www.ncbi.nlm.nih.gov/pubmed/30340519?tool=bestpractice.com
[163]Kimutai R, Musa AM, Njoroge S, et al. Safety and effectiveness of sodium stibogluconate and paromomycin combination for the treatment of visceral leishmaniasis in eastern Africa: results from a pharmacovigilance programme. Clin Drug Investig. 2017 Mar;37(3):259-72.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5315726
http://www.ncbi.nlm.nih.gov/pubmed/28066878?tool=bestpractice.com
მედიკამენტთა აღნიშნული კომბინაცია არ უნდა გამოიყენოთ >50 წლის პაციენტებში ან აივ-ინფიცირებულებში, რადგან განკურნების სიხშირე შემცირებულია და შეადგენს 81%-ს და 56%-ს, შესაბამისად.[163]Kimutai R, Musa AM, Njoroge S, et al. Safety and effectiveness of sodium stibogluconate and paromomycin combination for the treatment of visceral leishmaniasis in eastern Africa: results from a pharmacovigilance programme. Clin Drug Investig. 2017 Mar;37(3):259-72.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5315726
http://www.ncbi.nlm.nih.gov/pubmed/28066878?tool=bestpractice.com
იმის გამო, რომ პარენტერული პარომომიცინი არ არის ხელმისაწვდომი ევროპაში ან აშშ-ში, უჩვეულოა ამ რეჟიმის გამოყენება აღმოსავლეთ აფრიკის გარეთ.
სამხრეთ აზიაში ლიპოსომური ამფოტერიცინი B-ს კომბინაცია მილტეფოზინის და/ან პარომომიცინის მოკლე კურსთან, ან მიტეფოზინი პარომომიცინთან ერთად, მაღალეფექტური ალტერნატივაა ამფოტერიცინ-B-სთან შედარებით.[157]Rahman R, Goyal V, Haque R, et al. Safety and efficacy of short course combination regimens with AmBisome, miltefosine and paromomycin for the treatment of visceral leishmaniasis (VL) in Bangladesh. PLoS Negl Trop Dis. 2017 May 30;11(5):e0005635.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5466346
http://www.ncbi.nlm.nih.gov/pubmed/28558062?tool=bestpractice.com
[158]Goyal V, Mahajan R, Pandey K, et al. Field safety and effectiveness of new visceral leishmaniasis treatment regimens within public health facilities in Bihar, India. PLoS Negl Trop Dis. 2018 Oct 22;12(10):e0006830.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6197645
http://www.ncbi.nlm.nih.gov/pubmed/30346949?tool=bestpractice.com
[164]Sundar S, Sinha PK, Rai M, et al. Comparison of short-course multidrug treatment with standard therapy for visceral leishmaniasis in India: an open-label, non-inferiority, randomised controlled trial. Lancet. 2011 Feb 5;377(9764):477-86.
http://www.ncbi.nlm.nih.gov/pubmed/21255828?tool=bestpractice.com
მონოთერაპიის სხვა ვარიანტები
მილტეფოზინის მონოთერაპია ალტერნატიული ვარიანტია. სამხრეთ აზიაში თავდაპირველი შედეგები ძალიან კარგი იყო, მაგრამ 10 წლის შემდეგ მიზნობრივმა ეფექტურობამ იკლო და ახლა გამოიყენება ალტერნატივად ან კომბინაციაში სხვა მედიკამენტებთან. მონოთერაპიის ეფექტიანობა სამხრეთ აფრიკასა და სამხრეთ ამერიკაში სუბოპტიმალურია.[138]Chakravarty J, Sundar S. Current and emerging medications for the treatment of leishmaniasis. Expert Opin Pharmacother. 2019 Jul;20(10):1251-65.
http://www.ncbi.nlm.nih.gov/pubmed/31063412?tool=bestpractice.com
ხუთვალენტიანი ანტიმონიური პრეპარატები ნორმალური ეფექტურობით გამოიყენება L donovani-ს სამკურნალოდ აღმოსავლეთ აფრიკაში ან L infantum-ის სამკურნალოდ, მაგრამ მეორე რიგის პრეპარატებად მიიჩნევა, როცა სხვა საშუალებებია ხელმისაწვდომი. სამხრეთ აზიაში გავრცელებული რეზისტენტობის გამო ისინი არ გამოიყენება ამ რეგიონში.[107]Burza S, Croft SL, Boelaert M. Leishmaniasis. Lancet. 2018 Sep 15;392(10151):951-70.
http://www.ncbi.nlm.nih.gov/pubmed/30126638?tool=bestpractice.com
პარომომიცინით მონოთერაპიის ეფექტურობამ შეადგინა 95-98%, როდესაც იგი ამფოტერიცინ B-სთან იყო შედარებული ან დამოუკიდებლად გამოიყენებოდა სამხრეთ აზიის ლიმიტირებულ კვლევებში. თუმცა სხვა, მეტად უსაფრთხო და თანაბრად ეფექტური საშუალებების გამო, ეს ვარიანტი განიხილება ნაკლებად სასურველ ალტერნატივად იმ რეგიონებშიც კი, სადაც იგი ხელმისაწვდომია.[165]Sundar S, Jha TK, Thakur CP, et al. Injectable paromomycin for visceral leishmaniasis in India. N Engl J Med. 2007 Jun 21;356(25):2571-81.
https://www.nejm.org/doi/10.1056/NEJMoa066536?url_ver=Z39.88-2003
http://www.ncbi.nlm.nih.gov/pubmed/17582067?tool=bestpractice.com
[166]Jamil KM, Haque R, Rahman R, et al. Effectiveness study of paromomycin IM injection (PMIM) for the treatment of visceral leishmaniasis (VL) in Bangladesh. PLoS Negl Trop Dis. 2015 Oct 23;9(10):e0004118.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4619770
http://www.ncbi.nlm.nih.gov/pubmed/26496648?tool=bestpractice.com
პაციენტებს, რომელთაც საწყის თერაპიაზე არ აქვთ დადებითი შედეგი, ან აღენიშნებათ რეციდივი, უნდა ჩაუტარდეთ სხვა კლასის ანტი-ლეიშმანიური პრეპარატებით (ან მათი კომბინაციით) მკურნალობის სრული კურსი. თუმცა, თუ თავდაპირველი მკურნალობა მოიცავდა ლიპოსომურ ამფოტერიცინ-B-ს, განმეორებითი მკურნალობა შესაძლებელია იმავე მედიკამენტით, უფრო მაღალი ჯამური დოზებით.[8]Aronson N, Herwaldt BL, Libman M, et al. Diagnosis and treatment of leishmaniasis: clinical practice guidelines by the Infectious Diseases Society of America (IDSA) and the American Society of Tropical Medicine and Hygiene (ASTMH). Clin Infect Dis. 2016 Dec 15;63(12):1539-57.
https://academic.oup.com/cid/article/63/12/1539/2645617
http://www.ncbi.nlm.nih.gov/pubmed/27941143?tool=bestpractice.com
[107]Burza S, Croft SL, Boelaert M. Leishmaniasis. Lancet. 2018 Sep 15;392(10151):951-70.
http://www.ncbi.nlm.nih.gov/pubmed/30126638?tool=bestpractice.com
ორსული პაციენტები
მკურნალობა ძალიან მნიშვნელოვანია, რადგან არანამკურნალები ვისცერული ლეიშმანიოზი შესაძლოა ფატალური აღმოჩნდეს როგორც დედისათვის, ასევე ნაყოფისთვისაც.
მწირ მონაცემებზე დაყრდნობით, ლიპოსომური ამფოტერიცინი-B წარმოადგენს უსაფრთხო და ეფექტურ სამკურნალო საშუალებას.[8]Aronson N, Herwaldt BL, Libman M, et al. Diagnosis and treatment of leishmaniasis: clinical practice guidelines by the Infectious Diseases Society of America (IDSA) and the American Society of Tropical Medicine and Hygiene (ASTMH). Clin Infect Dis. 2016 Dec 15;63(12):1539-57.
https://academic.oup.com/cid/article/63/12/1539/2645617
http://www.ncbi.nlm.nih.gov/pubmed/27941143?tool=bestpractice.com
[119]Pagliano P, Carannante N, Rossi M, et al. Visceral leishmaniasis in pregnancy: a case series and a systematic review of the literature. J Antimicrob Chemother. 2005 Feb;55(2):229-33.
https://academic.oup.com/jac/article/55/2/229/856828?login=false
http://www.ncbi.nlm.nih.gov/pubmed/15649998?tool=bestpractice.com
ორსულობის დროს ხუთვალენტიანი ანტიმონიური პრეპარატები არ არის რეკომენდებული სპონტანური აბორტის ან ნაადრევი მშობიარობის მომატებული რისკის გამო. პარომომიცინის უსაფრთხოებაზე ორსულობის დროს მონაცემები არ არსებობს.[8]Aronson N, Herwaldt BL, Libman M, et al. Diagnosis and treatment of leishmaniasis: clinical practice guidelines by the Infectious Diseases Society of America (IDSA) and the American Society of Tropical Medicine and Hygiene (ASTMH). Clin Infect Dis. 2016 Dec 15;63(12):1539-57.
https://academic.oup.com/cid/article/63/12/1539/2645617
http://www.ncbi.nlm.nih.gov/pubmed/27941143?tool=bestpractice.com
თუმცა, თუ სხვა ვარიანტები ხელმისაწვდომი არ არის, მკურნალობა ამ მედიკამენტებით (ცალკეულად ან კომბინაციაში) დასაშვებია ექსპერტის მეთვალყურეობის ქვეშ.
მილტეფოზინის გამოყენებას თავი უნდა აარიდოთ ნაყოფის მხრივ რისკების გამო.
ვისცერული ლეიშმანიოზი: მკურნალობა იმუნოკომპრომისულ პაციენტებში
იმუნოკომპრომისული მდგომარეობა ვისცერული ლეიშმანიოზის მქონე პაციენტებში ყველაზე ხშირია იატროგენული იმუნოსუპრესიის შედეგად (მაგ., მყარი ორგანოს რეციპიენტებში), აივ კოინფექციის დროს. იმუნოკომპრომისული მდგომარეობების ფონზე არა მხოლოდ იზრდება სიმპტომური დაავადების განვითარების რისკი, ასევე მცირდება განკურნების შანსი, რეციდივის რისკის მატების ფონზე.[167]Akuffo H, Costa C, van Griensven J, et al. New insights into leishmaniasis in the immunosuppressed. PLoS Negl Trop Dis. 2018 May 10;12(5):e0006375.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5944929
http://www.ncbi.nlm.nih.gov/pubmed/29746470?tool=bestpractice.com
[168]Gajurel K, Dhakal R, Deresinski S. Leishmaniasis in solid organ and hematopoietic stem cell transplant recipients. Clin Transplant. 2017 Jan;31(1).
http://www.ncbi.nlm.nih.gov/pubmed/27801541?tool=bestpractice.com
საჭიროა კომპლექსური მიდგომა, რაც ითვალისწინებს პარაზიტის საწინააღმდეგო მკურნალობას, იმუნოსუპრესიის მართვას, რეციდივის მონიტორინგს და მეორეულ პროფილაქტიკას.
აივ/შიდსი
ანტირეტროვირუსული თერაპია (მთელი სიცოცხლის მანძილზე) უნდა დაიწყოს ან გაგრძელდეს აივ ინფიცირებულებში, ადგილობრივი გაიდლაინების თანახმად.
ლიპოსომური ამფოტერიცინი-B განიხილება, როგორც საუკეთესო ვარიანტი ვისცერული ლეიშმანიოზის და აივ ინფექციის მქონე პაციენტებისთვის.[8]Aronson N, Herwaldt BL, Libman M, et al. Diagnosis and treatment of leishmaniasis: clinical practice guidelines by the Infectious Diseases Society of America (IDSA) and the American Society of Tropical Medicine and Hygiene (ASTMH). Clin Infect Dis. 2016 Dec 15;63(12):1539-57.
https://academic.oup.com/cid/article/63/12/1539/2645617
http://www.ncbi.nlm.nih.gov/pubmed/27941143?tool=bestpractice.com
[169]National Institutes of Health, Centers for Disease Control and Prevention, HIV Medicine Association, and Infectious Diseases Society of America. Panel on Guidelines for the Prevention and Treatment of Opportunistic Infections in Adults and Adolescents with HIV. Guidelines for the prevention and treatment of opportunistic infections in adults and adolescents with HIV: Leishmaniasis. 2017 [internet publication].
https://clinicalinfo.hiv.gov/en/guidelines/hiv-clinical-guidelines-adult-and-adolescent-opportunistic-infections/leishmaniasis
[170]World Health Organization. WHO technical report series 949: control of the leishmaniases - report of a meeting of the WHO Expert Committee on the control of leishmaniases. 2010 [internet publication].
https://www.who.int/publications/i/item/WHO-TRS-949
იმუნოდეფიციტის მქონე პაციენტებში გამოიყენება უფრო მაღალი საერთო დოზა. თუმცა, მაღალი დოზის ფონზეც კი, მკურნალობა შეიძლება წარუმატებელი იყოს და რეციდივი ხშირია. გამოქვეყნებულ კლინიკურ კვლევაში, რომელიც აღმოსავლეთ აფრიკაში ჩატარდა, ლიპოსომური ამფოტერიცინი B-ს მონოთერაპიის მიზნობრივმა ეფექტურობამ იმ პაციენტებში, რომელთა CD4 უჯრედების რაოდენობის მედიანა უტოლდებოდა 69 უჯრედს/მიკროლიტრზე, შეადგინა მხოლოდ 55%.[171]Diro E, Blesson S, Edwards T, et al. A randomized trial of AmBisome monotherapy and AmBisome and miltefosine combination to treat visceral leishmaniasis in HIV co-infected patients in Ethiopia. PLoS Negl Trop Dis. 2019 Jan 17;13(1):e0006988.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6336227
http://www.ncbi.nlm.nih.gov/pubmed/30653490?tool=bestpractice.com
ამ კონტექსტში უნდა განიხილებოდეს კომბინირებული თერაპია. ზემოთ განხილულ, აღმოსავლეთ აფრიკაში ჩატარებულ ლიპოსომური ამფოტერიცინ-B-ს კლინიკურ კვლევაში, მეორე საკვლევ ჯგუფში ლიპოსომური ამფოტერიცინი B-ს და მილტეფოზინის კომბინაციის მიზნობრივმა ეფექტურობამ შეადგინა 88% იმ პაციენტებს შორის, რომელთა CD4 უჯრედების რაოდენობის მედიანა იყო 54 უჯრედი/მიკროლიტრზე.[171]Diro E, Blesson S, Edwards T, et al. A randomized trial of AmBisome monotherapy and AmBisome and miltefosine combination to treat visceral leishmaniasis in HIV co-infected patients in Ethiopia. PLoS Negl Trop Dis. 2019 Jan 17;13(1):e0006988.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6336227
http://www.ncbi.nlm.nih.gov/pubmed/30653490?tool=bestpractice.com
ინდოეთში, მილტეფოზინისა და ლიპოსომური ამფოტერიცინი B-ის კომბინაცია ასოცირდება 96%-იან მიზნობრივ ეფექტურობასთან, მილტეფოზინის მონოთერაპიასთან შედარებით (85%).[172]Burza S, Mahajan R, Kazmi S, et al. AmBisome monotherapy and combination AmBisome-Miltefosine therapy for the treatment of visceral leishmaniasis in patients coinfected with human immunodeficiency virus in India: a randomized open-label, parallel-Arm, phase 3 trial. Clin Infect Dis. 2022 Oct 12;75(8):1423-32.
https://www.doi.org/10.1093/cid/ciac127
http://www.ncbi.nlm.nih.gov/pubmed/35147680?tool=bestpractice.com
ნატრიუმის სტიბოგლუკონატის და პარომომიცინის კომბინაცია მაღალეფექტურია არა-აივ-კოინფიცირებულ პირებში აღმოსავლეთ აფრიკაში, მაგრამ განკურნების სიხშირე მხოლოდ 56%-ია, ამიტომ არ უნდა გამოიყენოთ, გარდა შემთხვევებისა, როცა ეს ერთადერთი ვარიანტია.[163]Kimutai R, Musa AM, Njoroge S, et al. Safety and effectiveness of sodium stibogluconate and paromomycin combination for the treatment of visceral leishmaniasis in eastern Africa: results from a pharmacovigilance programme. Clin Drug Investig. 2017 Mar;37(3):259-72.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5315726
http://www.ncbi.nlm.nih.gov/pubmed/28066878?tool=bestpractice.com
ჯანმრთელობის მსოფლიო ორგანიზაცია (WHO) რეკომენდაციას უწევს ლიპოსომურ ამფოტერიცინ-B-ს პლუს მილტეფოსინს, ვიდრე ლიპოსომური ამფოტერიცინი-B მონოთერაპიას აივ-ინფექციით დაავადებულ ადამიანებში აღმოსავლეთ აფრიკასა და სამხრეთ-აღმოსავლეთ აზიაში.[62]World Health Organization. WHO guideline for the treatment of visceral leishmaniasis in HIV co-infected patients in East Africa and South-East Asia. June 2022 [internet publication].
https://www.who.int/publications/i/item/9789240048294
ხუთვალენტიანი ანტიმონიური პრეპარატები ალტერნატივაა აივ-ინფიცირებულ პირებში; თუმცა, სიკვდილობა უფრო მაღალია, ვიდრე ამფოტერიცინ B-ს ფონზე. მძიმე გვერდითი ეფექტები უფრო ხშირია.[173]Cota GF, de Sousa MR, Fereguetti TO, et al. Efficacy of anti-leishmania therapy in visceral leishmaniasis among HIV infected patients: a systematic review with indirect comparison. PLoS Negl Trop Dis. 2013 May 2;7(5):e2195.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3642227
http://www.ncbi.nlm.nih.gov/pubmed/23658850?tool=bestpractice.com
[174]Laguna F, Lopez-Velez R, Pulido F, et al. Treatment of visceral leishmaniasis in HIV-infected patients: a randomized trial comparing meglumine antimoniate with amphotericin B. Spanish HIV-Leishmania Study Group. AIDS. 1999 Jun 18;13(9):1063-9.
http://www.ncbi.nlm.nih.gov/pubmed/10397536?tool=bestpractice.com
[175]Delgado J, Macías J, Pineda JA, et al. High frequency of serious side effects from meglumine antimoniate given without an upper limit dose for the treatment of visceral leishmaniasis in human immunodeficiency virus type-1-infected patients. Am J Trop Med Hyg. 1999 Nov;61(5):766-9.
http://www.ncbi.nlm.nih.gov/pubmed/10586909?tool=bestpractice.com
მეორეული პროფილაქტიკა აივ/შიდსის დროს
მეორეული პროფილაქტიკა ანტი-ლეიშმანიური მედიკამენტების გამოყენებით საჭიროა ყველა პაციენტისთვის, რომელთა CD4 უჯრედების რაოდენობა <200-დან 350-მდე უჯრედი/მიკროლიტრის ფარგლებში მერყეობს (ჯანმრთელობის პანამერიკული ორგანიზაცია რეკომენდაციას უწევს CD4-ის უფრო მაღალ ზღურბლს), რადგან რეციდივის რისკი მაღალია.[8]Aronson N, Herwaldt BL, Libman M, et al. Diagnosis and treatment of leishmaniasis: clinical practice guidelines by the Infectious Diseases Society of America (IDSA) and the American Society of Tropical Medicine and Hygiene (ASTMH). Clin Infect Dis. 2016 Dec 15;63(12):1539-57.
https://academic.oup.com/cid/article/63/12/1539/2645617
http://www.ncbi.nlm.nih.gov/pubmed/27941143?tool=bestpractice.com
[145]Pan American Health Organization. Guideline for the treatment of Leishmaniasis in the Americas. Second edition. Sep 2022 [internet publication].
https://iris.paho.org/handle/10665.2/56120
[169]National Institutes of Health, Centers for Disease Control and Prevention, HIV Medicine Association, and Infectious Diseases Society of America. Panel on Guidelines for the Prevention and Treatment of Opportunistic Infections in Adults and Adolescents with HIV. Guidelines for the prevention and treatment of opportunistic infections in adults and adolescents with HIV: Leishmaniasis. 2017 [internet publication].
https://clinicalinfo.hiv.gov/en/guidelines/hiv-clinical-guidelines-adult-and-adolescent-opportunistic-infections/leishmaniasis
[170]World Health Organization. WHO technical report series 949: control of the leishmaniases - report of a meeting of the WHO Expert Committee on the control of leishmaniases. 2010 [internet publication].
https://www.who.int/publications/i/item/WHO-TRS-949
არ არსებობს კონსენსუსი საუკეთესო რეჟიმზე, მაგრამ გაიდლაინები გვირჩევენ სხვადასხვა ვარიანტს.
აღმოსავლეთ აფრიკაში, პენტამიდინით პროფილაქტიკის პროსპექტულ კვლევაში 1 წლის შემდეგ რეციდივის სიხშირე იმ პაციენტებში, რომელთა CD4 უჯრედების რაოდენობა იყო <200 უჯრედი/მიკროლიტრი, აღმოჩნდა 46%; პროფილაქტიკის გარეშე რეციდივის სიხშირე 60-70%-ია.[176]Diro E, Edwards T, Ritmeijer K, et al. Long term outcomes and prognostics of visceral leishmaniasis in HIV infected patients with use of pentamidine as secondary prophylaxis based on CD4 level: a prospective cohort study in Ethiopia. PLoS Negl Trop Dis. 2019 Feb 21;13(2):e0007132.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6400407
http://www.ncbi.nlm.nih.gov/pubmed/30789910?tool=bestpractice.com
არ არსებობს კონსენსუსი მეორეული პროფილაქტიკის დასრულების დროის თაობაზე. ზოგიერთი გაიდლაინით რეკომენდებულია შეჩერება, როცა CD4 უჯრედების რაოდენობა მიაღწევს >200-350 უჯრედს/მიკროლიტრზე, ხოლო სხვა გაიდლაინებით რეკომენდებულია მუდმივი თერაპია, რადგან რეციდივის რისკი გრძელდება. აივ ინფიცირებულ ყველა პაციენტში აუცილებელია ფრთხილი მონიტორინგი რეციდივის ამოსაცნობად.[8]Aronson N, Herwaldt BL, Libman M, et al. Diagnosis and treatment of leishmaniasis: clinical practice guidelines by the Infectious Diseases Society of America (IDSA) and the American Society of Tropical Medicine and Hygiene (ASTMH). Clin Infect Dis. 2016 Dec 15;63(12):1539-57.
https://academic.oup.com/cid/article/63/12/1539/2645617
http://www.ncbi.nlm.nih.gov/pubmed/27941143?tool=bestpractice.com
[169]National Institutes of Health, Centers for Disease Control and Prevention, HIV Medicine Association, and Infectious Diseases Society of America. Panel on Guidelines for the Prevention and Treatment of Opportunistic Infections in Adults and Adolescents with HIV. Guidelines for the prevention and treatment of opportunistic infections in adults and adolescents with HIV: Leishmaniasis. 2017 [internet publication].
https://clinicalinfo.hiv.gov/en/guidelines/hiv-clinical-guidelines-adult-and-adolescent-opportunistic-infections/leishmaniasis
აღმოსავლეთ აფრიკაში რეციდივის სიხშირე მაღალია იმ პაციენტებშიც კი, რომელთა CD4 უჯრედების რაოდენობა შეადგენს >200 უჯრედს/მიკროლიტრზე; წარსულში რეციდივის არსებობა შემდგომი რეციდივის განვითარების ან სიკვდილის მნიშვნელოვანი პრედიქტორია.[176]Diro E, Edwards T, Ritmeijer K, et al. Long term outcomes and prognostics of visceral leishmaniasis in HIV infected patients with use of pentamidine as secondary prophylaxis based on CD4 level: a prospective cohort study in Ethiopia. PLoS Negl Trop Dis. 2019 Feb 21;13(2):e0007132.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6400407
http://www.ncbi.nlm.nih.gov/pubmed/30789910?tool=bestpractice.com
აღმოსავლეთ აფრიკაში, 2 წლიანი დაკვირვების შედეგად, 12-18 თვის განმავლობაში პენტამიდინით პროფილაქტიკის ფონზე დაფიქსირდა 37%-იანი რეციდივის მაჩვენებელი, უმეტესად მათში, ვისაც ბაზილარული CD4-ის დაბალი რაოდენობა ჰქონდა.[177]Diro E, Ritmeijer K, Boelaert M, et al. Long-term clinical outcomes in visceral leishmaniasis/human immunodeficiency virus-coinfected patients during and after pentamidine secondary prophylaxis in Ethiopia: a single-arm clinical trial. Clin Infect Dis. 2018 Jan 18;66(3):444-51.
https://www.doi.org/10.1093/cid/cix807
http://www.ncbi.nlm.nih.gov/pubmed/29020217?tool=bestpractice.com
იმუნოსუპრესიის სხვა ფორმები
მოიცავს მყარი ორგანოს რეციპიენტებს, ლიმფური ან ჰემატოლოგიური ავთვისებიანი სიმსივნეების მქონე პაციენტებს, ან სხვა ჩვენებით იმუნოსუპრესანტებით მკურნალობის შემთხვევებს.
თუ პაციენტი იმუნოსუპრესანტებს იღებს სხვა ჩვენებით, განიხილეთ დოზის შემცირება ან მედიკამენტის შეწყვეტა, თუ ეს შესაძლებელია. აღნიშნული ეფუძნება ექსპერტულ მოსაზრებებას, რადგან მონაცემები მწირია.[168]Gajurel K, Dhakal R, Deresinski S. Leishmaniasis in solid organ and hematopoietic stem cell transplant recipients. Clin Transplant. 2017 Jan;31(1).
http://www.ncbi.nlm.nih.gov/pubmed/27801541?tool=bestpractice.com
მკურნალობა შესაძლებელია სხვადასხვა რეჟიმით, მაგრამ რეკომენდებულია ლიპოსომური ამფოტერიცინ-B, განსაკუთრებით მყარი ორგანოების რეციპიენტებში.[8]Aronson N, Herwaldt BL, Libman M, et al. Diagnosis and treatment of leishmaniasis: clinical practice guidelines by the Infectious Diseases Society of America (IDSA) and the American Society of Tropical Medicine and Hygiene (ASTMH). Clin Infect Dis. 2016 Dec 15;63(12):1539-57.
https://academic.oup.com/cid/article/63/12/1539/2645617
http://www.ncbi.nlm.nih.gov/pubmed/27941143?tool=bestpractice.com
[145]Pan American Health Organization. Guideline for the treatment of Leishmaniasis in the Americas. Second edition. Sep 2022 [internet publication].
https://iris.paho.org/handle/10665.2/56120
მიუხედავად იმისა, რომ რეციდივი ხშირია, განსაკუთრებით მყარი ორგანოს რეციპიენტებში (დაახლ. 25%), მეორეული პროფილაქტიკის როლის შესახებ არსებული მონაცემები მწირია. IDSA/ASTMH გაიდლაინებით რეკომენდებული არ არის მეორეული პროფილაქტიკა პაციენტებში, რომელთაც რეციდივი არ ჰქონიათ, მაგრამ მცირე რეტროსპექტულ, შემთხვევა-კონტროლის კვლევაში რეციდივის რისკი მეორეული პროფილაქტიკის ფონზე მცირდებოდა 27%-ით.[8]Aronson N, Herwaldt BL, Libman M, et al. Diagnosis and treatment of leishmaniasis: clinical practice guidelines by the Infectious Diseases Society of America (IDSA) and the American Society of Tropical Medicine and Hygiene (ASTMH). Clin Infect Dis. 2016 Dec 15;63(12):1539-57.
https://academic.oup.com/cid/article/63/12/1539/2645617
http://www.ncbi.nlm.nih.gov/pubmed/27941143?tool=bestpractice.com
[178]Clemente W, Vidal E, Girão E, et al. Risk factors, clinical features and outcomes of visceral leishmaniasis in solid-organ transplant recipients: a retrospective multicenter case-control study. Clin Microbiol Infect. 2015 Jan;21(1):89-95.
https://www.clinicalmicrobiologyandinfection.com/article/S1198-743X(14)00008-1/fulltext
http://www.ncbi.nlm.nih.gov/pubmed/25636932?tool=bestpractice.com
მეორეული პროფილაქტიკა განიხილეთ ინდივიდუალურად, განსაკუთრებით, თუ პაციენტს აქვს რეციდივის ანამნეზი და იმუნოსუპრესიული მდგომარეობა.
იმუნოსუპრესირებულ პაციენტებში, რომელთაც რეციდივი აღენიშნებათ, მისაღებია მკურნალობა ამფოტერიცინ-B-ით, თუნდაც იმ შემთხვევაში, როცა პირველადი თერაპია ამავე მედიკამენტითაა ჩატარებული, რადგან წარუმატებლობის მიზეზად ამ შემთხვევაში მიიჩნევა იმუნოლოგიური ფაქტორი და არა მედიკამენტის მიმართ რეზისტენტობა. დასაშვებია სხვა ვარიანტების და კომბინაციური თერაპიების მოსინჯვა.[8]Aronson N, Herwaldt BL, Libman M, et al. Diagnosis and treatment of leishmaniasis: clinical practice guidelines by the Infectious Diseases Society of America (IDSA) and the American Society of Tropical Medicine and Hygiene (ASTMH). Clin Infect Dis. 2016 Dec 15;63(12):1539-57.
https://academic.oup.com/cid/article/63/12/1539/2645617
http://www.ncbi.nlm.nih.gov/pubmed/27941143?tool=bestpractice.com
ორსული პაციენტები
მკურნალობა ძალიან მნიშვნელოვანია, რადგან არანამკურნალები ვისცერული ლეიშმანიოზი შესაძლოა ფატალური აღმოჩნდეს როგორც დედისათვის, ასევე ნაყოფისთვისაც.
მწირ მონაცემებზე დაყრდნობით, ლიპოსომური ამფოტერიცინი-B წარმოადგენს უსაფრთხო და ეფექტურ სამკურნალო საშუალებას.[8]Aronson N, Herwaldt BL, Libman M, et al. Diagnosis and treatment of leishmaniasis: clinical practice guidelines by the Infectious Diseases Society of America (IDSA) and the American Society of Tropical Medicine and Hygiene (ASTMH). Clin Infect Dis. 2016 Dec 15;63(12):1539-57.
https://academic.oup.com/cid/article/63/12/1539/2645617
http://www.ncbi.nlm.nih.gov/pubmed/27941143?tool=bestpractice.com
[119]Pagliano P, Carannante N, Rossi M, et al. Visceral leishmaniasis in pregnancy: a case series and a systematic review of the literature. J Antimicrob Chemother. 2005 Feb;55(2):229-33.
https://academic.oup.com/jac/article/55/2/229/856828?login=false
http://www.ncbi.nlm.nih.gov/pubmed/15649998?tool=bestpractice.com
შესაძლებელია ამფოტერიცინის სხვა ფორმების გამოყენება, თუ ლიპოსომური ამფოტერიცინი ხელმისაწვდომი არ არის.
კალა-აზარის-შემდგომი კანის ლეიშმანიოზი
კალა-აზარის შემდგომი კანის ლეიშმანიოზის მართვასთან დაკავშირებით ჩატარებულია რამდენიმე კონტროლირებადი კვლევა. მსუბუქი და საშუალო სიმძიმის კალა-აზარის-შემდგომი კანის ლეიშმანიოზი თვითგანკურნებადია აღმოსავლეთ აფრიკის წარმომავლობის პაციენტების უმეტესობაში, 3-12 თვის პერიოდში. მკურნალობა ნაჩვენებია აღმოსავლეთ აფრიკელ პაციენტებში მძიმე, არათვითგანკურნებადი კალა-აზარის-შემდგომი, ან ინდური კალა-აზარის-შემდგომი ფორმების დროს და იმუნოკომპრომისულ პაციენტებში.[6]Zijlstra EE, Musa AM, Khalil EA, et al. Post-kala-azar dermal leishmaniasis. Lancet Infect Dis. 2003 Feb;3(2):87-98.
http://www.ncbi.nlm.nih.gov/pubmed/12560194?tool=bestpractice.com
სამხრეთ აზიაში მილტეფოზინი რეკომენდებულია პირველი რიგის თერაპიად კალა-აზარის შემდგომი ლეიშმანიოზის დროს.[170]World Health Organization. WHO technical report series 949: control of the leishmaniases - report of a meeting of the WHO Expert Committee on the control of leishmaniases. 2010 [internet publication].
https://www.who.int/publications/i/item/WHO-TRS-949
მეტა-ანალიზმა გამოავლინა მიზნობრივი ეფექტურობის დაქვეითება, რაც შეინიშნება თერაპიის 12 კვირაზეც კი, და უსაფრთხოების პრობლემები (მაგ., დარღვევები თვალების მხრივ, მათ შორის სიბრმავე, წყლულოვანი კერატიტი, ბუნდოვანი ხედვა, ფოტოფობია) მკურნალობის ხანგრძლივი კურსების შემთხვევაში.[179]Pijpers J, den Boer ML, Essink DR, et al. The safety and efficacy of miltefosine in the long-term treatment of post-kala-azar dermal leishmaniasis in South Asia - a review and meta-analysis. PLoS Negl Trop Dis. 2019 Feb 11;13(2):e0007173.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6386412
http://www.ncbi.nlm.nih.gov/pubmed/30742620?tool=bestpractice.com
[180]World Health Organization. Statement on miltefosine - potential ocular disorders in patients treated with miltefosine for post-kala-azar dermal leishmaniasis (PKDL). Feb 2022 [internet publication].
https://www.who.int/news/item/10-02-2022-statement-on-miltefosine---potential-ocular-disorders-in-patients-treated-with-miltefosine-for-post-kala-azar-dermal-leishmaniasis-(pkdl)
ამფოტერიცინი-B განიხილება მეორე რიგის პრეპარატად სამხრეთ აზიაში.[170]World Health Organization. WHO technical report series 949: control of the leishmaniases - report of a meeting of the WHO Expert Committee on the control of leishmaniases. 2010 [internet publication].
https://www.who.int/publications/i/item/WHO-TRS-949
ლიპოსომური ამფოტერიცინი-B გარკვეული მიზნობრივი ეფექტურობით ხასიათდება, რეგიონის ზოგიერთი ლიმიტირებული კვლევის მიხედვით.[181]Basher A, Maruf S, Nath P, et al. Case report: treatment of widespread nodular post kala-azar dermal leishmaniasis with extended-dose liposomal amphotericin B in Bangladesh – a series of four cases. Am J Trop Med Hyg. 2017 Oct;97(4):1111-5.
https://www.ajtmh.org/configurable/content/journals$002ftpmd$002f97$002f4$002farticle-p1111.xml?t:ac=journals%24002ftpmd%24002f97%24002f4%24002farticle-p1111.xml
http://www.ncbi.nlm.nih.gov/pubmed/28820697?tool=bestpractice.com
[182]Musa AM, Khalil EA, Mahgoub FA, et al. Efficacy of liposomal amphotericin B (AmBisome) in the treatment of persistent post-kala-azar dermal leishmaniasis (PKDL). Ann Trop Med Parasitol. 2005 Sep;99(6):563-9.
http://www.ncbi.nlm.nih.gov/pubmed/16156969?tool=bestpractice.com
თუმცა, მოლეკულური ანალიზით ვლინდება პარაზიტების ხელახალი გააქტიურება ლიპოსომური ამფოტერიცინ-B-ით მკურნალობიდან 6 თვეში, რაც არ აღინიშნება მილტეფოზინის ფონზე.[183]Moulik S, Chaudhuri SJ, Sardar B, et al. Monitoring of parasite kinetics in Indian post-kala-azar dermal leishmaniasis. Clin Infect Dis. 2018 Jan 18;66(3):404-10.
https://academic.oup.com/cid/article/66/3/404/4157560
http://www.ncbi.nlm.nih.gov/pubmed/29020350?tool=bestpractice.com
ინდოეთში, ლიპოსომური ამფოტერიცინი B-ის და მილტეფოზინის კომბინაციურმა 45-დღიანმა თერაპიამ აჩვენა 100%-იანი მიზნობრივი ეფექტურობა მილტეფოზინის 90-დღიან მონოთერაპიასთან შედარებით (75% ეფექტურობა).[184]Ramesh V, Dixit KK, Sharma N, et al. Assessing the efficacy and safety of liposomal amphotericin B and miltefosine in combination for treatment of post kala-azar dermal leishmaniasis. J Infect Dis. 2020 Feb 3;221(4):608-17.
https://www.doi.org/10.1093/infdis/jiz486
http://www.ncbi.nlm.nih.gov/pubmed/31854451?tool=bestpractice.com
ორსული პაციენტები
