ეტიოლოგია
ენდეთ მითითებებს
ebpracticenet პრიორიტეტი მიანიჭეთ ჩამოთვლილ ადგილობრივ გაიდლაინებს:
Cancer du côlon : diagnostic, traitement et suiviავტორი: KCEბოლო გამოქვეყნება: 2014Dikkedarmkanker: diagnose, behandeling en follow-upავტორი: KCEბოლო გამოქვეყნება: 2014კოლორექტული კიბო გენეტიკური და გარემო ფაქტორების კომპლექსური ურთიერთქმედების შედეგს წარმოადგენს.
გენეტიკური ფაქტორები:
კოლორექტული კიბოს შემთხვევების უმეტესობა სპორადულია და არა ოჯახური, თუმცა მიუხედავად ამისა, ასაკის შემდეგ, ოჯახური ანამნეზი წარმოადგენს ყველაზე მნიშვნელოვან რისკფაქტორს.
ერთი დაავადებული პირველი რიგის მონათესავე პირის შემთხვევაში, პაციენტში კოლორექტული კიბოს განვითარების ფარდობითი რისკი შეადგენს 2.24-ს.[10] აღნიშნული მაჩვენებელი 3.97-მდე იზრდება 2 დასენიანებული პირველი რიგის ნათესავის შემთხვევაში.[10] კოლორექტალური პოლიპების მქონე პაციენტების და-ძმები და ბავშვები ასევე არიან მსხვილი ნაწლავის კიბოს განვითარების რისკის ქვეშ (შანსების თანაფარდობა 1.40, 95% CI 1.35-დან 1.45-მდე).[11]
კიბოს ოჯახური სინდრომები, როგორებიცაა ოჯახური ადენომატოზური პოლიპოზი (FAP) და ლინჩის სინდრომი, შეადგენს მსხვილი ნაწლავის კიბოს საერთო რაოდენობის 2-5%-ს.[12][13] [Figure caption and citation for the preceding image starts]: გენეტიკური სინდრომების მქონე პაციენტებში კოლორექტული კიბოს კუმულაციური ინციდენტობა ასაკის მიხედვით შედარებული ზოგად მოსახლეობასთან (FAP = ოჯახური ადენომატოზური პოლიპოზი, HNPCC = მემკვიდრული არა-პოლიპოზური ცოლორექტული კიბო)Winawer SW, Fletcher RH, Mille L, et al. AGA guidelines: colorectal cancer screening: clinical guidelines and rationale. Gastroenterology. 1997 Feb;112(2):594 [Citation ends].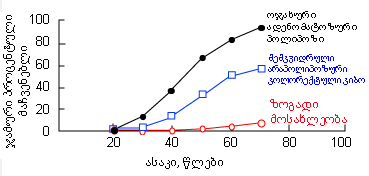 გარემო ფაქტორები:
გარემო ფაქტორები:
აშშ-ში კოლორექტალური კიბოს ნახევარზე მეტი (55%) განპირობებულია პოტენციურად მოდიფიცირებადი რისკფაქტორებით.[5]
ნორმალურწონიან პირებთან შედარებით, სიმსუქნე ზრდის მსხვილი ნაწლავის კიბოს განვითარების რისკს და აგრეთვე დაკავშირებულია სიკვდილობის უფრო მაღალ მაჩვენებელთან.[14][15][16][17][18] ერთ სისტემატურ მიმოხილვაში, სიმსუქნე ასოცირდება ადრეული კოლორექტალური კიბოს (50 წლამდე) გაზრდილ რისკთან ქალებში.[19]
სიმსუქნე, მაღალი კალორიების მიღება და ფიზიკური უმოქმედობა ალბათ სინერგიული რისკ-ფაქტორებია კოლორექტალური კიბოს განვითარებისთვის.[14][18][20][21] ერთი პროსპექტული და ხანგრძლივი დაკვირვების მქონე კვლევის თანახმად, დიდი რაოდენობით წითელი და გადამუშავებული ხორცის მიღება დაკავშირებულია კოლორექტული კიბოს განვითარების მაღალ რისკთან.[22][23][24] გარკვეული მტკიცებულებების მიხედვით, მამაკაცებში კოლორექტულ კიბოს შესაძლოა ზრდიდეს ნახშირწყლების დიდი რაოდენობით მიღება.[25]
კვლევათა უმეტესობა (თუმცა არა ყველა) მიუთითებს კოლორექტული კიბოს განვთარების რისკსა და ბოჭკოთი მდიდარი საკვების მიღებას შორის უკუპროპორციულ დამოკიდებულებაზე.[26][27][28]
[  ]
სიგარეტის მოწევა, ალკოჰოლის ზომიერი და ჭარბი მოხმარება და D ვიტამინის დაბალი დონე ასევე ასოცირდება კოლორექტალური კიბოს გაზრდილ რისკთან.[29][30][31][32]
]
სიგარეტის მოწევა, ალკოჰოლის ზომიერი და ჭარბი მოხმარება და D ვიტამინის დაბალი დონე ასევე ასოცირდება კოლორექტალური კიბოს გაზრდილ რისკთან.[29][30][31][32]
პათოფიზიოლოგია
უმეტეს შემთხვევაში კოლორექტული კიბო ვითარდება დისპლაზიური ადენომატოზური პოლიპიდან. ამ დროს მიმდინარეობს მრავასაფექხურიანი პროცესი, რომელიც მოიცავს სიმსივნის-სუპრესორული და დნმ-ის რეპარაციული სხვადასხვა გენის ინაქტივაციასა და ონკოგენების გააქტიურებას. აღნიშნული ცვლილებები ხელს უწყობს მსხვილი ნაწლავის ეპითელური უჯრედების სელექტიურ პროლიფერაციას და შემდგომ მათ ადენომატოზურ პოლიპად, საბოლოოდ კი კოლორექტულ კიბოდ გარდაქმნას.[33]
არსებობს გენომის არასტაბილურობის სამი ძირითადი გზა, რომელიც იწვევს კოლორექტალურ კიბოს: ქრომოსომული არასტაბილურობა (CIN), მიკროსატელიტური არასტაბილურობა (MSI) და CpG კუნძულის მეთილატორის ფენოტიპური გზები (CIMP). CIN გზა, რომელიც ხასიათდება ჰეტეროზიგოტიურობის და ანევპლოიდიის დაკარგვით, წარმოადგენს კოლორექტალური კიბოს შემთხვევების აბსოლუტურ უმრავლესობას (კოლორექტალური სპორადული კიბოს შემთხვევების 65%-70%).[34]
MSI არის დეფიციტური შეუსაბამობის აღდგენის (MMR) სისტემის მოლეკულური თითის ანაბეჭდი, რომელიც ახასიათებს კოლორექტალური კიბოს დაახლოებით 15%-ს. MSI სტატუსი გვაძლევს პროგნოზულ პასუხს 5-ფტორურაცილზე და ასევე შეიძლება განსაზღვროს რეაგირება სხვა კოლორექტალურ მკურნალობაზე, როგორიცაა იმუნოთერაპია. დეფიციტური MMR-ის იდენტიფიცირება მნიშვნელოვან გავლენას ახდენს პაციენტის შედეგებსა და მენეჯმენტზე.[35]
CIMP არის კოლორექტალური კიბოს ქვეჯგუფი, რომელიც ვითარდება ეპიგენეტიკური არასტაბილურობის გზით, მაგრამ ხასიათდება პრომოტორ CpG კუნძულების საიტების ჰიპერმეთილაციით, რაც იწვევს სიმსივნის სუპრესორული გენების ინაქტივაციას.[36]
ნაწლავის ადენომატოზური პოლიპოზი(APC) სიმსივნის სუპრესორული გენი
გამეტების მუტაციები განაპირობებს მსხვილი ნაწლავის კიბოს ზემოთ აღნიშულ ოჯახურ სინდრომებს, მაშინ, როდესაც სპორადული შემთხვევები ვითარდება სომატური გენების მუტაციების თანმიმდევრული დაგროვების შედეგად. გამეტებში ნაწლავის ადემონატოზური პოლიპოზის (APC) სიმსივნის-სუპრესორული გენის მუტაცია იწვევს აუტოსომურ დომინანტურ სინდრომს - ოჯახურ ადენომატოზურ პოლიპოზს. კლინიკურად დაავადება იმ შემთხვევაში ვლინდება, როდესაც ნაწლავის ადენომატოზური პოლიპოზის ერთი ალელის დამემკვიდრებულ მუტაციას მეორე ალელის მუტაცია ან დელეცია მოჰყვება. APC მუტაციები ასევე ხშირად შეინიშნება სპორადულ ადენომებში (30% - 70%) და სპორადულ სიმსივნეებში (72%), რაც მიუთითებს იმაზე, რომ APC ფუნქციის დაკარგვა გადამწყვეტი ადრეული მოვლენაა კოლორექტალური კიბოს სიმსივნეში.
APC არის სიმსივნის სუპრესორული გენი, რომელიც არეგულირებს β-კატენინს. APC ფუნქციის დაკარგვა იწვევს β-კატენინის დაგროვებას, რაც იწვევს Wnt სიგნალის გააქტიურებას და უჯრედების ზრდისა და პროლიფერაციის სტიმულირებას. KRAS მუტაცია, რომელიც იწვევს KRAS აქტივაციას, ხშირად არის შემდეგი ნაბიჯი CIN გზაზე, რასაც მოჰყვება მუტაციები TGFβ, P53 და PIK3CA გზებში.[34]
მეტასტაზები
კოლორექტული კიბო ადგილობრივად ლიმფურ კვანძებში ვრცელდება, ენტერული ვენური დრენაჟის საშუალებით ღვიძლში, არტერიული სისხლის მეშვეობით კი ფილტვებში და უფრო იშვიათად ძვლებსა და ტვინში. თუმცა, იქიდან გამომდინარე, რომ სისტემური ქიმიოთერაპიის შედეგად გადარჩენის პერიოდი გახანგრძლივდა, უფრო გახშირდა ძვლისა და ტვინის მეტასტაზების შემთხვევები.[37][38]
კლასიფიკაცია
ამერიკის ერთობლივი კომიტეტი კიბოს TNM სტადირების სისტემა (ვერსია 9)[2]
კიბოს ამერიკული ერთობლივი კომიტეტი (AJCC) აღწერს დაავადების მასშტაბებს შემდეგი ანატომიური ფაქტორების საფუძველზე: პირველადი სიმსივნის ზომა და გავრცელება (T); რეგიონალური ლიმფური კვანძის ჩართულობა (N); და შორეული მეტასტსაზების არსებობა ან არარსებობა (M). არაანატომიური პროგნოზული ფაქტორები (მაგ. სიმსივნის ხარისხი, ბიომარკერები) შეიძლება გამოყენებულ იქნას გარკვეული კიბოს შემთხვევაში სტადიის დასამატებლად.
ამ მასალის გამოყენება ექვემდებარება ჩვენს განცხადებას