Etiologia
A doença de Lyme é causada por espiroquetas pertencentes ao complexo Borrelia burgdorferi sensu lato (sl), que consiste em cerca de 20 genoespécies com uma estrutura genômica complexa. Nem todas as espécies de B burgdorferi sl são patogênicas.[1] A doença de Lyme na América do Norte é causada principalmente por Borrelia burgdorferi sensu stricto e é transmitida pelos carrapatos Ixodes scapularis e I pacificus. Uma nova genoespécie patogênica de B burgdorferi sl, B mayonii, foi descrita no centro-oeste setentrional dos EUA. Este patógeno foi isolado e geneticamente identificado em humanos e carrapatos I scapularis. A B mayonii causa borreliose de Lyme com espiroquetemia excepcionalmente alta.[15] A doença de Lyme na Europa e na Ásia é causada predominantemente por B afzelii e B garinii.[1]
As espécies de Borrelia são espiroquetas (bactérias móveis em forma de espiral) com 7 a 11 flagelos e uma membrana externa contendo uma abundância de proteínas de superfície de membrana externa (Osp). Essas proteínas, designadas pelas letras A a F, são codificadas por plasmídeos. As OspA e OspC são potencialmente úteis para o desenvolvimento de vacinas contra a doença de Lyme.[16]
Os maiores reservatórios da B burgdorferi são os camundongos, ratos do campo, esquilos, pássaros e outros animais pequenos. Os cervos não são um reservatório importante, mas são um hospedeiro importante para carrapatos Ixodes adultos, os vetores de transmissão. Esses carrapatos estão em grande parte confinados às zonas climáticas temperadas do hemisfério norte.[1]
O I scapularis é o vetor primário no nordeste e centro-oeste dos EUA. A transmissão em seu estágio ninfal, que prevalece na primavera e no início do verão, é mais provável transmitir a infecção por meio de picada, embora a infecção possa ser adquirida nos 3 estágios (larval, ninfal e adulto).
O I ricinus é o principal vetor na Europa e o I persulcatus é o principal vetor em grandes partes da Rússia e da Ásia.[1] Na costa oeste dos EUA, o I pacificus é o vetor predominante.[17] Na Europa, 12% das ninfas e 15% dos carrapatos I ricinus adultos estão infectados com B burgdorferi sl, e 2% a 3% dos humanos desenvolvem a doença de Lyme após uma picada de carrapato. A incidência é semelhante nos EUA.[1]
[Figure caption and citation for the preceding image starts]: Carrapato de veados (ou carrapato de patas pretas), Ixodes scapularis, subindo em uma folhaBiblioteca de Imagens do CDC [Citation ends]. [Figure caption and citation for the preceding image starts]: Sob grande ampliação, a micrografia eletrônica de varredura colorida digitalmente retrata três bactérias Borrelia burgdorferi anaeróbias gram-negativas, derivadas de uma cultura puraBiblioteca de Imagens do CDC [Citation ends].
[Figure caption and citation for the preceding image starts]: Sob grande ampliação, a micrografia eletrônica de varredura colorida digitalmente retrata três bactérias Borrelia burgdorferi anaeróbias gram-negativas, derivadas de uma cultura puraBiblioteca de Imagens do CDC [Citation ends].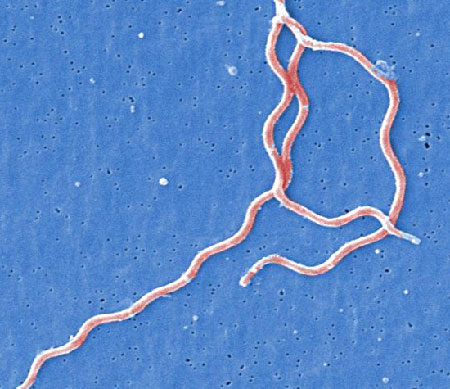
Fisiopatologia
A B burgdorferi é inoculada na pele através da alimentação do carrapato Ixodes, geralmente após o carrapato ter se alimentado por mais de 48 horas. A infecção inicial é estabelecida no local da mordida do carrapato. Após a inoculação cutânea, a B burgdorferi move-se através da matriz extracelular ligando-se aos componentes, como os proteoglicanos derivados de células, e interagindo com a decorina, os glicosaminoglicanos e a fibronectina. Isso leva à expansão da erupção cutânea.[18]A Borrelia se dissemina rapidamente da pele para outros órgãos. Ela se replica, mata as células hospedeiras e emerge através da membrana dessas células. Alguns dias ou semanas após a infecção, a Borrelia foi encontrada no sangue, líquido cefalorraquidiano, miocárdio, retina, músculo, osso, baço, fígado, meninges e cérebro.[19]
A resposta imune do hospedeiro à Borrelia integra os mecanismos humorais e mediados por células. A maioria dos pacientes tem uma resposta de anticorpo IgM contra a OspC ou a proteína flagelar (41-kDa) da Borrelia dentro de alguns dias após o início. As respostas imunes humorais podem ser limitadas inicialmente, e um nível clinicamente detectável de anticorpos pode ocorrer tardiamente. O tratamento precoce com antibióticos pode atrasar ou anular a resposta do linfocítica B. Na fase crônica, anticorpos contra uma variedade de epítopos da Borrelia tornam-se detectáveis. Embora a resposta de células B na fase crônica seja robusta, ela não previne futuras infecções.[18]
Os sintomas clinicamente persistentes, como os de inflamação crônica das articulações, foram atribuídos à autoimunidade. As linfocinas e os linfócitos T ativos do fenótipo da célula T auxiliar (células CD4) exercem um papel importante na patogênese da artrite de Lyme.[18]
O uso deste conteúdo está sujeito ao nosso aviso legal